
11 天前

11 天前
当你饿到头晕、血液里胆固醇超标,或是体内钙离子浓度异常时,你的细胞正经历一场隐秘的危机:负责合成蛋白质、储存钙离子的内质网,会有局部区域因过载而损伤。过去科学家只知道细胞会启动「内质网自噬」清理这些受损片段,但没人能说清,细胞是如何精准定位这些「垃圾」,又是怎么发出清理指令的。直到中科院生物物理研究所张宏团队的新研究,才第一次把这个过程的完整链条铺在了我们面前——这场细胞自救的触发开关,竟然是两个不起眼的机械感知通道。
你可以把内质网想象成细胞里的大型工厂,其中片状的车间储存着大量钙离子,是工厂的「能源库」。当细胞遭遇饥饿、胆固醇失衡等应激时,这些高钙车间会率先扩张受损——就像过载的电路会发烫一样。
研究人员用超分辨多模态活细胞成像技术观察到,此时两种机械感知通道蛋白PIEZO1和TRPV1会精准聚集在这些受损区域。它们就像贴在车间墙上的烟雾报警器,能感知到钙离子浓度变化带来的膜张力改变,随即触发局部钙离子快速释放,形成短暂的「钙瞬变」信号。
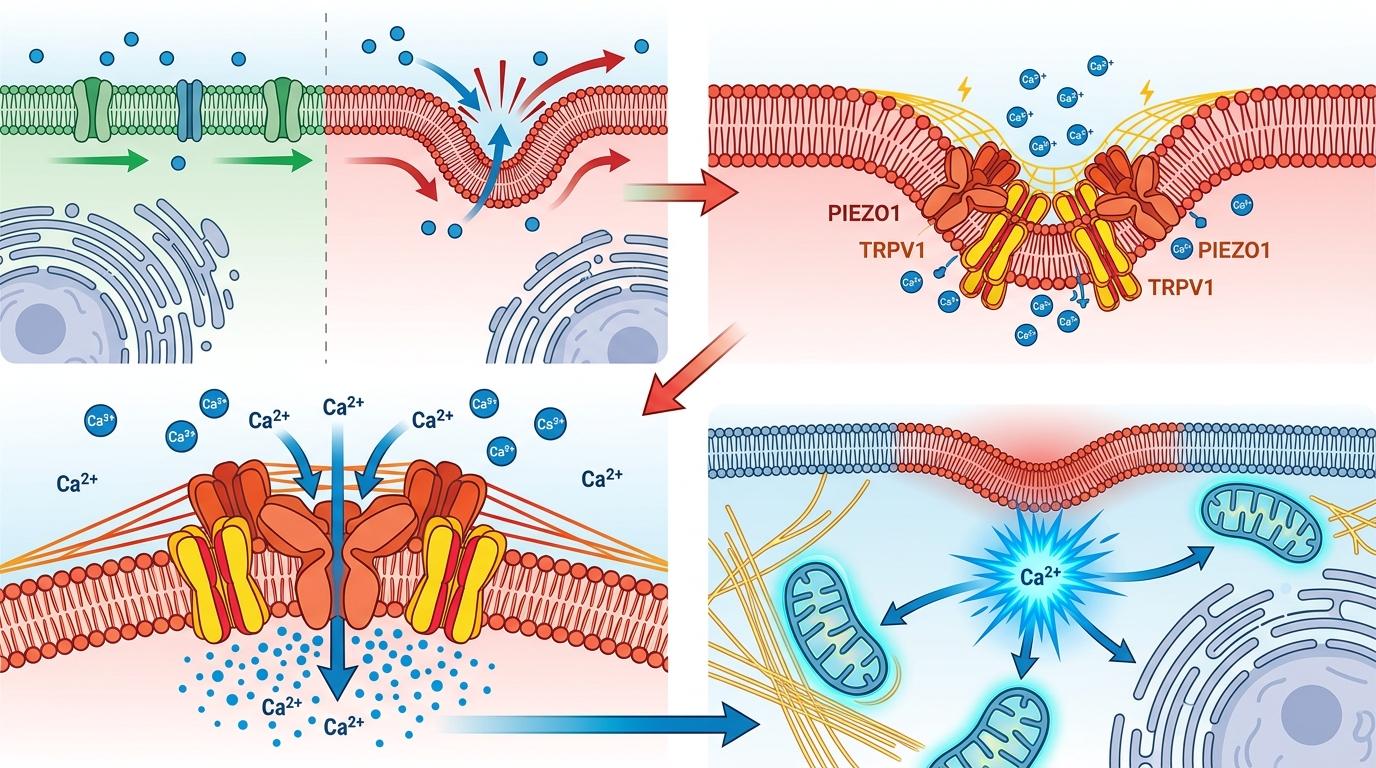
这不是普通的信号波动。
这种快速、局部的钙信号会直接激活自噬起始复合物FIP200,让它们像被磁铁吸引一样聚集在一起,发生液-液相分离——就像一堆碎铁突然被吸成了一块磁铁,成为启动自噬的核心位点。
更让人意外的是,包裹受损内质网的自噬小体膜,并不是从其他细胞器调来的「垃圾袋」,而是内质网自己重塑而来——相当于工厂自己拆了受损车间的墙壁,把废料打包起来。
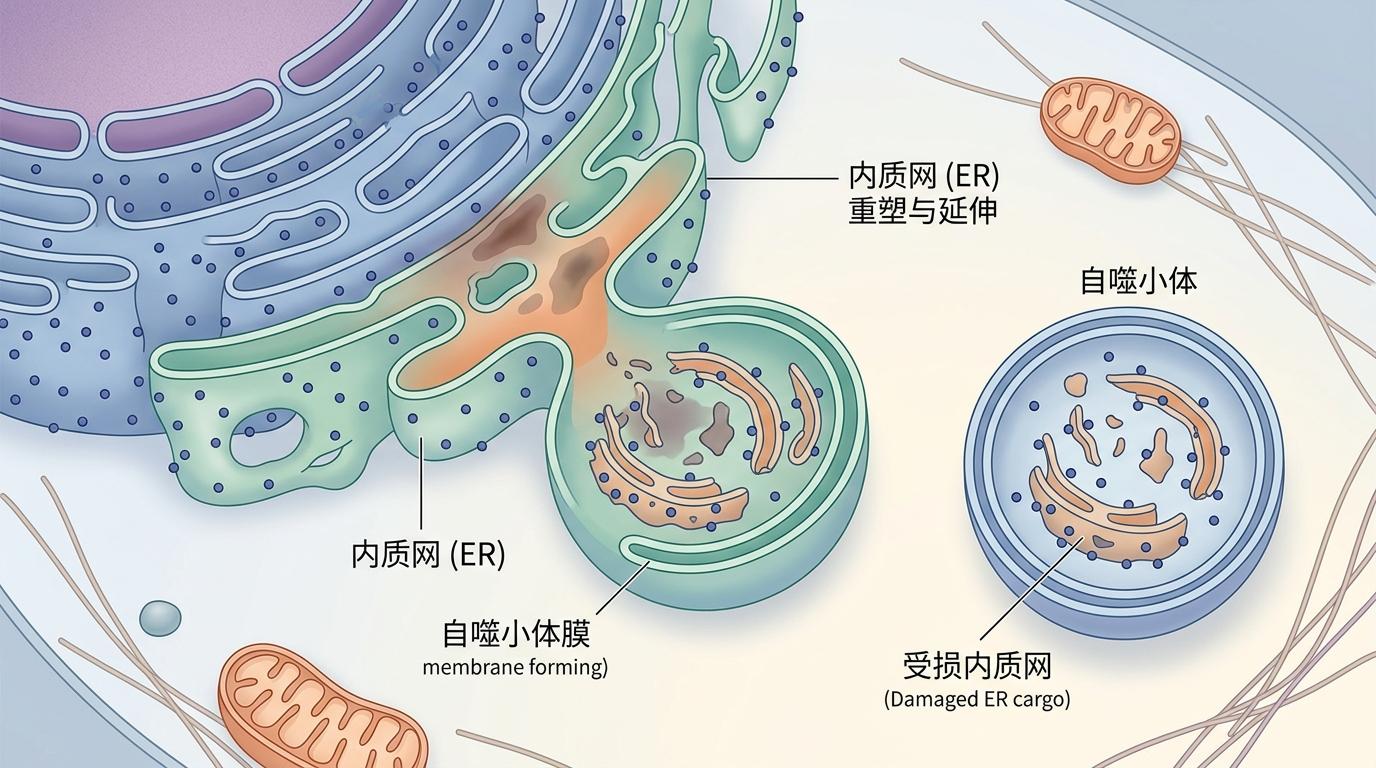
通过冷冻电子断层扫描,研究人员清晰地看到,自噬小体膜和受损的内质网膜直接相连,是内质网通过自我折叠、断裂形成的双层膜结构。这个过程只需要两个关键蛋白的配合:内质网自噬受体FAM134B负责标记受损区域,脂化LC3则像打包带一样把膜结构固定成自噬小体。
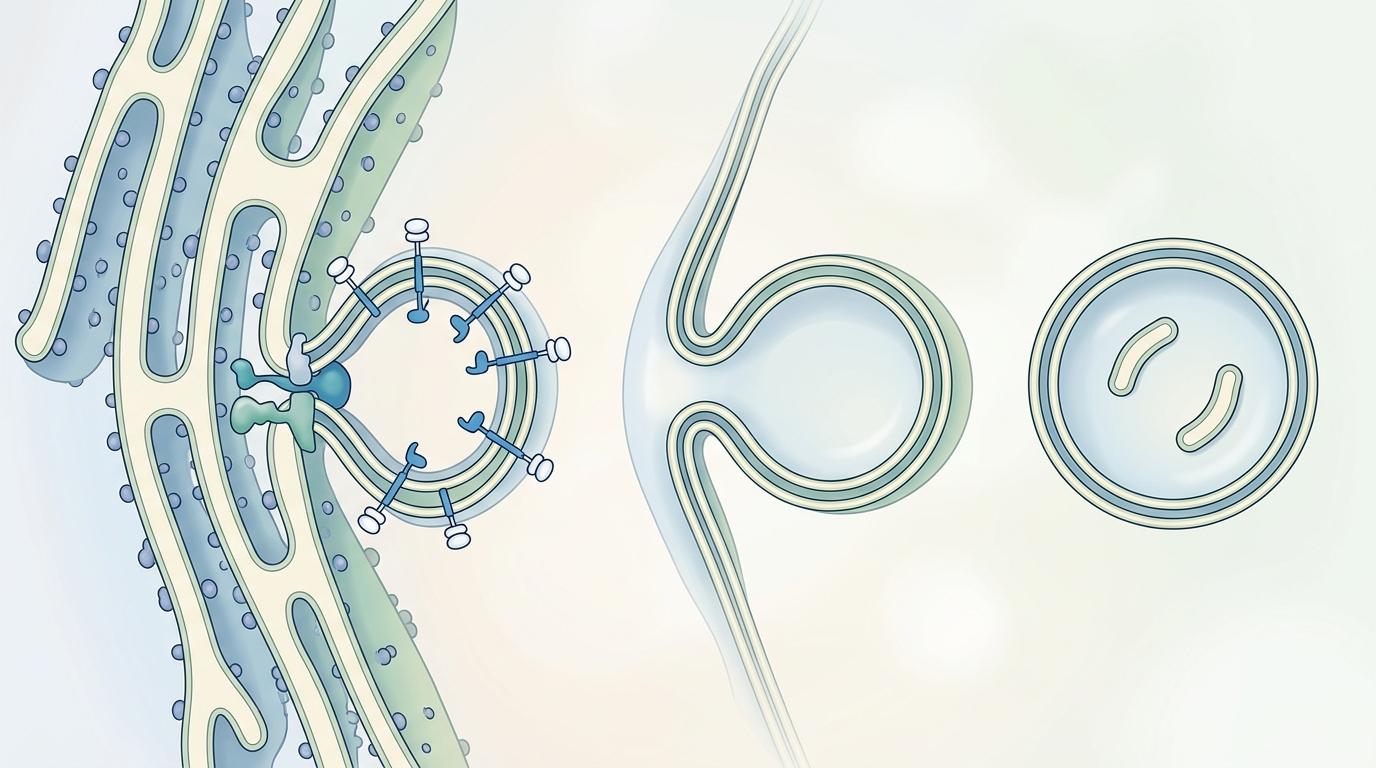
这和传统自噬路径完全不同——经典自噬必需的ATG14和ATG9蛋白,在这里根本派不上用场。这意味着细胞进化出了一套专门针对内质网的「快速清理通道」,不需要调动全局资源,就能精准解决局部问题。
不过目前的研究还存在局限:这种自噬路径在神经细胞、免疫细胞等不同类型细胞中是否存在差异,还需要进一步验证;而机械感知通道如何精准识别不同程度的内质网损伤,也是尚未解开的谜题。
内质网功能障碍和自噬异常,早已被证实和神经退行性疾病、癌症、代谢病密切相关:比如FAM134B基因突变会导致遗传性感觉神经病变,而阿尔茨海默病患者的大脑中,内质网自噬的关键蛋白常常出现异常聚集。
这次的发现,相当于给这些疾病的治疗找到了一个新的「开关」。如果能通过药物调控PIEZO1和TRPV1的活性,或是增强钙瞬变信号,就能精准激活内质网自噬,清理受损的细胞结构。比如在神经退行性疾病中,或许可以通过这种方式减少异常蛋白的积累;在肿瘤细胞中,甚至可能通过过度激活自噬,让肿瘤细胞「自我清理」走向死亡。
当然,这一切还处于实验室阶段。要把这个分子机制转化为临床治疗手段,还需要解决很多问题:如何让药物精准作用于特定细胞的内质网,如何避免过度激活自噬导致正常细胞受损,这些都是未来研究需要跨越的门槛。
我们总说细胞是生命的基本单位,但直到今天,我们才刚刚看清它应对危机的精密逻辑:从感知损伤到发出信号,再到精准清理,每一步都像经过精心设计的流水线。
「细胞自救的开关,藏在钙的波动里。」这句话或许能帮我们记住这个发现——它不仅填补了细胞自噬机制的空白,更让我们意识到,那些看似微小的分子信号,可能就是打开疾病治疗大门的钥匙。未来,当我们再谈论疾病治疗时,或许会更多地把目光投向细胞内部,那些正在发生的、隐秘的自救故事。
点击充电,成为大圆镜下一个视频选题!