
10 天前

10 天前
晚期癌症病房里,常有这样的患者:他们还能抬手喝水,却连翻身都懒得动;明明有想吃的东西,却连坐起来的力气都「不想有」。过去我们总把这种「冷漠」归为身体虚弱、意志消沉,甚至是对死亡的妥协——但2025年两项发表在《Science》和《Cell》的研究,彻底推翻了这个想当然的结论。这种让患者失去生活意愿的「冷漠」,根本不是心理问题,而是肿瘤释放的炎症分子,悄悄劫持了大脑里的一条神经回路。
你可以把这条被劫持的神经回路想象成公司的「动力传输链」:脑干后角区是公司的「前台」,负责接收全身的信号;臂旁核是「部门主管」,把信号传给黑质网状部这个「项目经理」;最后由腹侧被盖区的多巴胺神经元——也就是公司的「奖金发放员」——给负责行动的伏隔核发「努力奖励」。
但真实的机制比这更精确:当肿瘤生长时,血液里的白细胞介素-6(IL-6)会飙升。这种炎症分子能直接穿透血脑屏障,精准激活脑干后角区的IL-6受体神经元。这些神经元随即向臂旁核发送信号,臂旁核再激活黑质网状部的抑制性神经元,最终让腹侧被盖区的多巴胺神经元「罢工」——伏隔核拿不到「奖金」,自然就失去了付出努力的动力。
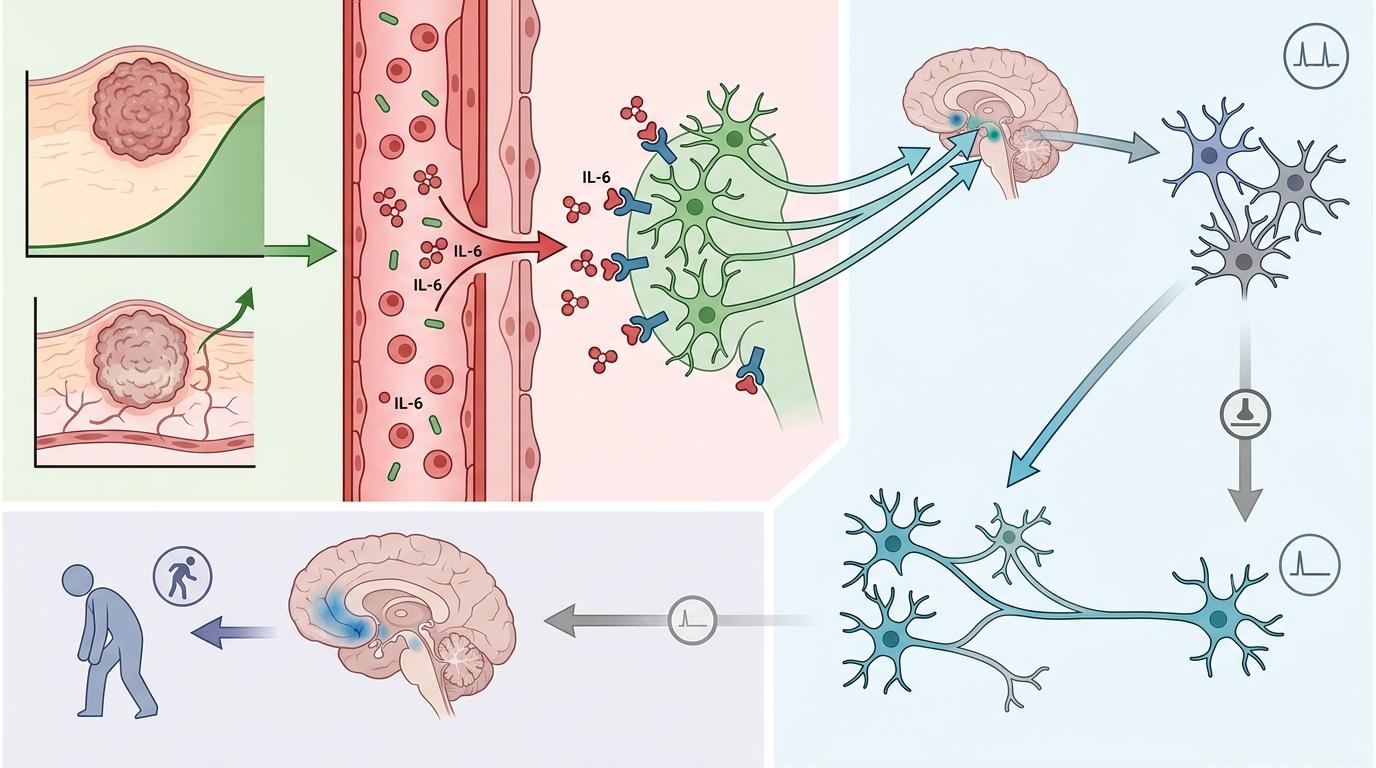
实验数据直截了当地证明了这一点:
如果说神经回路是「冷漠」的幕后黑手,那肝脏就是「消瘦」的直接执行者。过去我们以为肝脏只是恶病质的受害者,海德堡大学的研究却发现,它其实是主动参与消耗的「指挥官」。
肿瘤引发的炎症会让肝脏的昼夜节律基因REV-ERBα显著下调,就像关掉了肝脏的「正常作息开关」。失去REV-ERBα调控的肝脏会开始疯狂分泌三种肝因子:LBP、ITIH3和IGFBP1。这些分子进入血液后,会直接命令肌肉细胞分解蛋白质、脂肪细胞加速产热,甚至让心肌细胞也开始消耗自身能量。
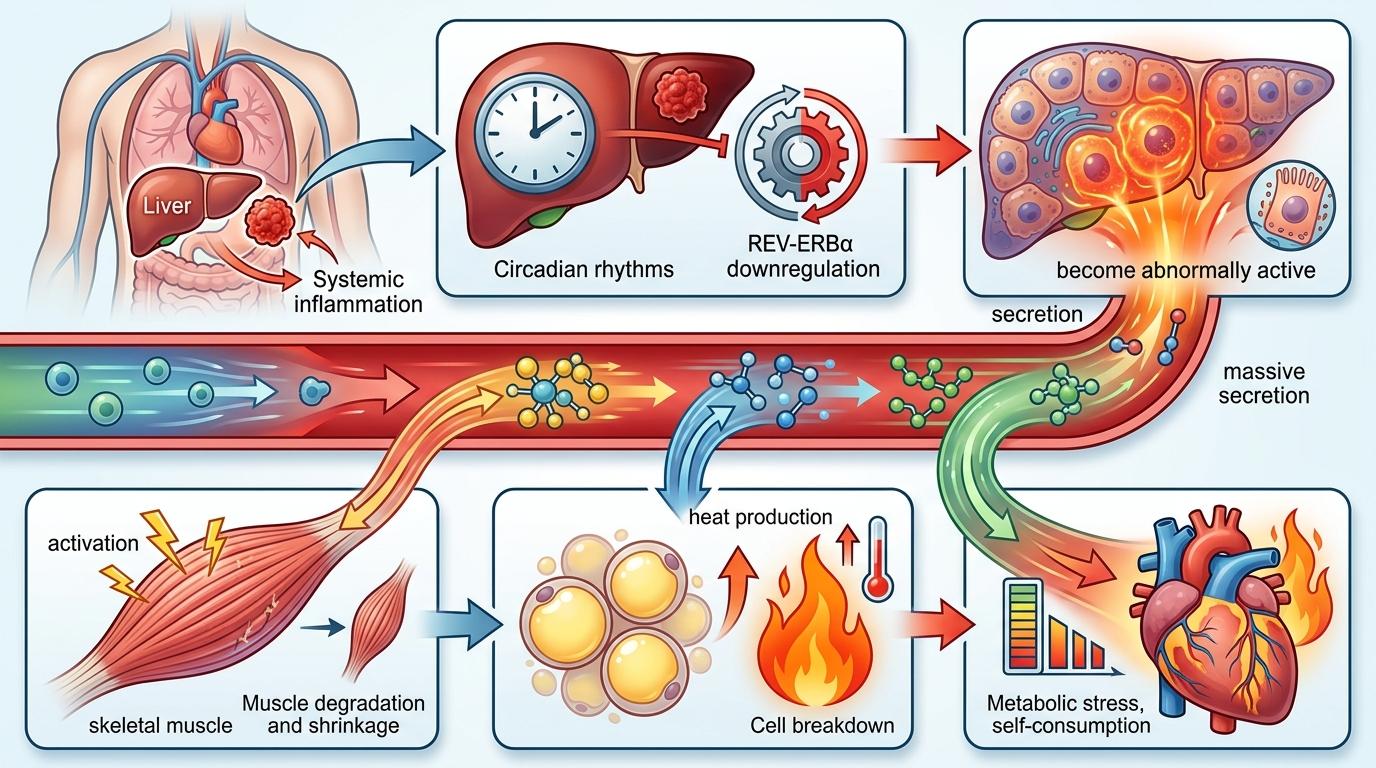
最关键的是IGFBP1,它会阻断胰岛素样生长因子1的合成信号——就像拆掉了肌肉的「修复补丁」,让肌肉只能持续流失而无法再生。在人类恶病质患者的血液里,这三种肝因子的水平比健康人高出2-3倍,而且数值越高,患者的肌肉萎缩速度越快。
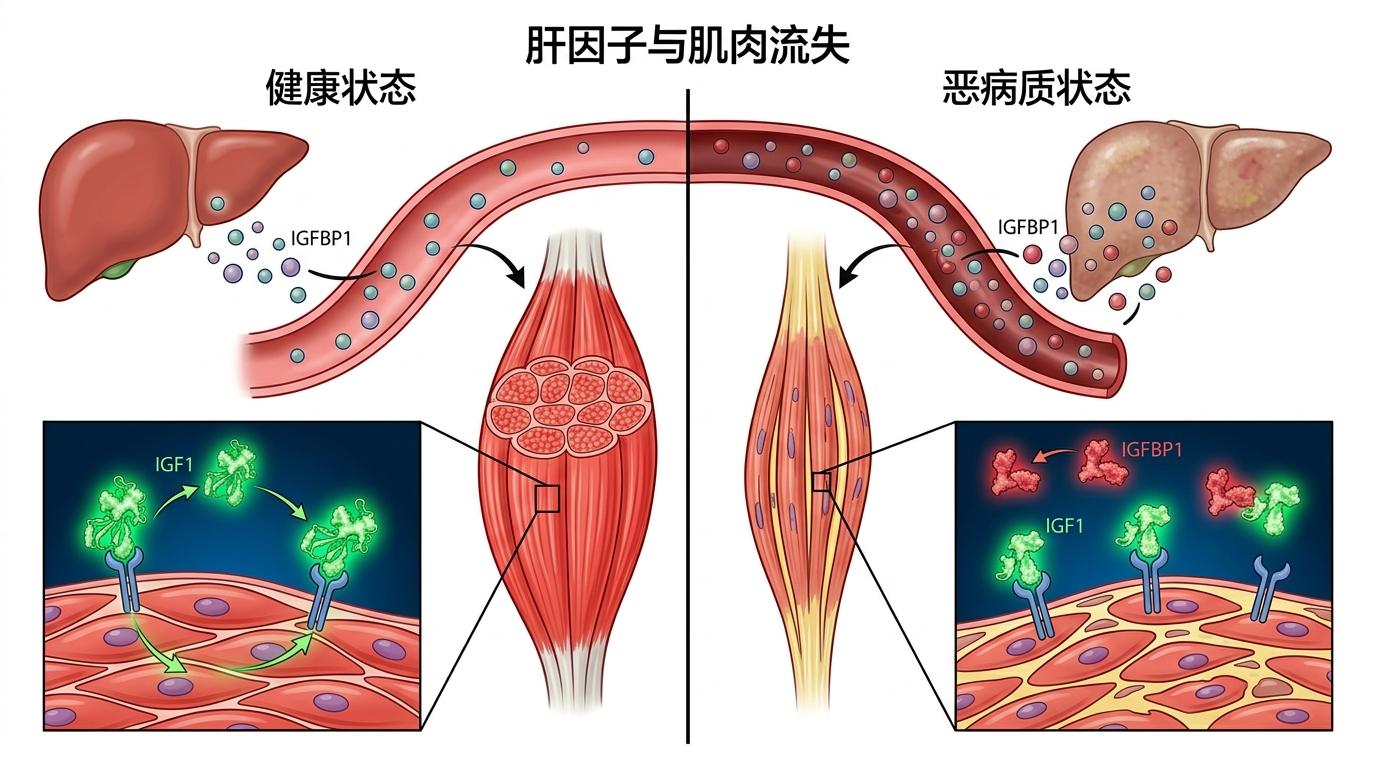
更值得警惕的是,即使使用抗IL-6药物控制了神经炎症,肝脏的这种「消耗指令」依然会继续——这意味着要逆转恶病质,必须同时瞄准神经回路和肝脏代谢两个靶点。
目前针对恶病质的治疗还停留在「缓解」而非「逆转」阶段:抗IL-6抗体已经在小范围临床试验中改善了患者的冷漠症状,但无法阻止体重下降;针对REV-ERBα的药物还在动物实验阶段,距离临床应用至少需要3-5年。
还有很多未解之谜:为什么同样是IL-6升高,有的患者只表现为消瘦,有的却同时出现严重的冷漠?除了IL-6,肿瘤分泌的GDF15、TNF-α等炎症分子是否也在影响其他神经回路?脑内的免疫细胞是否会和炎症分子协同作用,放大这种病理信号?
更现实的问题是,这些针对神经回路的干预会不会有副作用?比如过度激活多巴胺系统会不会导致患者出现躁狂症状?如何精准调控肝脏的基因表达,而不影响它的正常代谢功能?这些都是未来研究必须跨越的障碍。
过去我们总把恶病质患者的「不想活」当成生命走到尽头的自然表现,但这两项研究告诉我们:那不是放弃,而是大脑被炎症劫持后的被动状态。
炎症才是恶病质的真正操盘手。它一边让大脑失去行动的动力,一边让肝脏加速身体的消耗,把患者拖进一个看不见的恶性循环里。
未来的恶病质治疗,或许不再是单纯的营养补充或心理疏导,而是精准地「解绑」被劫持的神经回路,「叫停」肝脏的消耗指令——让那些连翻身都懒得动的患者,重新有坐起来喝一口水的意愿。这不是奇迹,而是科学正在一步步靠近的真相。
点击充电,成为大圆镜下一个视频选题!