对抗知识焦虑,从看懂这条开始
App 下载
原来脂肪产热的刹车,藏在这两个基因里
UCP1蛋白|能量代谢调控|产热脂肪细胞|RUNX2基因|RUNX1基因|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
UCP1蛋白|能量代谢调控|产热脂肪细胞|RUNX2基因|RUNX1基因|分子细胞生物学|生命科学
当你在零下的街头搓手哈气时,身体里正悄悄发生一场能量争夺战——一部分脂肪细胞会放弃储存热量,转而把多余能量烧成热量维持体温。这种能“燃烧脂肪产热”的细胞,就是科学家对抗肥胖的希望。但过去没人搞懂,是什么在死死按住这些产热细胞的“启动键”。直到广州医科大学和中山大学的团队,在《自然·通讯》上揪出了两个关键的“刹车分子”:RUNX1和RUNX2。它们不是默默旁观的路人,是直接阻碍产热脂肪发育的“拦路虎”。为什么我们的身体要给自己留这样的刹车?这得从细胞里的精密调控说起。
你可以把产热脂肪细胞的发育,看成一场需要精准启动的基因派对——UCP1、PGC1α这些“派对核心”要准时到场,才能让脂肪开始烧能量。而RUNX1和RUNX2,就是专门来砸场的不速之客,只是它们的捣乱方式完全不同。
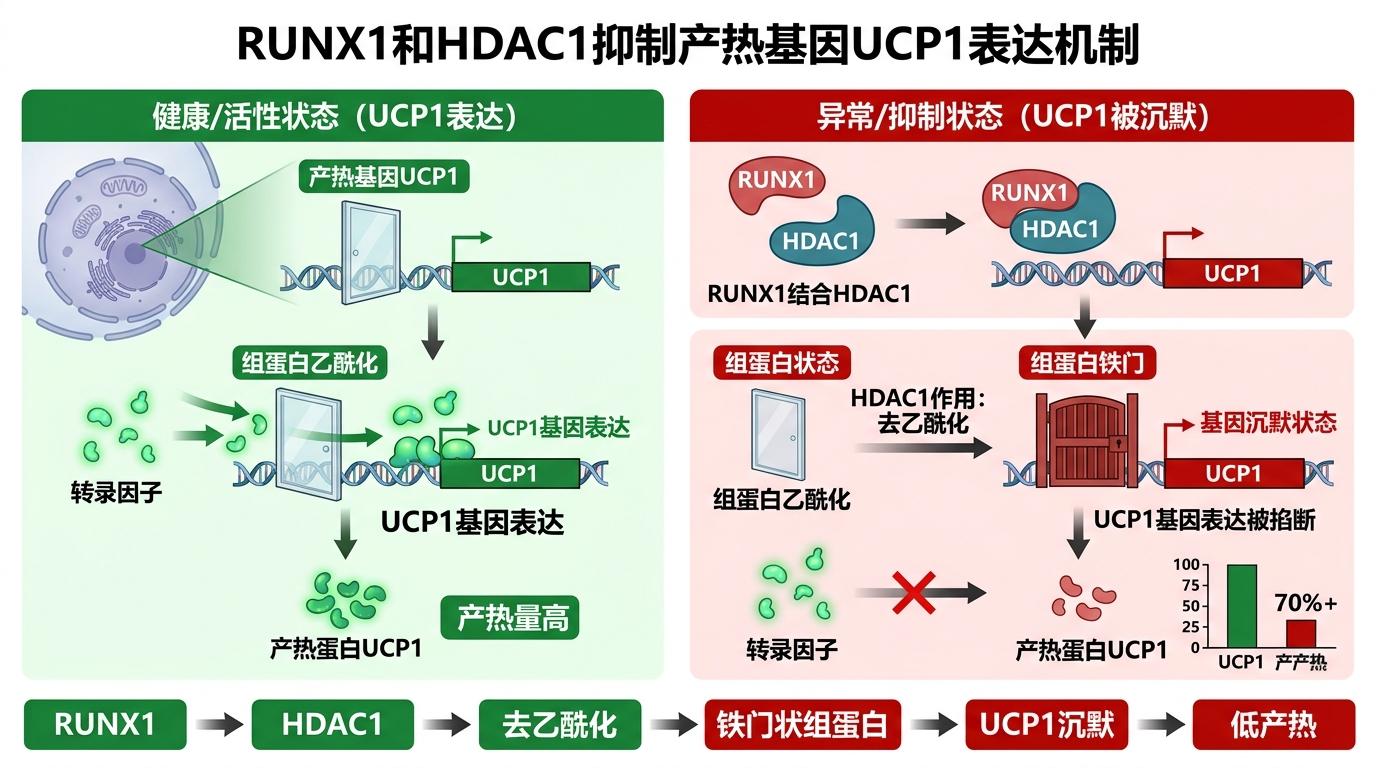
先看RUNX1,它是个“搞装修的”——会找来组蛋白去乙酰化酶HDAC1,给产热基因的“家门”刷上一层“黑漆”。这里的组蛋白乙酰化,就像是给基因的调控区安上一扇透明玻璃门,能让转录因子轻松进去启动基因;而HDAC1的作用,就是把这扇玻璃门换成密不透风的铁门,让产热基因彻底“沉默”。实验数据显示,RUNX1一旦和HDAC1结合,产热基因UCP1的表达量会直接下降70%以上,相当于把派对的主电源给掐了。
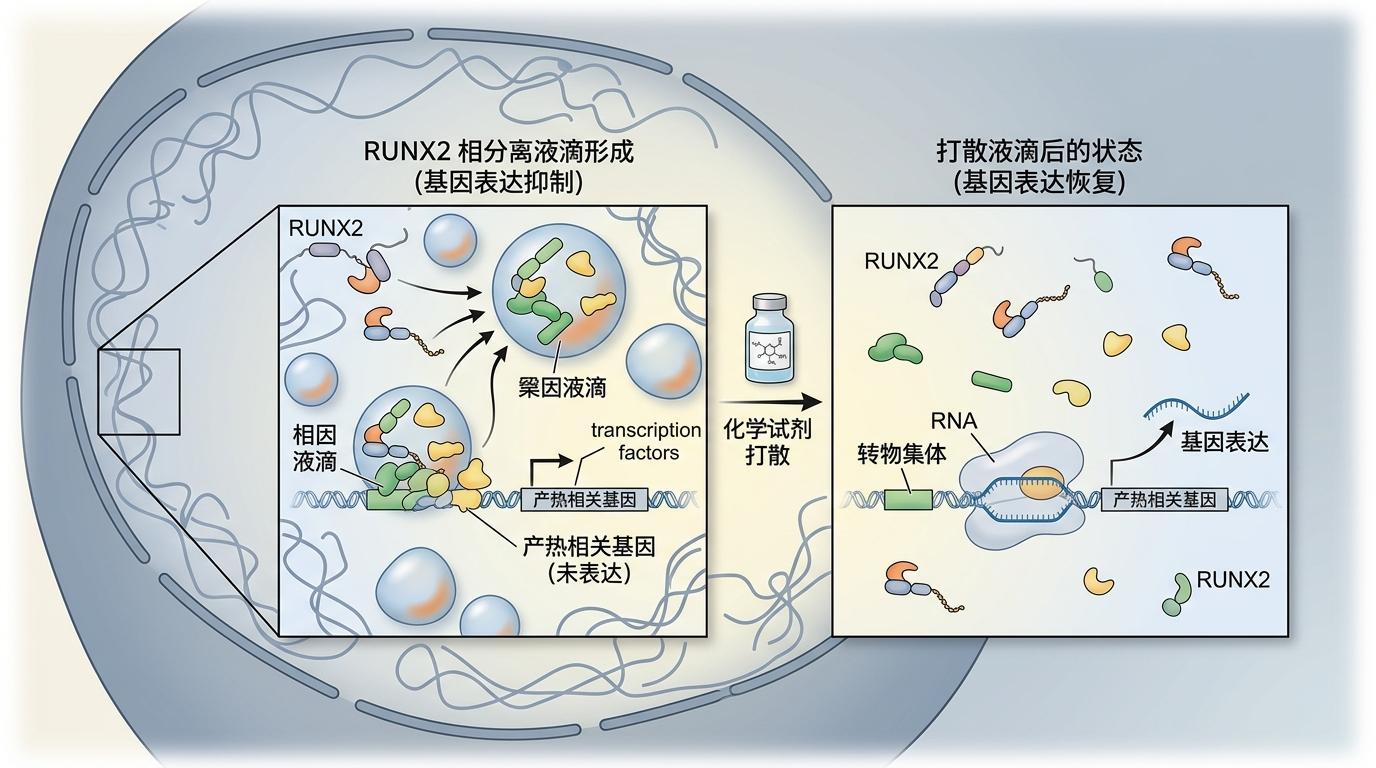
RUNX2的路子则更“高端”,它靠的是“相分离”——就像把一堆乐高积木倒进水里,密度大的会沉底聚成一团。RUNX2自带一段没有固定结构的“柔软尾巴”,能在细胞里自发聚成一个个小液滴,把产热相关的转录因子和调控元件全“关”进这些液滴里,让它们没法接触到基因。只要用化学试剂打散这些液滴,产热基因的表达立刻就能恢复大半。
这两个刹车还挺“识时务”:当身体遇到寒冷刺激,它们的表达量会快速下降,给产热脂肪让路。但如果它们一直处于高表达状态,就会牢牢按住产热的开关,让多余脂肪只囤不烧。
为了确认这两个刹车的作用,科学家在小鼠身上做了“拆刹车”实验:在脂肪细胞里特异性敲除RUNX1或RUNX2。
结果很直接——两种小鼠的皮下脂肪都长出了更多米色脂肪细胞(那种能产热的“好脂肪”),线粒体数量翻了一倍多,基础代谢率也提高了15%左右。但有意思的是,两个刹车的影响并不完全一样:敲除RUNX1的小鼠,不仅代谢变快,还能更好地控制血糖,胰岛素敏感性提高了30%;而敲除RUNX2的小鼠,虽然产热增加,但对全身血糖的影响要弱得多。
反过来,如果给小鼠的脂肪细胞强行“装刹车”——过表达RUNX1或RUNX2,产热基因的表达会被直接压制,就算把小鼠放进4℃的冷箱里,它们的体温也会比正常小鼠低2℃以上,产热脂肪几乎完全“罢工”。
更关键的是,科学家找到了能“松刹车”的药物:用药理学抑制剂降低RUNX1/2的活性后,小鼠的能量消耗明显增加,吃同样多的高脂饲料,体重比对照组轻了20%,血糖和血脂水平也回到了正常范围。这意味着,这两个刹车分子,完全可以成为减肥药的精准靶点。
不过,这两个刹车分子的故事还没讲完。
RUNX1和RUNX2本来就不是脂肪细胞的“专属分子”——RUNX1是造血系统的关键调控因子,RUNX2更是骨骼发育的核心开关。这意味着,要开发靶向它们的减肥药,必须精准瞄准脂肪细胞,不能影响到血液和骨骼的正常功能。比如,要是不小心抑制了骨骼里的RUNX2,可能会导致骨质疏松,这显然是不能接受的。
另外,临床数据显示,肥胖患者脂肪组织里的RUNX1表达量确实比正常人高,但RUNX2的表达差异并不明显。这说明RUNX1可能是更主要的“肥胖元凶”,但为什么RUNX2在人体和小鼠身上的表现不一样,还需要更多临床研究来解释。
还有个更有意思的发现:RUNX1的高表达还和脂肪组织的炎症有关,它会促进TNF-α、IL-6这些炎症因子的释放,而炎症正是导致胰岛素抵抗的关键原因。这意味着,抑制RUNX1不仅能让脂肪产热,还能同时改善脂肪炎症,相当于“一箭双雕”。
我们总以为肥胖只是“管不住嘴迈不开腿”的结果,但细胞里的每一个分子开关,都在悄悄影响着能量的流向。RUNX1和RUNX2这两个“刹车分子”的发现,让我们终于摸到了产热脂肪调控的核心逻辑——原来身体里从来都不缺能烧脂肪的细胞,只是它们被悄悄按住了开关。
脂肪不是只会囤能量的“懒细胞”,它是个能根据环境调整状态的“智能组织”。未来的减肥药,或许不用再靠抑制食欲或拉肚子来减重,只要轻轻松开细胞里的那道刹车,就能让多余脂肪自己“烧”掉。
控住脂肪刹车,就能握住代谢钥匙。