对抗知识焦虑,从看懂这条开始
App 下载
肠道细菌能造胆汁酸,还能救脓毒症孩子
华中科技大学|胆汁酸硫酸化|DCA-3S|肠道细菌|脓毒症儿童|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
华中科技大学|胆汁酸硫酸化|DCA-3S|肠道细菌|脓毒症儿童|感染性疾病|医学健康
全球每5个死亡的人里,就有1个死于脓毒症——而其中近一半是5岁以下的孩子。这些小患者的身体会对感染做出过度反应,肠道像破了洞的口袋,毒素和细菌直接涌入血液,引发全身炎症和器官衰竭。过去我们只能靠抗生素和输液硬扛,却始终补不上那个破洞。直到华中科技大学和武汉纺织大学的团队发现,我们之前完全找错了方向:不是要从外面补,而是要唤醒肠道里一种不起眼的细菌,以及它制造的一种特殊胆汁酸——DCA-3S。
我们以前一直以为,胆汁酸的硫酸化修饰只能在肝脏里完成——就像工厂里的精加工车间,给胆汁酸加上硫酸根,让它能顺利代谢排出。但这次的研究直接推翻了这个定论:肠道里的棉子糖肠球菌(Enterococcus raffinosus),才是DCA-3S这种硫酸化胆汁酸的主要生产者,贡献了至少80%的产量。
你可以把这个过程想象成:肝脏生产出基础款的胆汁酸原料,送到肠道这个“代工厂”,棉子糖肠球菌就像里面的特种技工,给原料加上硫酸根的“保护套”,变成了DCA-3S。这种经过改造的胆汁酸,和未修饰的脱氧胆酸(DCA)完全是两种“性格”——DCA会破坏肠道上皮的紧密连接,像一把钥匙捅开肠道的防御;而DCA-3S反而会加固这些连接蛋白,把破掉的口袋重新缝好。
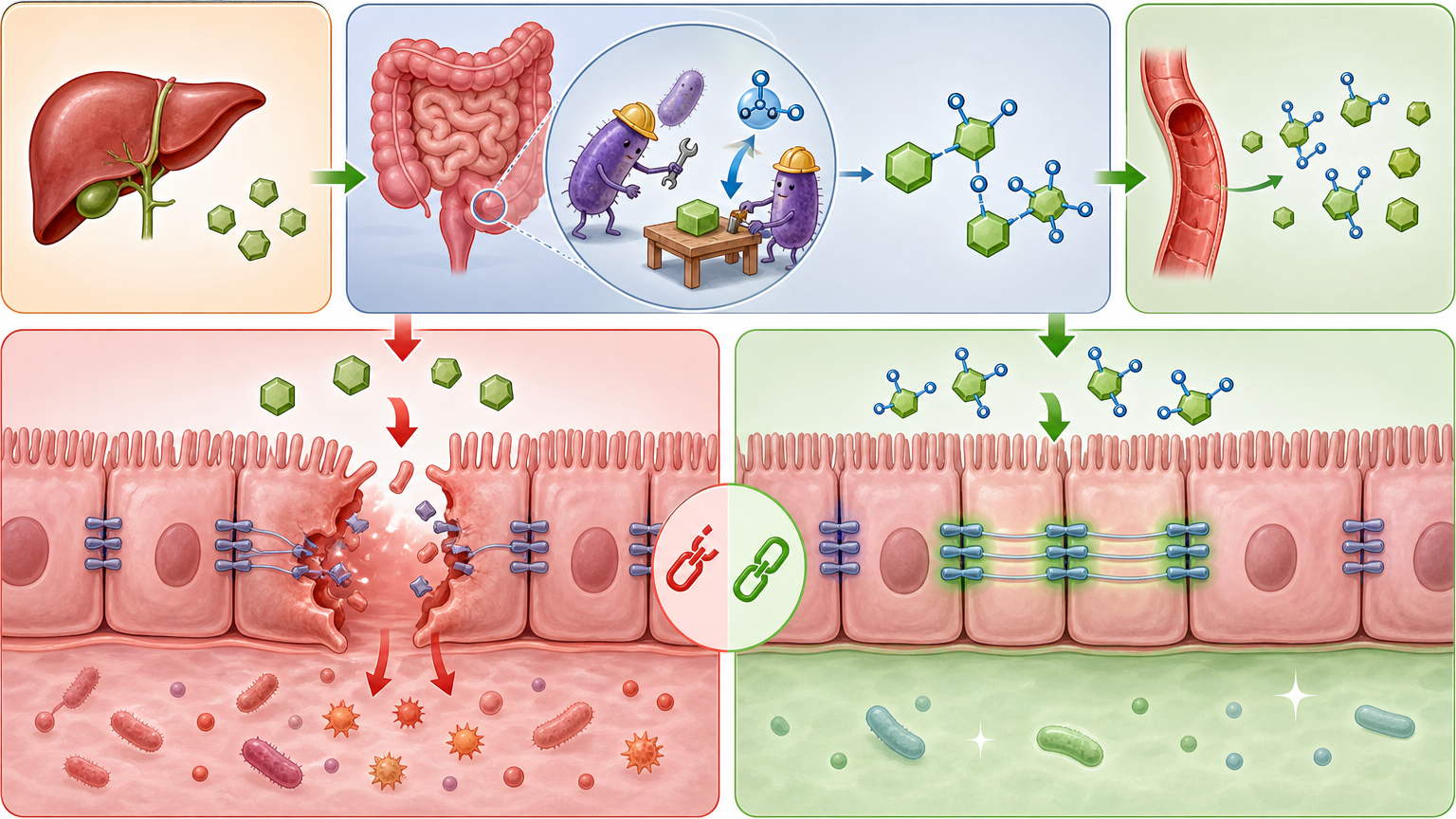
更关键的是,在儿童脓毒症患者体内,DCA-3S的水平明显低于健康孩子,而且病情越重,这种胆汁酸的含量就越低。它就像一个精准的警报器,能提前告诉医生孩子的感染正在失控。
研究团队在小鼠和肠道类器官模型里做了验证:给脓毒症模型补充DCA-3S后,小鼠的存活率显著提升,肠道的通透性明显下降,血液里的炎症因子也少了很多。它的作用机制很清晰,像同时握着两把武器:
第一把武器是修复肠道屏障。DCA-3S能上调ZO-1、Occludin这些紧密连接蛋白的表达,就像给肠道上皮细胞之间的缝隙打上铆钉,阻止细菌和毒素进入血液循环。
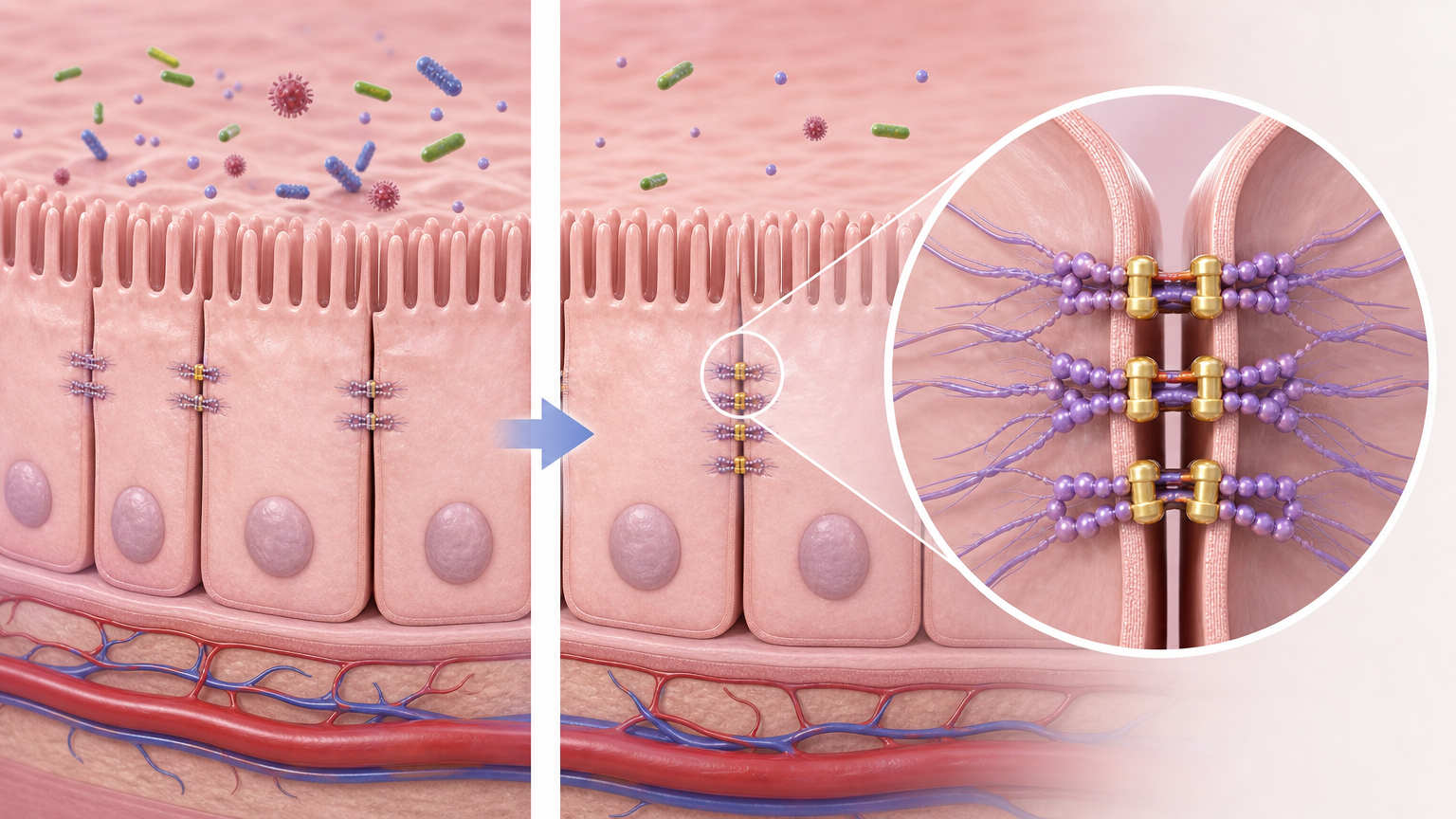
第二把武器是抑制炎症风暴。它能直接阻断NF-κB和MAPK这两条炎症信号通路,就像掐断了炎症反应的电源,减少TNF-α、IL-6这些“炎症炸弹”的释放,避免全身器官被过度免疫反应损伤。
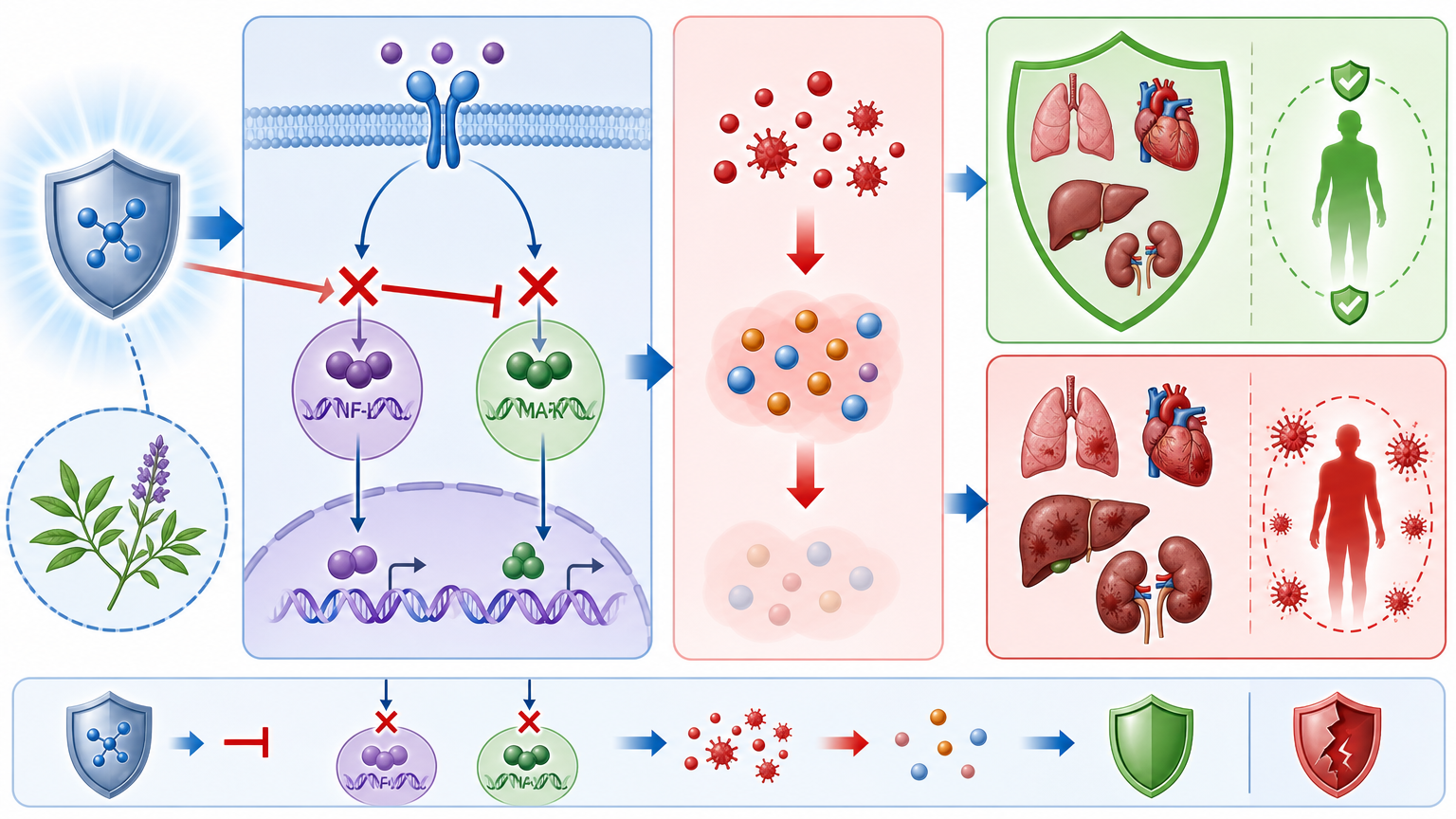
和传统的抗生素治疗不同,DCA-3S不杀细菌,而是调节身体的免疫状态和肠道稳态——这正好补上了现有治疗的短板:我们终于不用再盯着细菌打,而是学会了帮身体自己筑好防线。不过要注意的是,目前这还只是动物和类器官实验的结果,要用到临床上,还需要大样本的人体试验来验证剂量、安全性和疗效。
当然,这个发现也留下了不少待解的谜题。比如,棉子糖肠球菌在健康人的肠道里本来就存在,为什么脓毒症孩子体内的这种细菌会减少?是感染杀死了它们,还是肠道环境的变化让它们无法生存?
再比如,我们能不能直接给患者补充棉子糖肠球菌,让它在肠道里自己制造DCA-3S?但这种细菌本身也有一定的耐药性,甚至在免疫抑制患者中可能引发感染,直接补充菌株的安全性还需要仔细评估。
还有,DCA-3S在人体内的代谢途径是什么?它会不会和其他药物相互作用?这些问题都需要进一步的研究才能回答。毕竟,从实验室的发现到临床的应用,还有很长的路要走。
当我们把目光从肝脏转向肠道,从抗生素转向微生物代谢产物,其实是在重新理解疾病和身体的关系。我们以前总把细菌当成敌人,却忘了肠道里的很多细菌是我们的盟友——它们制造的分子,可能比我们发明的药物更懂我们的身体。
肠道菌群、代谢分子和疾病之间,从来不是单向的因果,而是一张互相影响的网络。小细菌里,藏着大健康的密码。这个发现不仅给脓毒症的治疗带来了新希望,也提醒我们:在探索人体的道路上,最不起眼的角落,可能藏着最关键的答案。