对抗知识焦虑,从看懂这条开始
App 下载
心脏修复的隐藏开关:Retsat的线粒体新身份
小鼠实验|哈尔滨医科大学|心肌细胞增殖|线粒体定位|Retsat酶|心脑血管疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
小鼠实验|哈尔滨医科大学|心肌细胞增殖|线粒体定位|Retsat酶|心脑血管疾病|医学健康
当心肌梗死发生,数百万心肌细胞会在几小时内死亡,而成年人类的心脏几乎没有能力再生新的心肌细胞——这是心血管疾病成为全球头号死因的核心原因。哈尔滨医科大学的研究团队却在小鼠实验中发现了一个反常识的突破:一种原本被认为只在细胞内质网里处理维生素A的酶,居然藏在心肌细胞的线粒体中,像个开关一样启动了心肌细胞的增殖。更意外的是,它发挥作用完全不靠自己的老本行。这到底是怎么回事?
我们可以把细胞想象成一个分工明确的工厂:内质网是负责加工小分子的车间,而线粒体是供应能量的发电厂。视黄醇饱和酶(Retsat)原本是内质网车间的老员工,工作是把维生素A转化成身体需要的代谢产物。
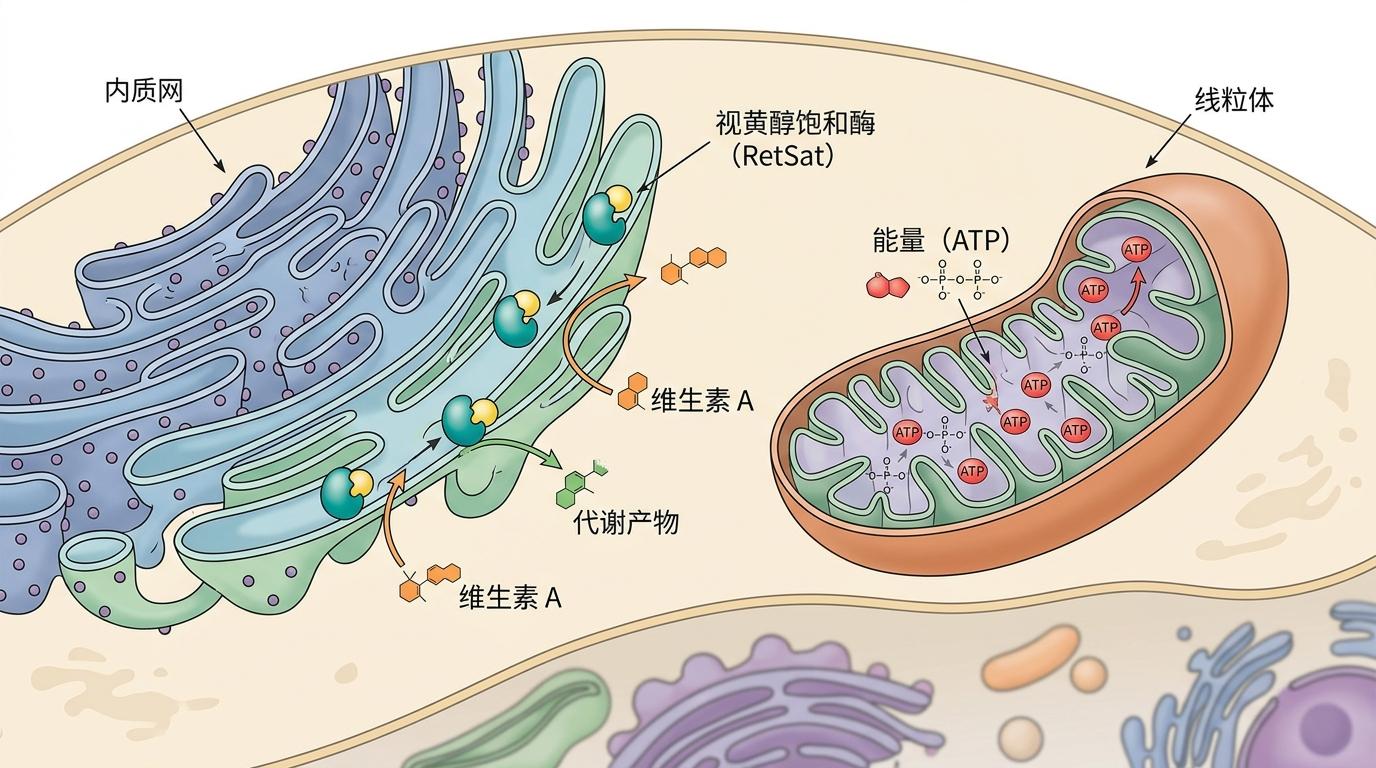
但哈尔滨医科大学的团队在观察小鼠心脏再生时发现,心肌细胞里的Retsat不仅待在车间,还偷偷溜进了发电厂。他们用基因技术让心肌细胞只在线粒体里过表达Retsat,结果这些细胞的增殖能力直接被激活,甚至能在心脏损伤后帮助修复组织。
这个过程和它原本的维生素A代谢功能毫无关系。
研究人员通过蛋白质互作实验找到了Retsat进厂的钥匙:它能和线粒体膜上的Tom70、Tim23蛋白结合,通过这两个转运蛋白组成的“门禁系统”,顺利进入线粒体内部。
线粒体这个发电厂的核心工作是通过三羧酸循环产生能量,而异柠檬酸脱氢酶2(Idh2)和谷氨酸脱氢酶1(Glud1)就是循环里的关键齿轮——它们的活性直接决定了能量生产的效率,还能控制一种叫α-酮戊二酸(αKG)的代谢物含量。
αKG就像细胞的增殖信号弹,它能打开控制细胞分裂的基因开关。但Idh2和Glud1这两个齿轮很容易被一种叫“乙酰化”的化学修饰卡住,一旦被卡住,活性就会下降,αKG的产量也会跟着减少。
而溜进线粒体的Retsat,恰好是乙酰化的“拮抗剂”。它能直接降低Idh2和Glud1的乙酰化水平,让这两个齿轮重新高效运转,从而提升αKG的含量,最终启动心肌细胞的增殖程序。
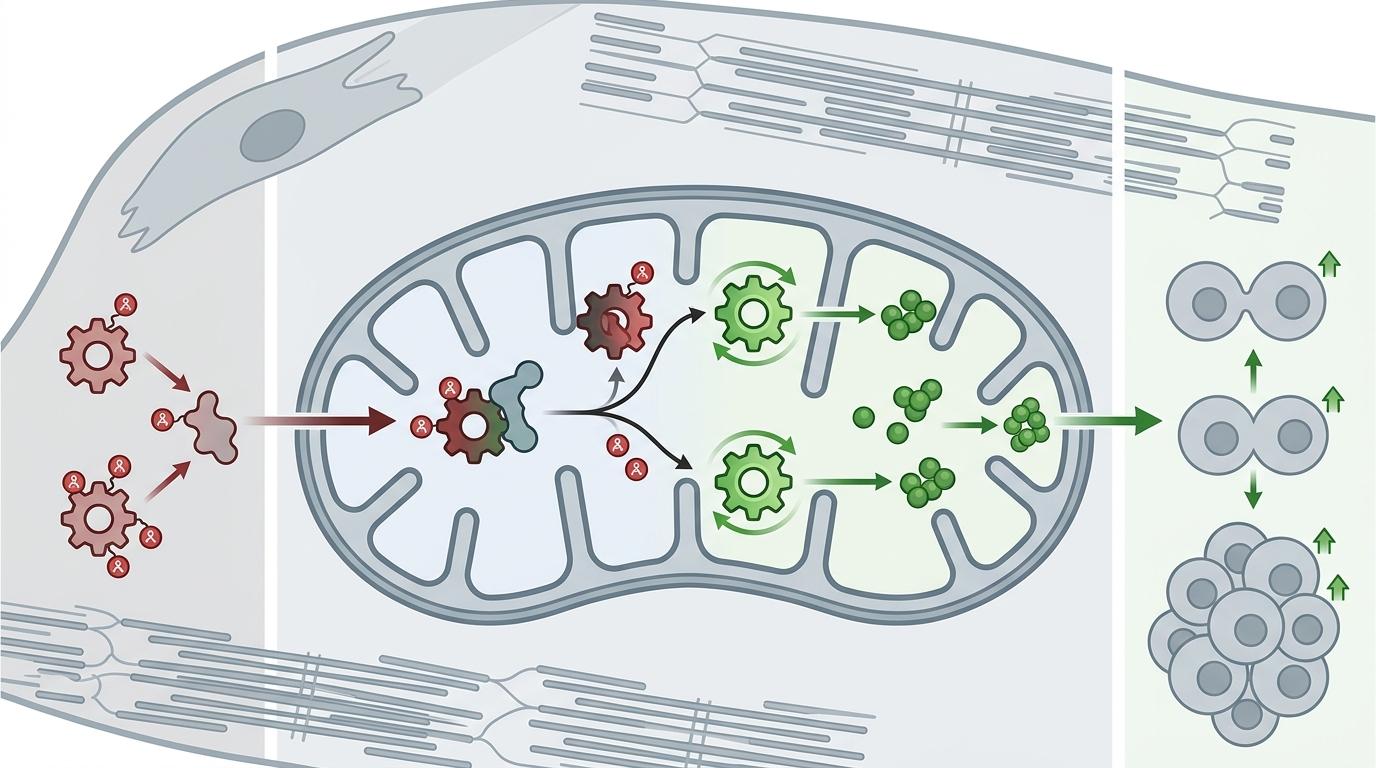
团队通过敲除和过表达实验验证了这个机制:心肌细胞里特异性敲除Retsat,新生小鼠的心脏再生能力会被抑制;而让Retsat只在线粒体里工作,就能让受损的心脏重新长出心肌组织。
这个发现最直接的价值,是给心脏修复提供了一个全新的靶点。和之前针对代谢酶或信号通路的尝试不同,Retsat的线粒体功能是一个完全未被开发的调控通路——它既不依赖传统的维生素A代谢,也不干扰线粒体的基础能量供应,安全性理论上更高。
但更值得关注的是,这项研究也暴露了我们对细胞代谢调控的认知盲区:一个酶居然能在不同细胞器里扮演完全不同的角色,而且这种“跨界功能”可能比我们想象的更普遍。Retsat在肝脏、脂肪组织里也有高表达,它会不会在其他器官里也有类似的“隐藏身份”?
当然,从实验室到临床还有很长的路要走。目前的研究只在小鼠身上完成了验证,Retsat在人类心肌细胞里的作用是否完全一致、如何精准靶向线粒体里的Retsat而不干扰它的内质网功能,这些都是需要解决的问题。
我们总习惯给生物分子贴上“功能标签”,以为它们一辈子只会干同一件事——就像我们以为心脏一旦受损就无法再生一样。但Retsat的跨界之旅提醒我们,生命的调控网络远比我们想象的复杂。
细胞的潜力,藏在未被发现的分工里。
未来或许有一天,医生能通过靶向线粒体里的Retsat,让受损的心脏重新长出心肌组织。但更重要的是,这个发现让我们明白:那些被我们定义为“单一功能”的生物分子,可能还藏着改变医学格局的秘密。