
3 个月前

3 个月前
衰老,并非如诗歌中所描绘的平静黄昏,而更像一场在我们体内悄然蔓延的“慢性火灾”。这场火灾,在科学界被称为“炎症性衰老”(Inflammaging),是一种低度、无菌、持续存在的炎症状态。它不像急性感染那样猛烈,却如温水煮蛙,日积月累地侵蚀着我们的组织和器官,催生了心脏病、糖尿病、神经退行性疾病乃至癌症等一系列老年顽疾。多年来,科学家们一直在追问:点燃这场“火灾”的最初火星,究竟来自哪里?
就在2025年9月24日,顶级学术期刊《自然》(Nature)上的一篇研究为我们揭开了这团迷雾的一角。来自德国马克斯·普朗克衰老生物学研究所的Thomas Langer教授团队发表了一项颠覆性的研究成果。他们发现,衰老的“第一缕烟”,可能源自我们细胞内最基础的代谢活动——核苷酸代谢的失衡。
这项研究精准地描绘了一条从微观代谢紊乱到宏观衰老现象的完整通路:细胞内用于构建DNA的“原料”供应失衡,导致线粒体DNA(mtDNA)在合成时出现了大量的“拼写错误”。这些脆弱的、充满错误的mtDNA极易断裂并“越狱”到细胞质中,如同内奸泄露了机密,从而触发了细胞内最敏感的“警报系统”,点燃了那场名为“炎症与衰老”的熊熊大火。
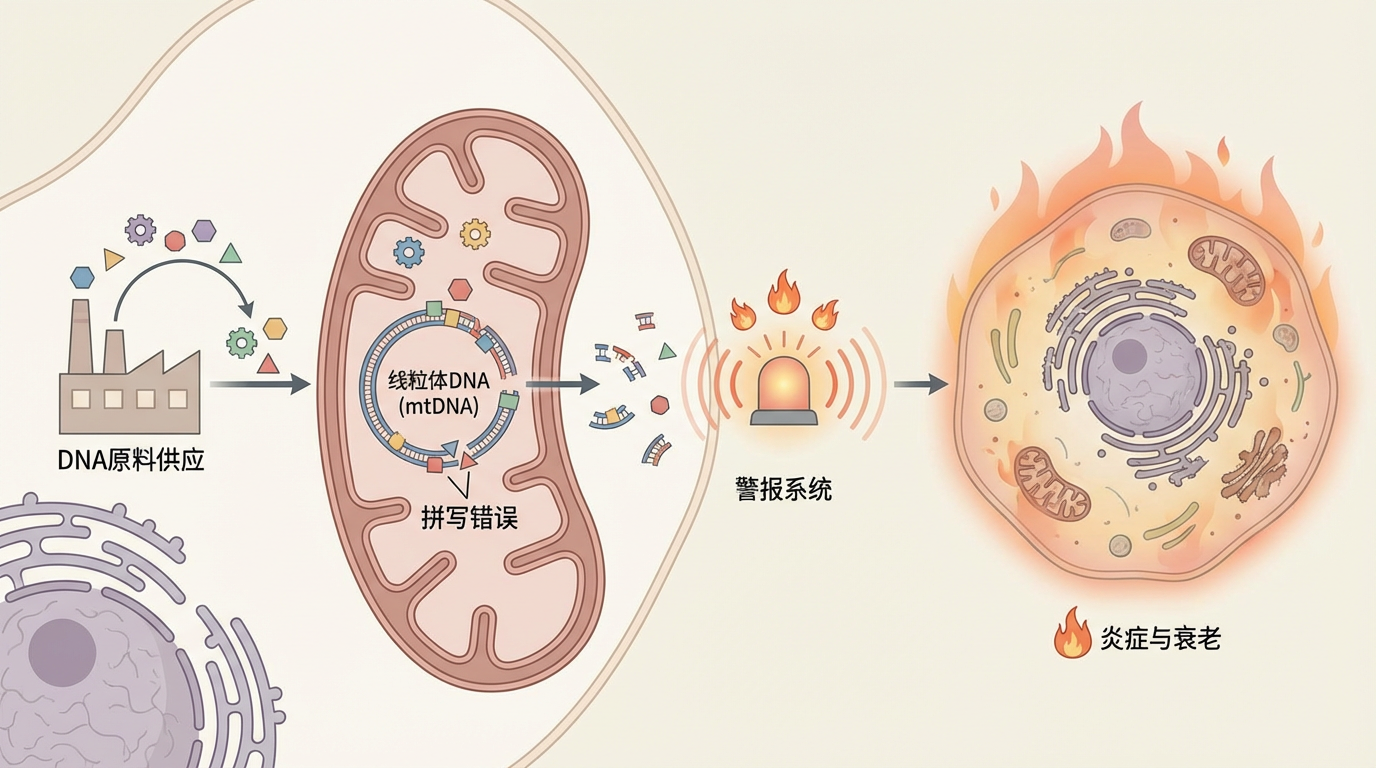
要理解这个过程,我们必须深入细胞内部的“能量工厂”——线粒体。线粒体不仅为我们提供生命活动所需的绝大部分能量,还拥有自己的一套独立遗传物质,即线粒体DNA(mtDNA)。这套DNA非常特殊,它源自远古时期被我们祖先细胞吞噬的细菌,因此,一旦它从线粒体中逃逸出来,就会被细胞的免疫系统误认为是“入侵的敌人”。
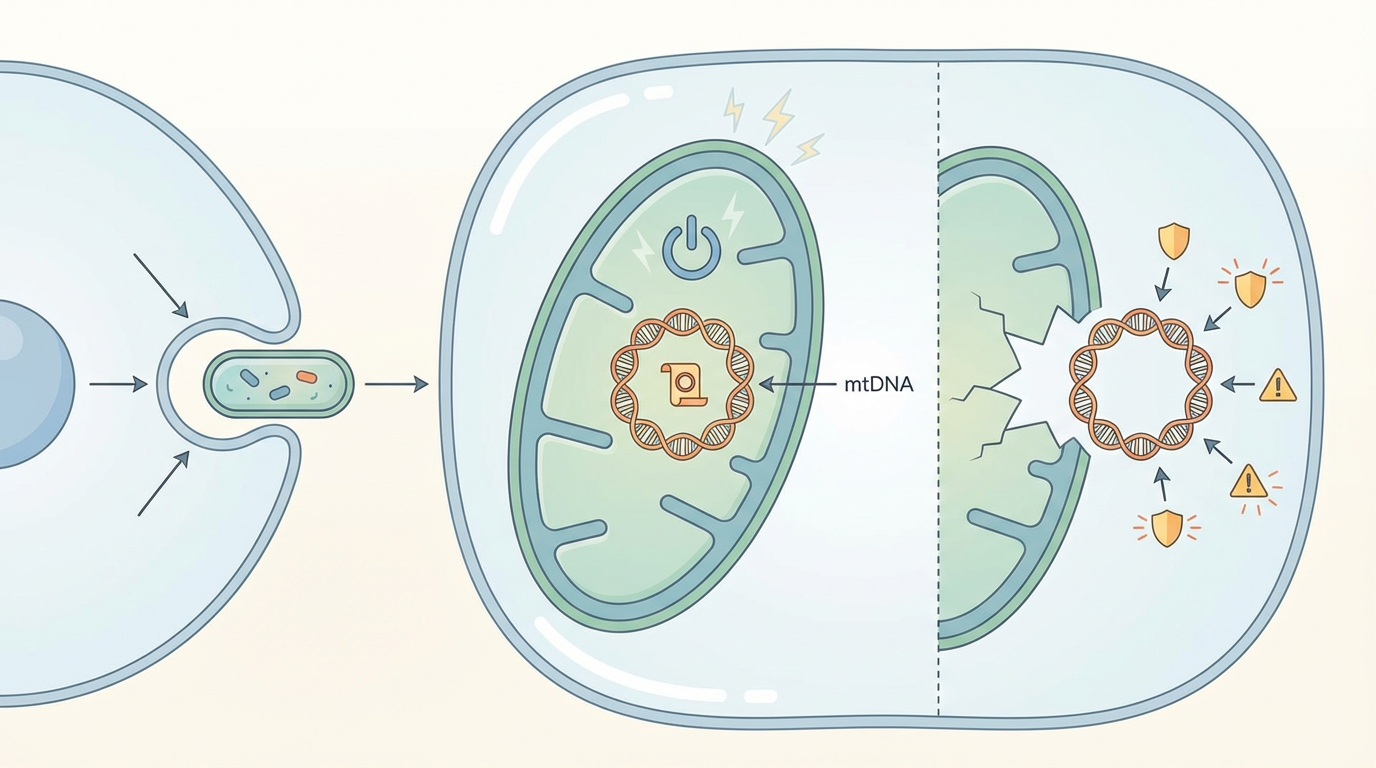
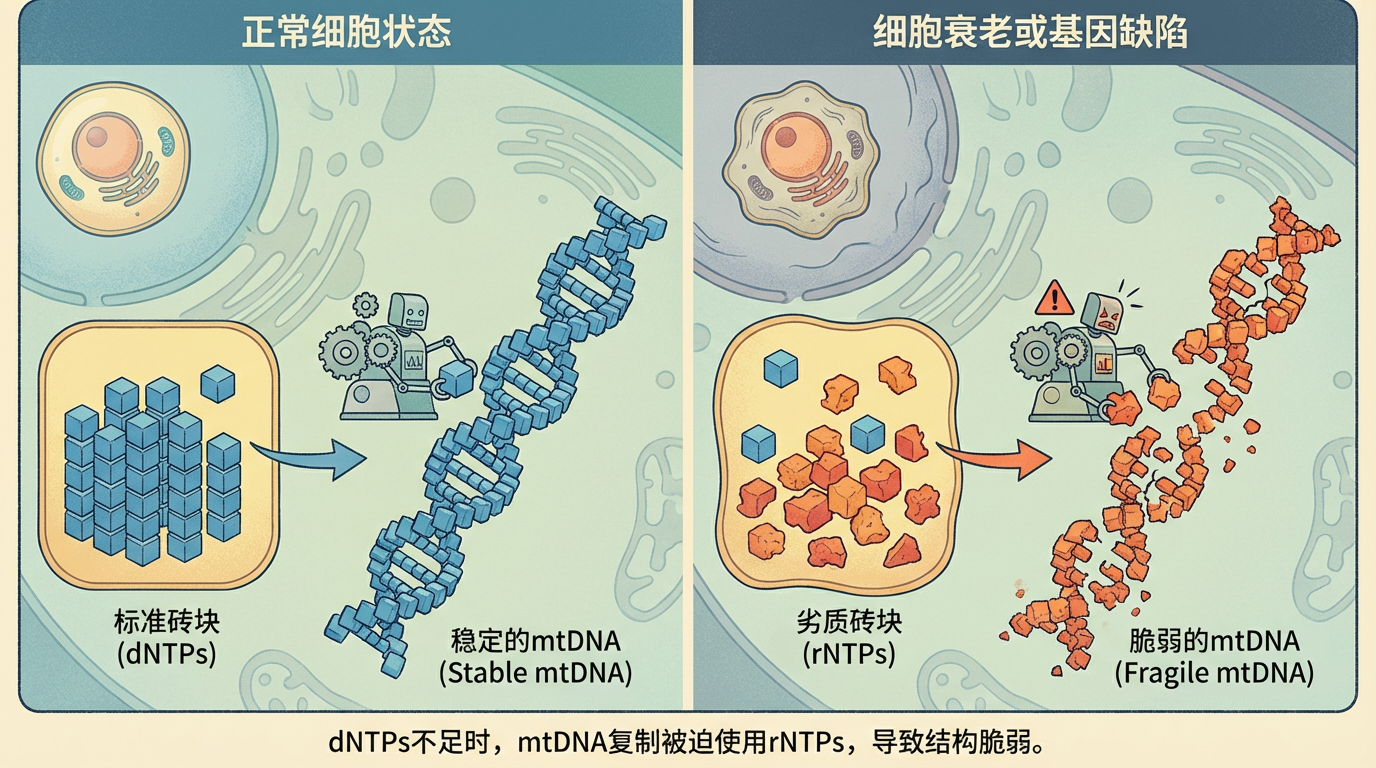
细胞在构建DNA时,需要使用四种名为“脱氧核糖核苷酸”(dNTPs)的精确“建筑材料”。然而,细胞内还充斥着另一种数量多出数十甚至上百倍的、用于构建RNA的“原料”——“核糖核苷酸”(rNTPs)。你可以将dNTPs想象成坚固耐用的标准砖块,而rNTPs则是临时搭建用的“劣质砖块”。
正常情况下,细胞的DNA合成系统会优先选用“标准砖块”。但Langer团队发现,随着细胞衰老或在特定基因缺陷下,细胞内的“标准砖块”(dNTPs)库存会严重不足。 这时,mtDNA的复制机器在别无选择的情况下,只能大量抓取“劣质砖块”(rNTPs)来勉强完成建造。用劣质材料建成的mtDNA,其结构稳定性可想而知,变得异常脆弱,稍有风吹草动便会分崩离析。
Langer团队的发现之旅,始于一个令人费解的动物模型。他们研究了一种基因敲除小鼠,这些小鼠体内缺少一个名为MGME1的基因。MGME1蛋白就像是mtDNA复制过程中的“质检员”,负责修复错误。失去了“质检员”的小鼠,表现出惊人的一致性:它们会随着年龄增长出现严重的肾脏炎症,并在一岁左右就因肾功能衰竭而过早死亡。
这背后究竟发生了什么?
第一步:发现“逃犯”。 研究人员在这些早衰小鼠的肾脏细胞质中,检测到了大量本不该出现在那里的mtDNA碎片。这些“逃犯”的数量是正常小鼠的数倍之多。
第二步:锁定“警报系统”。 他们接着关闭了细胞内的“DNA警报系统”——cGAS-STING信号通路。神奇的是,一旦警报系统失灵,即便mtDNA碎片依然存在,小鼠的肾脏炎症和组织损伤也得到了极大的缓解。这证明,正是这些“逃犯”拉响了错误的警报,引发了致命的免疫风暴。
第三步:揪出“幕后黑手”。 最关键的问题来了:为什么这些mtDNA会破碎并逃逸?通过深入的代谢分析,谜底终于揭晓。这些基因缺陷细胞内的“标准砖块”(dNTPs)水平急剧下降,导致“劣质砖块”(rNTPs)被大量掺入mtDNA。利用尖端测序技术,科学家们亲眼看到了这些mtDNA上布满了密密麻麻的“拼写错误”。
这个发现,如同一道闪电,照亮了一条全新的致病路径:代谢失衡 → 原料短缺 → mtDNA“豆腐渣工程” → DNA碎片逃逸 → 免疫警报大作 → 慢性炎症与器官衰竭。
这项研究最深远的意义在于,它并不仅仅解释了一种罕见基因缺陷病的成因。研究团队进一步发现,这一机制在普遍的、正常的衰老过程中同样存在。
当正常细胞进入衰老状态时,它们的细胞核DNA复制已经停止,合成“标准砖块”(dNTPs)的关键酶活性也随之大幅下降。这同样造成了dNTPs的短缺和rNTP/dNTP比率的飙升。实验证实,来自年老小鼠多个组织(如肾脏、肝脏)的mtDNA,以及体外诱导衰老的人类细胞,都表现出对碱性环境更高的敏感性——这意味着它们的DNA链中掺入了大量“劣质砖块”,变得一触即溃。
这些衰老细胞也因此不断向外释放mtDNA碎片,激活cGAS-STING通路,并分泌大量的促炎因子和组织破坏酶,形成所谓的“衰老相关分泌表型”(SASP)。SASP就像衰老细胞释放的“毒雾”,不仅会毒害自身,还会弥漫到周围,诱导健康的邻居细胞一同衰老,从而将局部的衰老信号放大为全身性的衰老进程。
揭示机制的最终目的是为了寻找干预的可能。Langer团队进行了一项激动人心的实验:他们向正在衰老的细胞培养基中,直接“喂食”了合成“标准砖块”的原材料——脱氧核糖核苷。
结果令人振奋:这一简单的“营养补充”,显著降低了衰老细胞中泄漏的mtDNA水平,稳固了mtDNA的结构,并最终成功抑制了关键SASP炎症基因的表达。 这无疑是一个强有力的证据,表明通过纠正核苷酸代谢失衡,或许能够从源头上掐断衰老炎症的导火索。
这一发现为开发全新的抗衰老策略打开了大门:
当然,从细胞实验到真正的人类抗衰老疗法,依然道阻且长。我们仍需回答诸多问题:这种代谢失衡在人体所有组织中都普遍存在吗?究竟是什么最先触发了衰老细胞中dNTPs的合成减少?长期人为干预核苷酸代谢是否安全?
尽管如此,这项研究依然为我们描绘了一幅充满希望的蓝图。它告诉我们,衰老或许并非一个无法逆转的、被动接受损伤的过程,而是一个由精确分子事件驱动的主动程序。通过理解并干预这些深藏在细胞代谢网络中的关键节点,我们或许真的有机会去调节衰老的节奏,将生命的乐章演奏得更长久,也更健康。
点击充电,成为大圆镜下一个视频选题!