对抗知识焦虑,从看懂这条开始
App 下载
奥美拉唑治胃痛,乱搭药可能埋隐患
血小板抑制率|质子泵抑制剂|药物相互作用|氯吡格雷|奥美拉唑|临床诊疗技术|医学健康
62岁的张阿姨因胃溃疡吃了3年奥美拉唑,胃痛反酸的老毛病确实没再犯。直到上个月她因冠心病加服氯吡格雷,没过两周就突发胸闷被送进急诊——检查显示血小板抑制率不足标准的一半,血栓风险飙升。医生说,罪魁祸首就是她每天同吃的奥美拉唑。这不是个例:每年都有近10%的PPI使用者,因不当联用药物出现疗效打折或不良反应。为什么一款治胃痛的常用药,会和心脏药产生致命冲突?
胃里的“酸开关”:奥美拉唑的双重抑酸术
你可以把胃壁细胞想象成一座胃酸工厂,质子泵就是工厂的核心流水线——它把细胞内的氢离子泵进胃腔,最终变成腐蚀食物的胃酸。奥美拉唑作为质子泵抑制剂(PPI),是个精准的“流水线破坏者”。
它以肠溶剂型躲过胃酸的“自相残杀”,在小肠被吸收后钻进胃壁细胞的分泌小管。这里的强酸环境会把它激活成带正电的硫酰胺,像粘胶一样牢牢粘在质子泵的关键位点上,形成不可逆的共价键——相当于把流水线的电源焊死了。
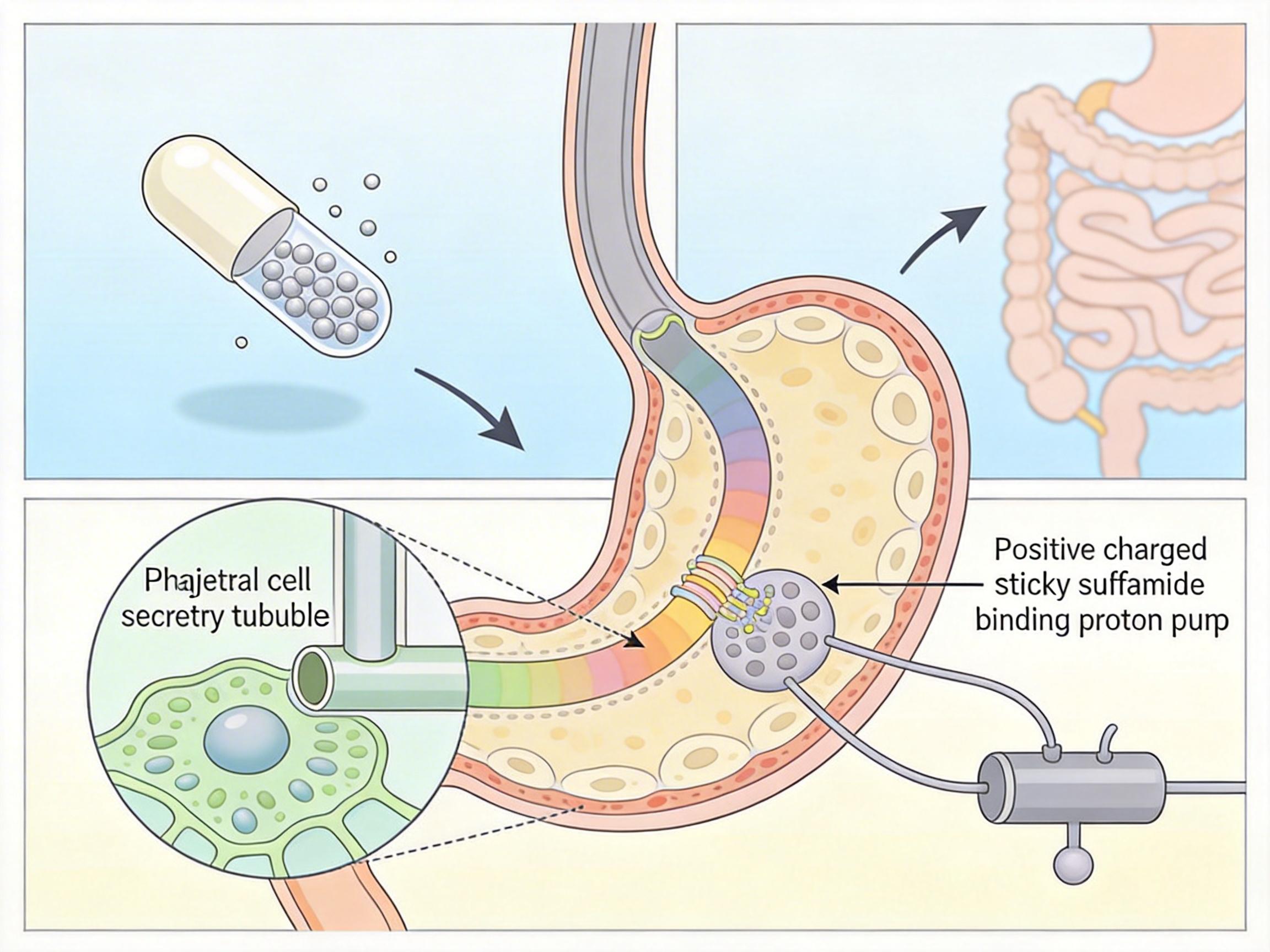
但真实的机制比这更精确:除了堵死质子泵,最新研究发现奥美拉唑还能抑制胃黏膜里的碳酸酐酶。这种酶负责给胃酸生产提供“氢离子原料”,双重阻断下,胃酸分泌能被抑制80%-95%,且效果能持续36小时以上——远超过它在血液里的半衰期。
正是这种强效且持久的抑酸能力,让它成为胃溃疡、胃食管反流病的首选药,但也为后续的药物相互作用埋下了伏笔。
两类冲突:从胃里到肝脏的“化学战争”
奥美拉唑的药物相互作用,本质上是两场“化学战争”:一场在胃里改变环境,一场在肝脏抢酶。
第一战场是胃内pH值的剧变。它能把胃内pH从1-2的强酸环境拉到4以上,这会让那些依赖酸性环境才能溶解吸收的药物直接“罢工”:比如铁剂需要胃酸把三价铁转化成易吸收的二价铁,奥美拉唑会让铁的吸收率下降30%-50%;酮康唑这类抗真菌药,在中性环境里几乎不溶解,联用后抗真菌效果直接打对折。
第二战场在肝脏的酶系统。奥美拉唑主要靠CYP2C19酶代谢,但它同时也是这个酶的“抑制剂”——相当于一边占着厨房灶台做饭,一边把别人的锅给藏了。氯吡格雷就是受害者之一:它本身是个“前体药”,必须靠CYP2C19酶激活才能变成抗血小板的活性物质。奥美拉唑会把CYP2C19酶的活性抑制70%以上,直接让氯吡格雷的有效成分减少一半,血栓风险飙升。
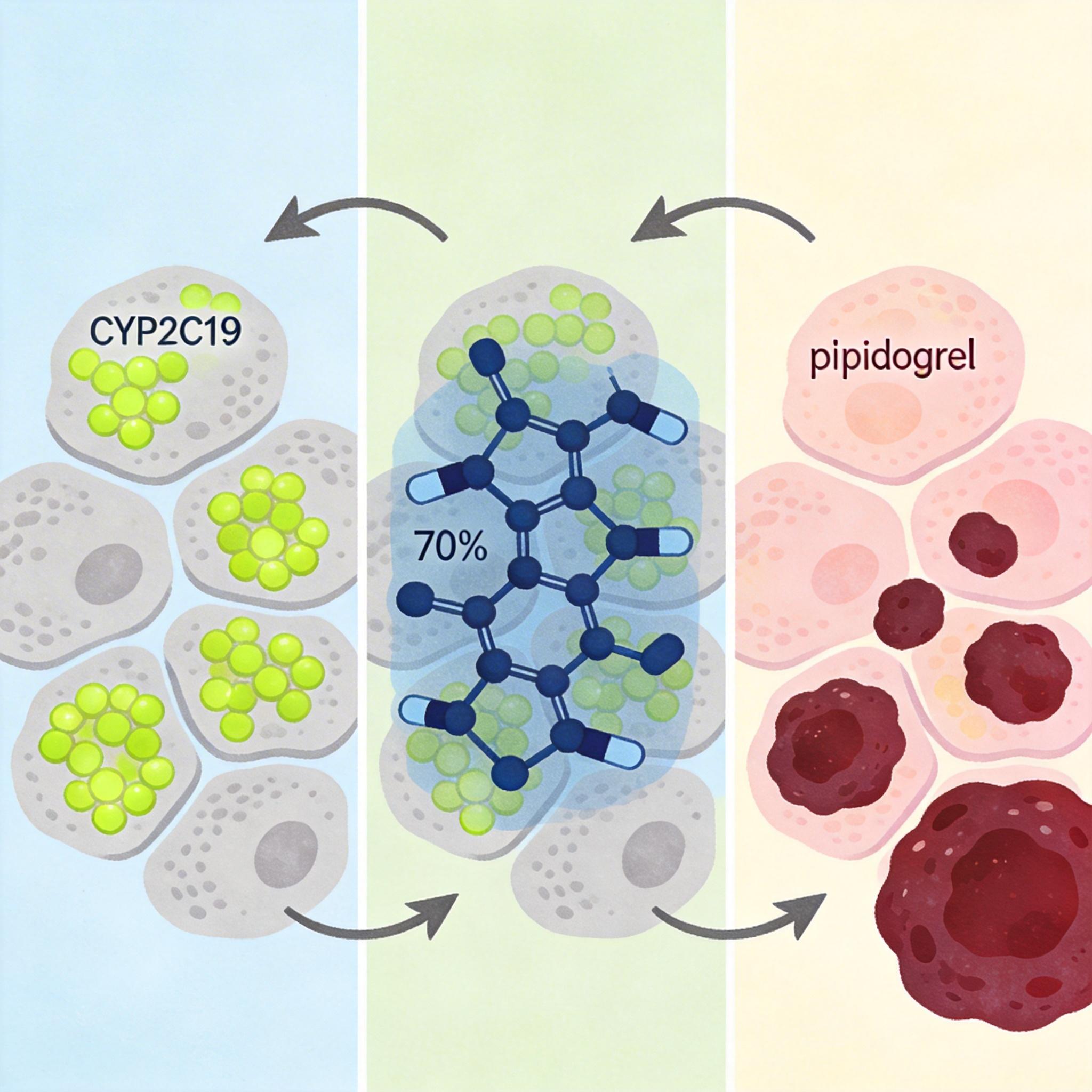
更棘手的是,这种酶抑制是时间依赖性的——哪怕错开8小时吃,也躲不开它的影响。美国FDA早在2012年就修改了氯吡格雷的说明书,明确警示避免与奥美拉唑联用。
被忽略的基因暗线:有人天生“敏感体质”
你可能不知道,CYP2C19酶的活性天生有差异——这是基因决定的。
人群里大概有30%的人是CYP2C19慢代谢型,他们的肝脏代谢奥美拉唑的速度比普通人慢2-3倍,药物在体内停留的时间更长,抑酸效果更强,但也更容易和其他药物发生冲突。比如慢代谢型患者同时吃奥美拉唑和硝苯地平,硝苯地平的血药浓度会比常人高30%,低血压、头晕的风险直接翻倍。
反过来,有10%的人是CYP2C19快代谢型,他们吃奥美拉唑的效果会打折扣,可能需要加倍剂量才能达到抑酸目标,但这也意味着他们的酶被抑制的风险更低。
我认为,这是最容易被忽略的用药盲区:目前国内很少在开奥美拉唑前做基因检测,但对于需要长期联用多种药物的老年患者,基因检测能帮医生精准调整剂量,避免不必要的风险。
张阿姨出院后,医生把她的奥美拉唑换成了对CYP2C19酶影响极小的泮托拉唑,胸闷的症状再也没出现过。这个案例里藏着一个朴素的真相:再安全的常用药,也不是“百搭款”。
奥美拉唑的诞生是胃肠病学的里程碑,但它的“双刃剑”属性也提醒我们:药物从来不是孤立的个体,它们在体内的相互作用远比我们想象的复杂。与其把它当“万能胃药”长期依赖,不如在医生和药师的指导下,精准使用——毕竟,能治病的药,用对了才是良药。
药无好坏,用对是关键。