对抗知识焦虑,从看懂这条开始
App 下载
最严细胞监管落地:灰产退场,患者与行业的阵痛与新生
违规收费|细胞治疗乱象|干细胞公司|CAR-T治疗|818号令|公共政策|临床诊疗技术|社会人文|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
违规收费|细胞治疗乱象|干细胞公司|CAR-T治疗|818号令|公共政策|临床诊疗技术|社会人文|医学健康
2026年五一假期的病房里,有癌症患者在赶最后一班“低价车”——他们要在5月1日前完成医院违规的“同情CAR-T”治疗,10万元的花费是上市药的十分之一。而在广州南沙的写字楼里,数十家小型细胞公司正在连夜转让营业执照,墙上“国际领先干细胞抗衰”的海报还没来得及摘下。这一天,被称为“中国细胞行业最严监管”的818号令正式实施:临床研究严禁收费,违规最高罚20倍所得,地下灰产的口子被彻底焊死。没人想到,一场关于“救命药”的洗牌,会来得如此迅猛。
细胞治疗的乱局,早不是新鲜事。干细胞被包装成“一针年轻十岁”的抗衰神针,在美容会所喊出20万元一针的天价,成本却仅几千元——有些机构甚至在细胞液里掺兴奋剂制造“体感明显”的假象;免疫细胞治疗领域,2016年魏则西事件后,灰色操作仍未绝迹,“同情CAR-T”打着临床研究的旗号,让患者私下给细胞公司打款,成了买不起上市药的患者最后的“救命通道”。
清华大学药学院创始院长丁胜记得,每次给EMBA学员上课,总有企业家问“哪里能打干细胞”。这些非标准、未验证的治疗,正是818号令要清除的毒瘤。2018年贺建奎基因编辑婴儿事件,更是暴露了生物医学新技术的监管漏洞——当技术跑在规则前面,患者的权益和行业的底线都会失守。
818号令的核心逻辑很简单:先守底线,再谈发展。它把细胞治疗、基因治疗、脑机接口等十余项新技术全部纳入监管,临床研究必须在三甲医院开展,且严禁向受试者收费;违规者最高罚20倍违法所得,相关责任人可能被吊销执照。这相当于给行业划了一条生死线:要么合规,要么退场。
严监管的另一面,是给合规创新开了一扇门。818号令首次明确:三甲医院完成合规临床研究后,可将个性化、难标准化的疗法按技术路径转化收费——这给罕见病治疗、个性化细胞疗法提供了一条绕开药品注册漫长流程的商业化通道。
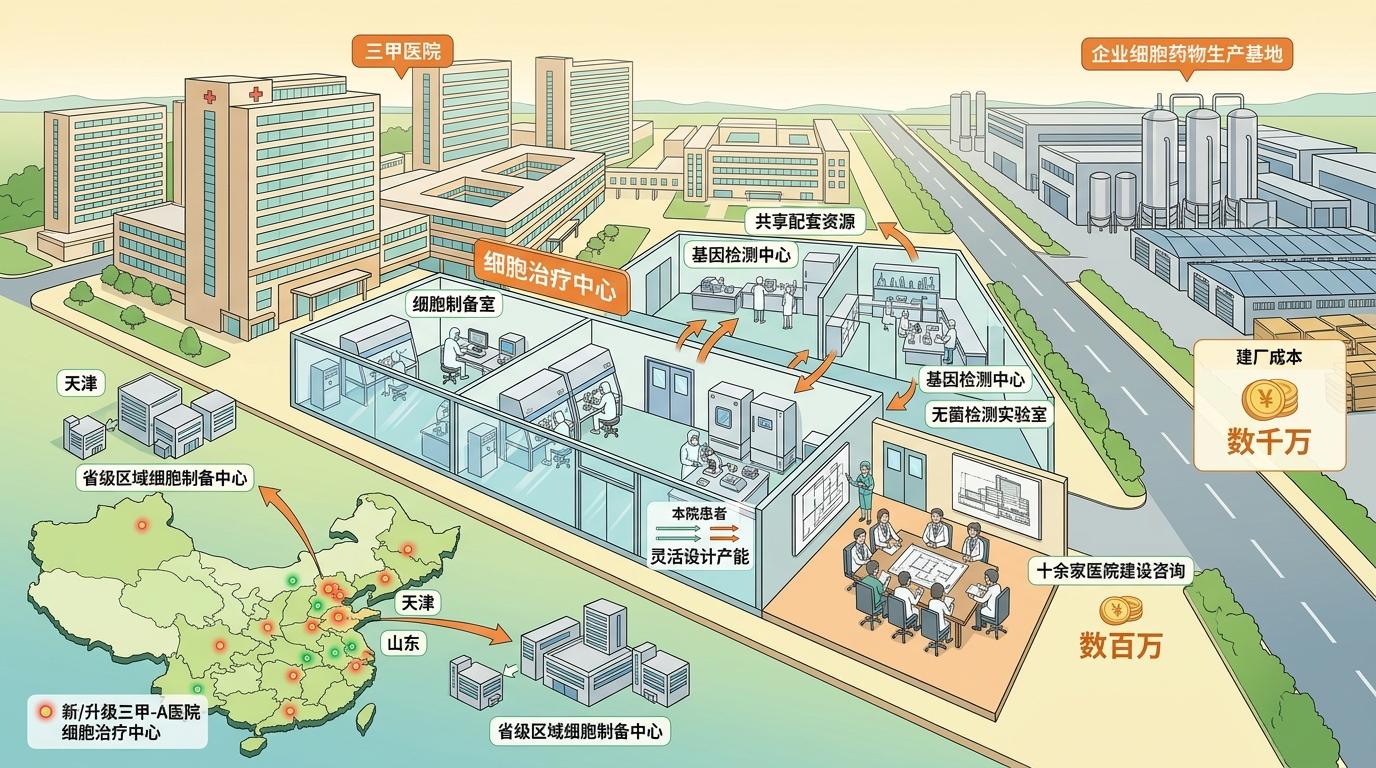
全国已有70余家三甲医院新建或升级细胞治疗中心,天津、山东等地正在布局省级区域细胞制备中心。和企业动辄几千万的建厂成本不同,医院的细胞制备中心只需几百万,可根据本院患者量灵活设计产能,还能共享医院的基因检测、无菌检测等配套资源。一位产业界人士透露,最近已经接到十几家医院的建设咨询,“以前医院都找外面的实验室代加工,现在都想自己干”。
资本也闻风而动。头部细胞公司的融资额较去年翻倍,非医疗行业的高净值个人开始涌入赛道,甚至有些之前做“抗衰干细胞”的公司,也在抓紧升级实验室、补临床数据,试图“改邪归正”。对他们来说,818号令不是死路,而是把之前“赚快钱”的灰色收入,变成了“赚长钱”的合规生意。
但新秩序的建立,注定伴随着阵痛。那些依赖“同情CAR-T”的患者,突然失去了低价救命的渠道——上市的CAR-T药虽有效,却动辄百万元,医保覆盖有限。一位血液科医生坦言,之前科室一年有两三百个患者需要CAR-T,用得起上市药的只有二三十人,剩下的都靠“同情CAR-T”续命。
行业的困惑也不少。818号令提到的“同类机制原理”界定至今模糊:如果已有间充质干细胞药物获批,那同类机制的干细胞疗法是否还能走技术转化通道?这直接关系到大量在研项目的命运。有投资人担心,最后能走转化通道的,会不会都是“没人愿意做药”的小众项目?
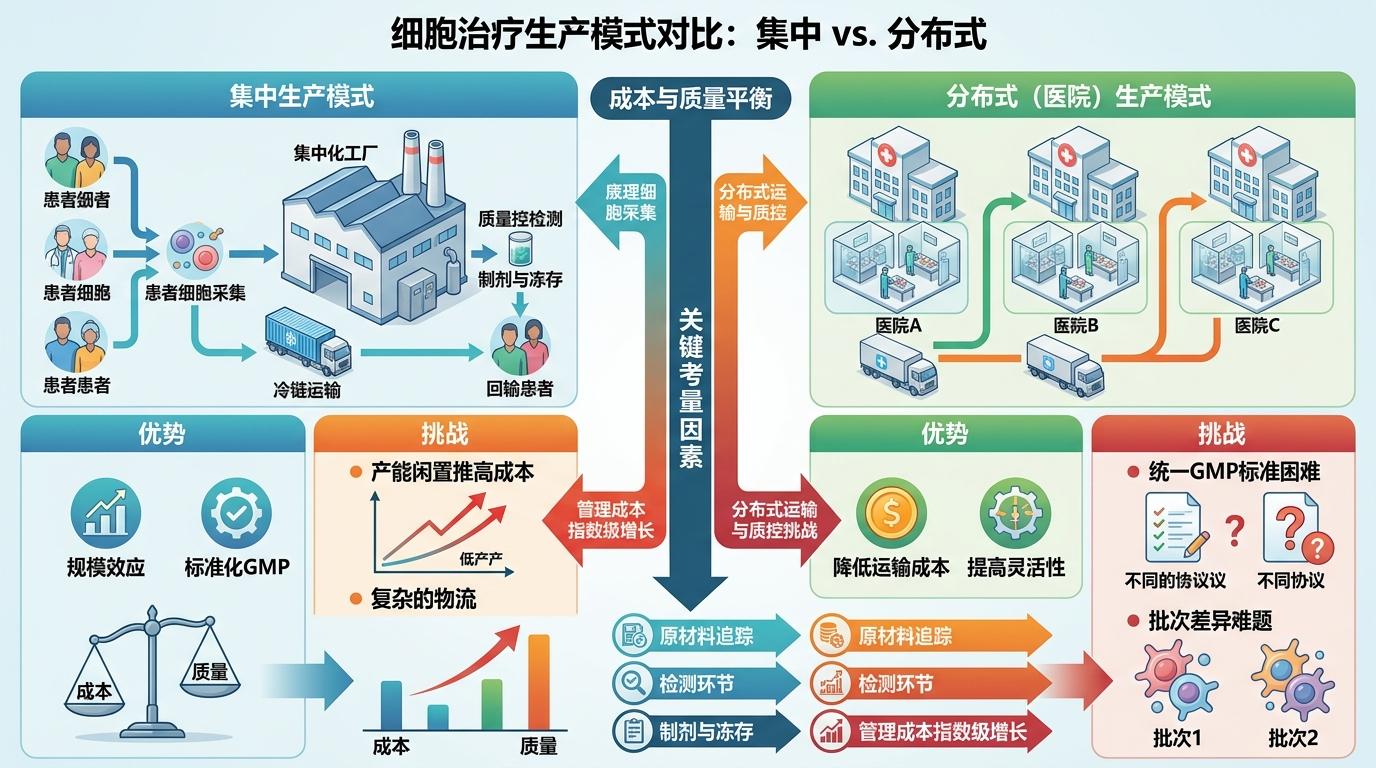
更现实的问题是成本与质量的平衡。细胞治疗的集中生产模式,往往因产能闲置推高成本;而医院分布式生产,又面临如何统一GMP标准、避免批次差异的难题。一位药企高管举例,CAR-T药物的原材料追踪、检测环节,规模化生产的管理成本会指数级增长,但分布式生产的冷链运输、质量管控,又是新的挑战。
当灰产的泡沫被戳破,细胞治疗行业终于站在了合规的起跑线上。它不再是少数人眼中的“抗衰神话”,也不是患者走投无路时的“灰色救命稻草”,而是要在规则的框架下,重新寻找技术与伦理、创新与普惠的平衡点。
严管不是终点,是让真正的救命技术走得更远。 未来的细胞治疗,或许不会再有“一针暴富”的神话,却能让更多患者放心地接受治疗;或许不会再有野蛮生长的乱象,却能让真正的创新者获得长期的回报。这场洗牌,洗走的是短期的浮躁,留下的是行业的底气——毕竟,医学的终极目标,从来不是赚快钱,而是救活人。