对抗知识焦虑,从看懂这条开始
App 下载
皮炎竟从肠道来,这种代谢物是关键
肠-皮轴机制|TLR4受体|肠道代谢物|特应性皮炎|自身免疫疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
肠-皮轴机制|TLR4受体|肠道代谢物|特应性皮炎|自身免疫疾病|医学健康
当孩子反复挠着泛红起疹的胳膊,当成年人被顽固的皮肤瘙痒缠得睡不好觉,特应性皮炎(AD)的折磨,总让人把目光盯在皮肤上——是不是护肤品选错了?是不是接触了过敏原?但南方医科大学2026年发表在《Immunity》的研究,却把答案指向了一个意想不到的地方:肠道。他们发现,肠道里的一种代谢物,会悄悄驱动皮肤的炎症风暴,而这一切,从肠道上皮的一个免疫受体缺陷就已经开始了。为什么肠道出问题,皮肤会先遭殃?这背后藏着一套精密又难缠的「肠-皮轴」机制。
要理解这套机制,得先从肠道上皮的「守门人」——TLR4受体说起。TLR4就像肠道黏膜上的哨兵,能识别细菌的信号,维持菌群的平衡。当这个哨兵「罢工」(TLR4缺陷),肠道菌群就会彻底乱套:原本能保护肠道屏障的益生菌嗜黏蛋白阿克曼菌(Akkermansia muciniphila)数量大减,而一种带CutC基因的细菌开始疯狂繁殖。
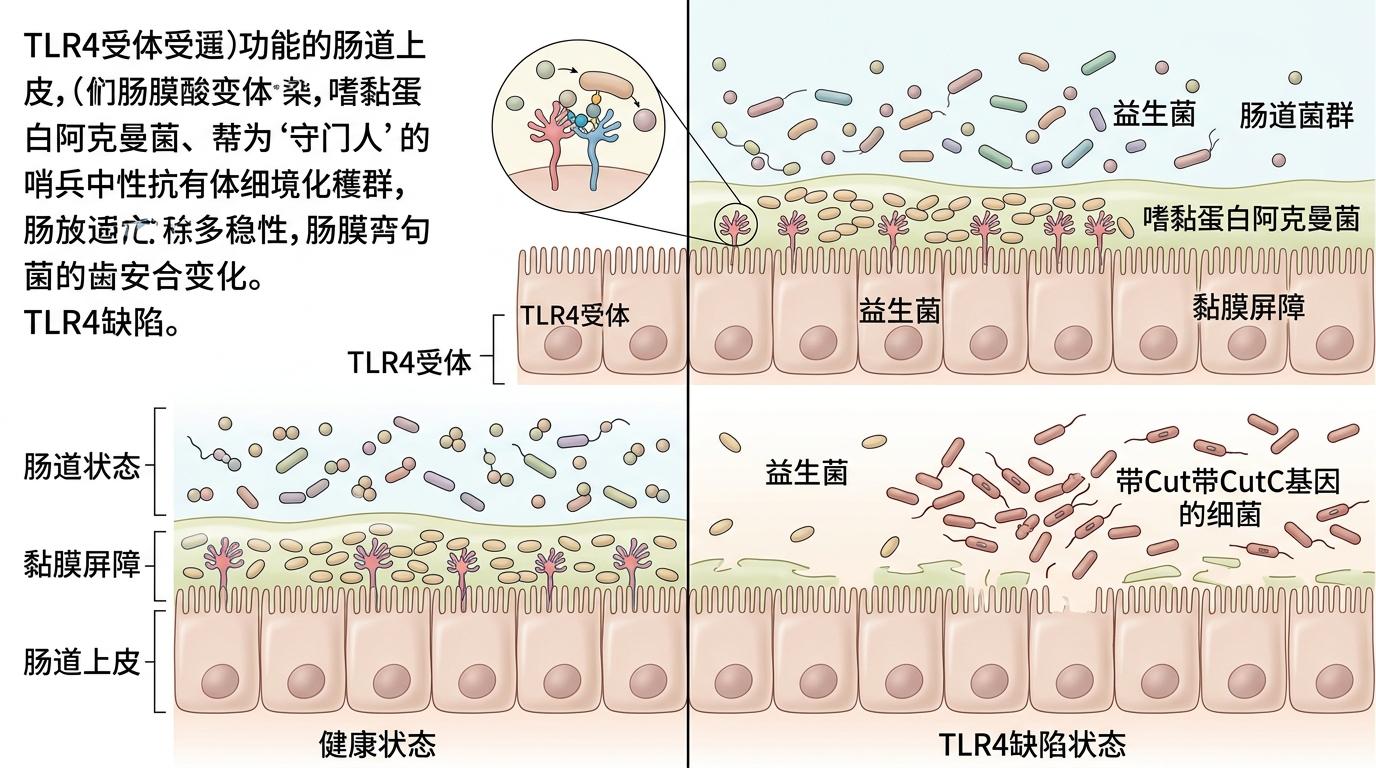
CutC基因编码的胆碱裂解酶,就像一把专门拆解胆碱的剪刀。胆碱是我们从鸡蛋、红肉里摄入的营养,正常情况下会被人体合理利用,但在CutC菌的作用下,它会被拆解成三甲胺(TMA),再经过肝脏氧化,变成氧化三甲胺(TMAO)——就是这场皮肤炎症的「幕后推手」。
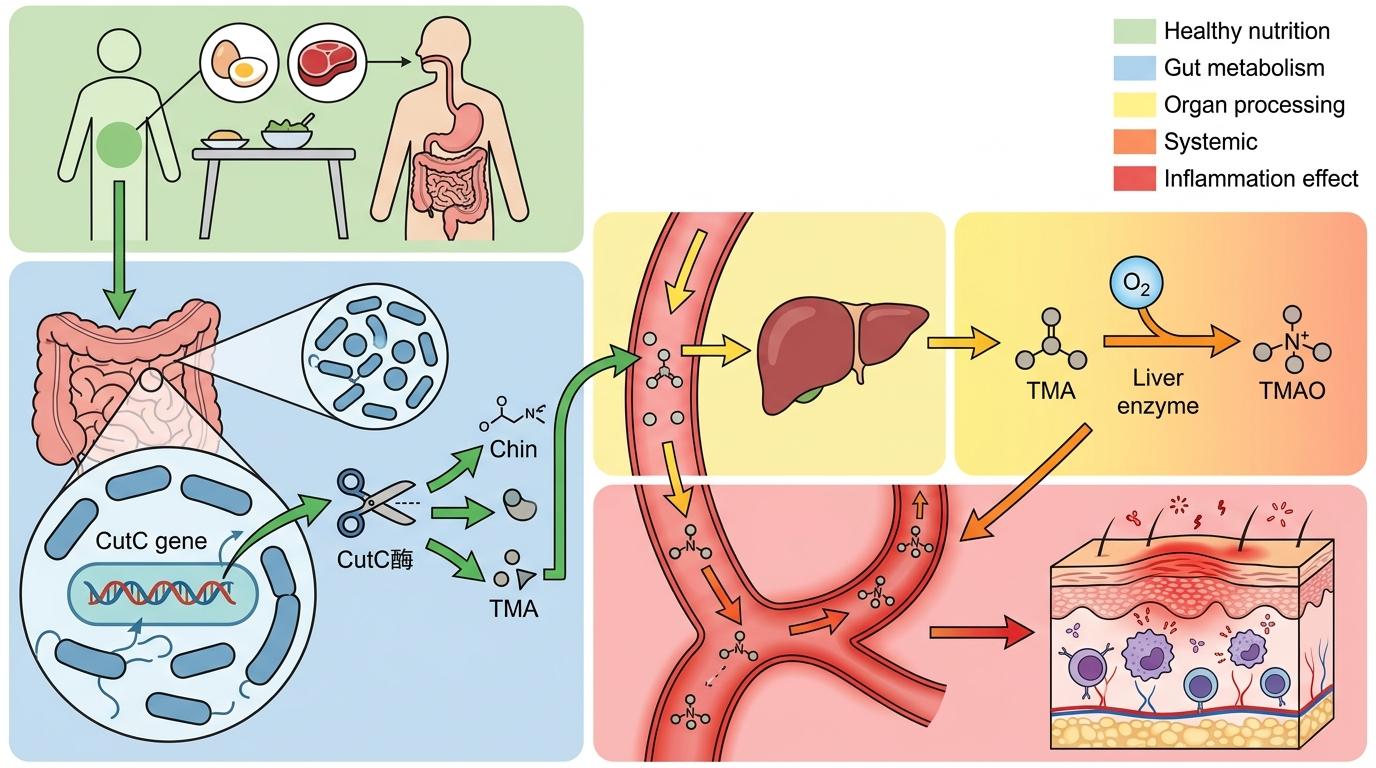
在小鼠实验里,肠道上皮TLR4缺陷的小鼠,血浆TMAO水平比正常小鼠高得多,它们的特应性皮炎症状也明显更严重:皮肤红斑范围更大,瘙痒抓挠的频率更高,血清里的IgE(过敏反应的核心抗体)水平翻了好几倍。
TMAO是怎么从肠道跑到皮肤兴风作浪的?关键就在辅助性T细胞(Th2)——特应性皮炎的「炎症发动机」。
研究人员用精密的分子实验追踪发现,TMAO会直接找到免疫细胞里的蛋白磷酸酶5(PPP5),和它紧紧结合。这一结合,就像给PPP5踩了油门,让它的活性大幅增强。而被激活的PPP5,会精准地给PPARγ蛋白「松绑」——把PPARγ上的磷酸基团去掉,让它从「沉睡」状态苏醒。
苏醒的PPARγ是Th2细胞分化的「指挥官」,它会指挥原本中立的CD4+T细胞,大量转化为Th2细胞。这些Th2细胞会跑到皮肤,分泌IL-4、IL-5、IL-13等炎症因子,一方面破坏皮肤屏障,让过敏原更容易入侵;另一方面刺激身体产生更多IgE,形成「过敏-炎症」的恶性循环。
更关键的是,如果在CD4+T细胞里特异性敲除PPARγ,哪怕小鼠血浆里的TMAO再高,皮肤炎症也不会加重——这直接坐实了PPARγ是TMAO驱动皮肤炎症的核心靶点。
临床数据也印证了实验室的发现:特应性皮炎患者血浆里的TMAO水平,比健康人高出近40%,而且TMAO浓度越高,患者的湿疹面积和严重度指数(EASI)、血清IgE水平也越高。英国生物库的大样本数据还显示,高胆碱饮食的人群,特应性皮炎的发病风险比普通人高15%——这和TMAO的生成路径完全吻合。
但要把这个发现变成治疗手段,还有不少难题。比如,怎么精准降低肠道里的TMAO?直接补充嗜黏蛋白阿克曼菌,虽然能在一定程度上恢复肠道菌群平衡,但这种菌对生存环境要求极高,口服后很难在肠道定植;抑制CutC菌的生长,又可能破坏肠道菌群的整体平衡。
更现实的问题是,每个人的肠道菌群都是独一无二的,TMAO的生成效率也因人而异,很难用一套方案覆盖所有患者。目前的研究还停留在动物实验和关联分析阶段,要验证「降低TMAO就能缓解特应性皮炎」,还需要大规模的临床干预试验。
我们总把皮肤当成独立的器官,却忘了它和肠道共享着一套「免疫通讯网络」。肠道里的每一种细菌、每一个代谢产物,都可能像远程遥控器一样,操控着皮肤的健康。
「肠道安,则皮肤宁」,这不是一句养生口号,而是被分子机制印证的科学逻辑。未来的皮肤病治疗,或许不再只盯着皮肤表面的疹子,而是要从调整肠道菌群、调控代谢产物入手——毕竟,解决问题的根源,永远比缓解症状更有效。