对抗知识焦虑,从看懂这条开始
App 下载
老药新用:糖皮质激素瞄准肾癌致命代谢环
葡萄糖代谢|糖皮质激素|H4K12乳酰化|VHL基因缺陷|透明细胞肾癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
葡萄糖代谢|糖皮质激素|H4K12乳酰化|VHL基因缺陷|透明细胞肾癌|肿瘤学|医学健康
70%的透明细胞肾癌患者体内,都存在一个致命的“代谢死循环”——VHL基因缺陷让肿瘤细胞陷入“假性缺氧”,疯狂消耗葡萄糖产乳酸,而乳酸又反过来给肿瘤“加油”,让它越涨越快。过去十年,针对这个通路的靶向药最多只能让25%的患者肿瘤缩小,多数人最终还是会耐药。直到2026年4月,北京大学、北大第一医院与美国德州大学西南医学中心的联合团队,从一种常用老药里找到了打破循环的钥匙。
你可以把肿瘤细胞的基因组想象成一本被乱涂乱画的书,组蛋白就是固定书页的夹子,而H4K12乳酰化(H4K12la)就是夹子上的一个“打开”标记——它会把和糖酵解相关的书页翻到最外面,让肿瘤细胞疯狂生产乳酸。
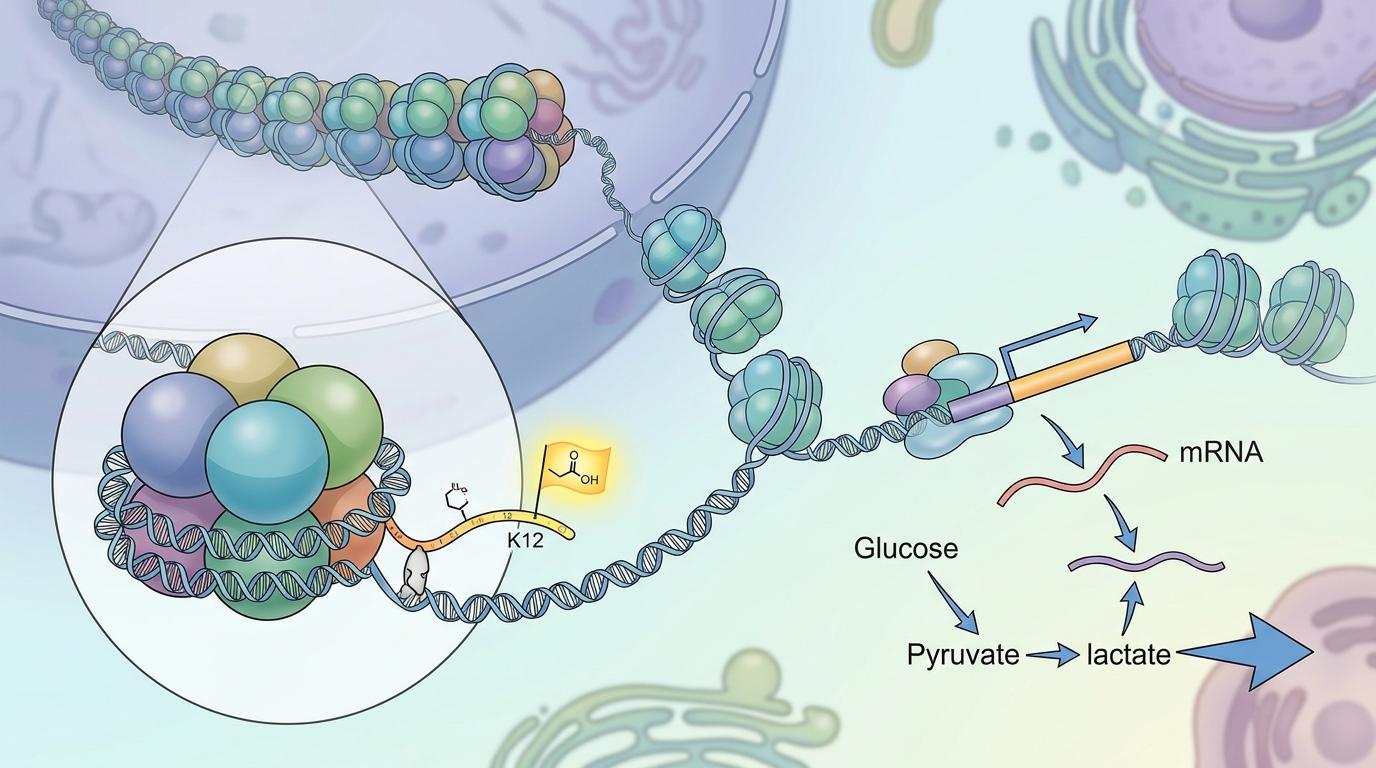
但真实的机制比这更精确:VHL缺陷的肾癌中,H4K12la会精准粘在糖酵解关键酶PGK1的基因启动子上,让PGK1的产量飙升。PGK1就像一台高速运转的乳酸发生器,产出的乳酸又会反过来给更多组蛋白加上H4K12la标记,形成“乳酸越多→标记越多→乳酸更多”的正反馈环。临床数据显示,肾癌组织里的H4K12la水平比正常肾组织高3倍以上,而且标记越多,患者的肿瘤分期越晚,五年生存率越低。
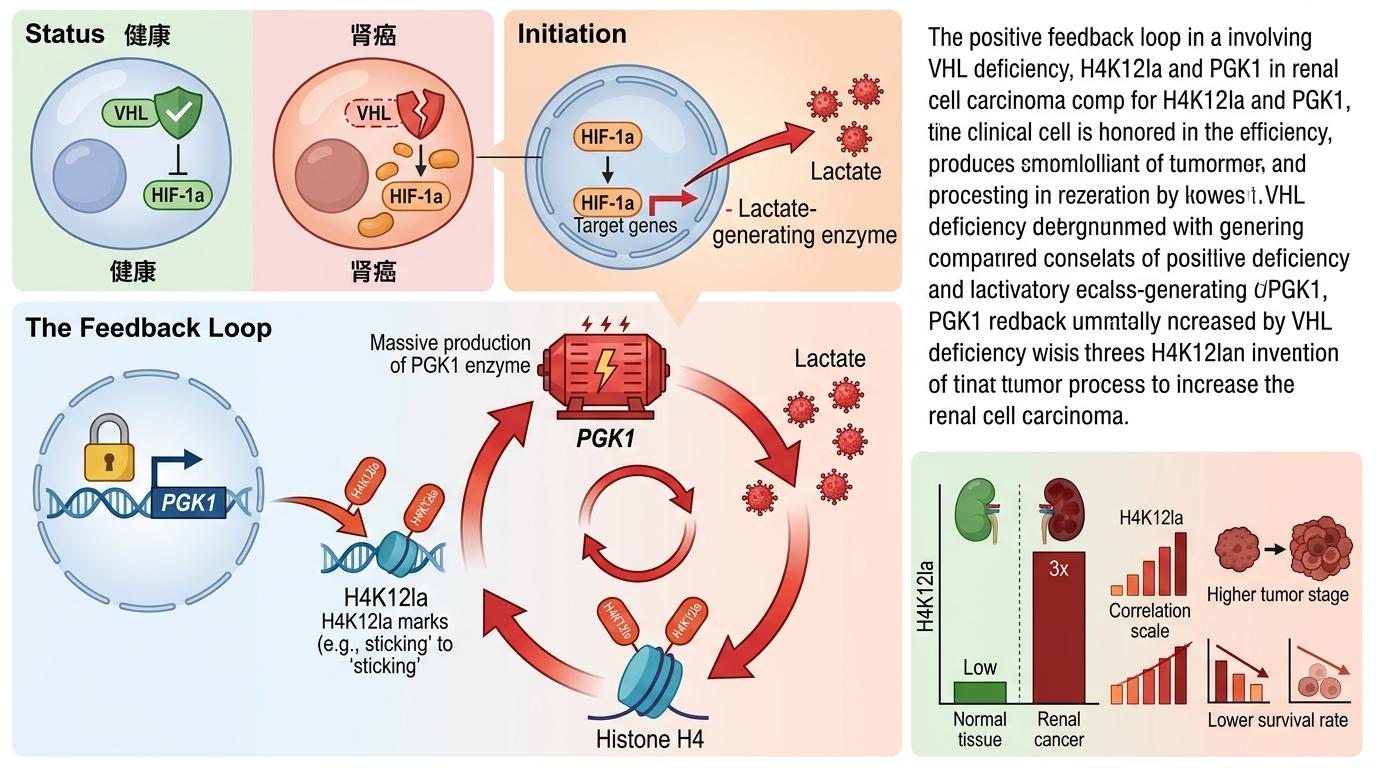
研究团队做了个简单的实验:给肿瘤细胞加了能阻断乳酸生成的药物,结果H4K12la水平直接下降了40%,肿瘤细胞的增殖速度也慢了一半。这证明,只要切断乳酸的供应,就能打破这个死循环。
研究团队用高内涵药物筛选了上千种已上市药物,最后把目光锁定在了糖皮质激素身上——就是那种常用的抗炎、抗过敏老药,比如地塞米松。
它的作用路径很直接:糖皮质激素通过结合细胞内的糖皮质激素受体,直接抑制糖酵解相关基因的转录,从源头减少乳酸的生成。更关键的是,这种抑制在VHL缺陷的肾癌细胞里特别明显——因为这些细胞对糖酵解的依赖度远高于正常细胞,相当于“打蛇打七寸”。实验数据显示,用地塞米松处理后,VHL缺陷肾癌细胞里的乳酸浓度下降了30%,H4K12la水平下降超过40%,细胞增殖率被抑制了60%。
但老药的问题也不能回避:长期用糖皮质激素可能会导致骨质疏松、代谢紊乱,而且肿瘤细胞也可能通过调整糖皮质激素受体的表达产生耐药。研究团队也承认,目前的实验只在细胞和动物模型里验证了效果,要用到临床上,还需要优化剂量,找到“有效又安全”的平衡点。
既然糖皮质激素能打破乳酸正反馈环,而HIF-2α抑制剂能阻断VHL缺陷带来的假性缺氧信号,研究团队自然想到了把两者结合起来。
在肾癌原位移植模型和患者来源的异种移植模型里,联合用药的效果远超单药:肿瘤体积缩小了70%,而单用HIF-2α抑制剂只能缩小30%。更重要的是,联合用药还能降低肿瘤细胞对HIF-2α抑制剂的耐药性——因为它从代谢层面削弱了肿瘤细胞的生存基础,让靶向药能更精准地发挥作用。
不过这种联合策略也不是万能的:它只对VHL缺陷的肾癌有效,对其他类型的肾癌效果有限。而且目前还没有临床数据,需要进一步的临床试验来验证安全性和有效性。
过去我们总觉得,抗癌药就得是全新研发的“精准导弹”,但这次的研究却告诉我们,那些被我们用了几十年的老药,可能藏着被忽略的精准靶点。
这不仅仅是给肾癌患者找到了一种新的治疗选择,更重要的是,它打通了肿瘤代谢和表观遗传之间的桥梁——原来代谢产物不只是能量来源,还能直接调控基因的表达。代谢为笔,表观为纸,肿瘤写下了自己的生存密码。未来的抗癌治疗,或许不再只是盯着单个基因或蛋白,而是要从整个代谢网络入手,找到肿瘤的“命门”。