对抗知识焦虑,从看懂这条开始
App 下载
癌细胞致命失误:“带伤生产”破解耐药困局
毒副作用|实体瘤|铂类药物|化疗耐药|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
毒副作用|实体瘤|铂类药物|化疗耐药|肿瘤学|医学健康
在癌症治疗的战场上,化疗曾是人类最强大的重型武器。然而,这场战争常常陷入一种令人沮丧的循环:起初有效的药物,在反复使用后,肿瘤细胞仿佛获得了“免疫”,变得刀枪不入,甚至越打越强。这种被称为“化疗耐药”的现象,是现代肿瘤学最棘手的难题之一,尤其是作为多种实体瘤治疗基石的铂类药物,其耐药问题让无数患者和医生束手无策。
传统的应对策略往往是加大火力——提高化疗剂量或更换更强的药物,但这无异于一场“焦土战争”,在杀伤癌细胞的同时,也对患者身体造成了巨大的毒副作用。我们能否找到一种更聪明的战术,不是比拼蛮力,而是找到敌人盔甲上的缝隙,一击致命?一项发表于国际顶尖杂志《Genes & Development》的突破性研究,为我们揭示了这样一条出人意料的路径:利用癌细胞自身的“工作失误”,引爆其内部的一场致命混乱。
细胞的日常运作,就像一个高度精密的蛋白质制造工厂。DNA是生产蓝图,而一种名为“RNA聚合酶II”(RNAPII)的分子机器,则负责沿着DNA蓝图读取指令,生产信使RNA(mRNA),进而制造蛋白质。这是一个秩序井然的过程,拥有一套严格的“交通规则”。
当铂类化疗药物进入细胞,它们会像在蓝图上制造路障一样,在DNA上形成“隆突损伤”。当RNAPII这台“读码器”行驶到损伤点时,便会卡住,生产线被迫暂停。这本是细胞的自我保护机制,一个关键的停车信号。此时,一位名叫p300的“现场调度员”会登场,它的工作是清除卡住的RNAPII,为DNA修复团队争取时间,确保在蓝图修复前,不会生产出任何残次品。这是维持基因组稳定、避免灾难性错误的根本法则。
然而,来自西尔维斯特综合癌症中心的科学家们提出了一个大胆的设想:如果把这位“调度员”p300撤掉,会发生什么?实验结果令人震惊。在p300功能被抑制后,卡在损伤点的RNAPII无法被及时清除。但癌细胞并未因此停工,反而做出了一个疯狂的决定——“闯红灯”。它们强行绕过DNA损伤点,继续“带伤生产”。
这一行为的后果是灾难性的。按照一份破损、涂改的图纸施工,产出的必然是大量结构异常、无法正常折叠的“危楼”——错误蛋白质。这些劣质产品在细胞内部,特别是内质网中疯狂堆积,如同工厂仓库被残次品塞满,引发了剧烈的内部压力,即**“未折叠蛋白反应”(UPR)**。一场由生产失控引发的内部暴乱,就此拉开序幕。
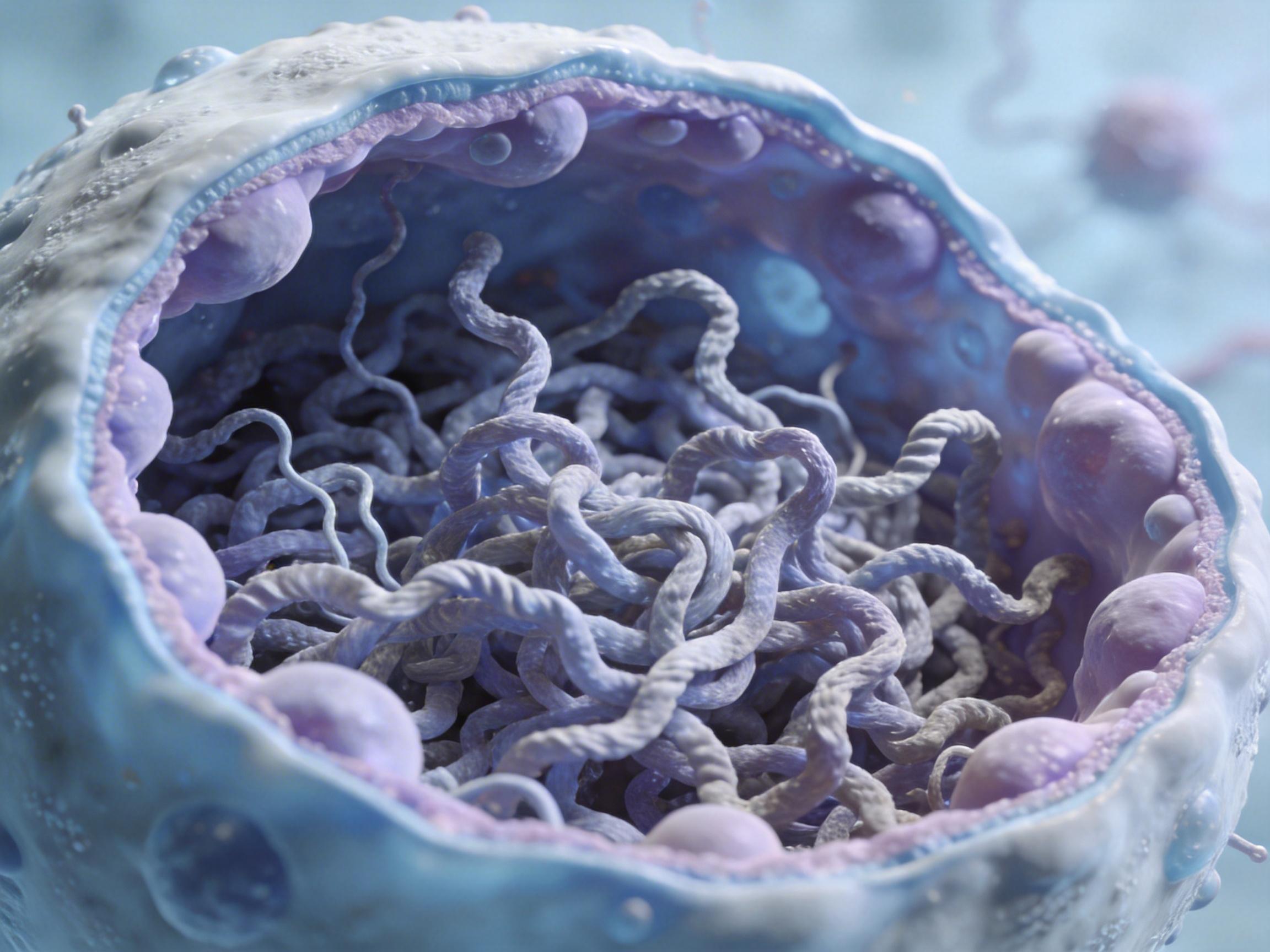
许多耐药的癌细胞之所以“顽固”,正是因为它们进化出了强大的DNA修复能力,能从容应对铂类药物造成的损伤。然而,p300抑制剂的出现,彻底改变了游戏规则。它并不直接增加DNA损伤,而是剥夺了癌细胞在损伤面前“停车检修”的权利。
这就创造了一种精妙的“合成致死”局面:
癌细胞能忍受DNA损伤,却无法承受随之而来的、雪崩般的蛋白质毒性压力。持续的内质网应激,就像一场无法扑灭的内部大火,最终将癌细胞自身吞噬。在结直肠癌和儿童骨肉瘤的患者来源肿瘤模型中,研究者验证了这一策略的威力。单独使用铂类药物或p300抑制剂,效果都十分有限;可一旦两者联手,便能精准而高效地摧毁那些原本坚不可摧的耐药肿瘤。
这标志着一种全新的抗癌哲学:**我们利用的不是药物的杀伤力,而是癌细胞在压力下的脆弱性。**我们不再试图用更强的外力去摧毁堡垒,而是诱使其内部发生结构性坍塌。
这一发现为克服化疗耐药开辟了全新的战场,其核心武器就是靶向p300/CBP的抑制剂。近年来,这类药物的研发已进入快车道,尤其是PROTAC(蛋白降解靶向嵌合体)技术的兴起,更是带来了革命性的变化。
传统的抑制剂如同给p300这个“调度员”戴上手铐,限制其功能。而PROTAC技术则更进一步,它像一个“分子暗杀者”,直接将p300标记出来,引导细胞自身的“垃圾处理系统”(泛素-蛋白酶体)将其彻底降解清除。这种方式更彻底,效果更持久,为临床应用带来了巨大潜力。
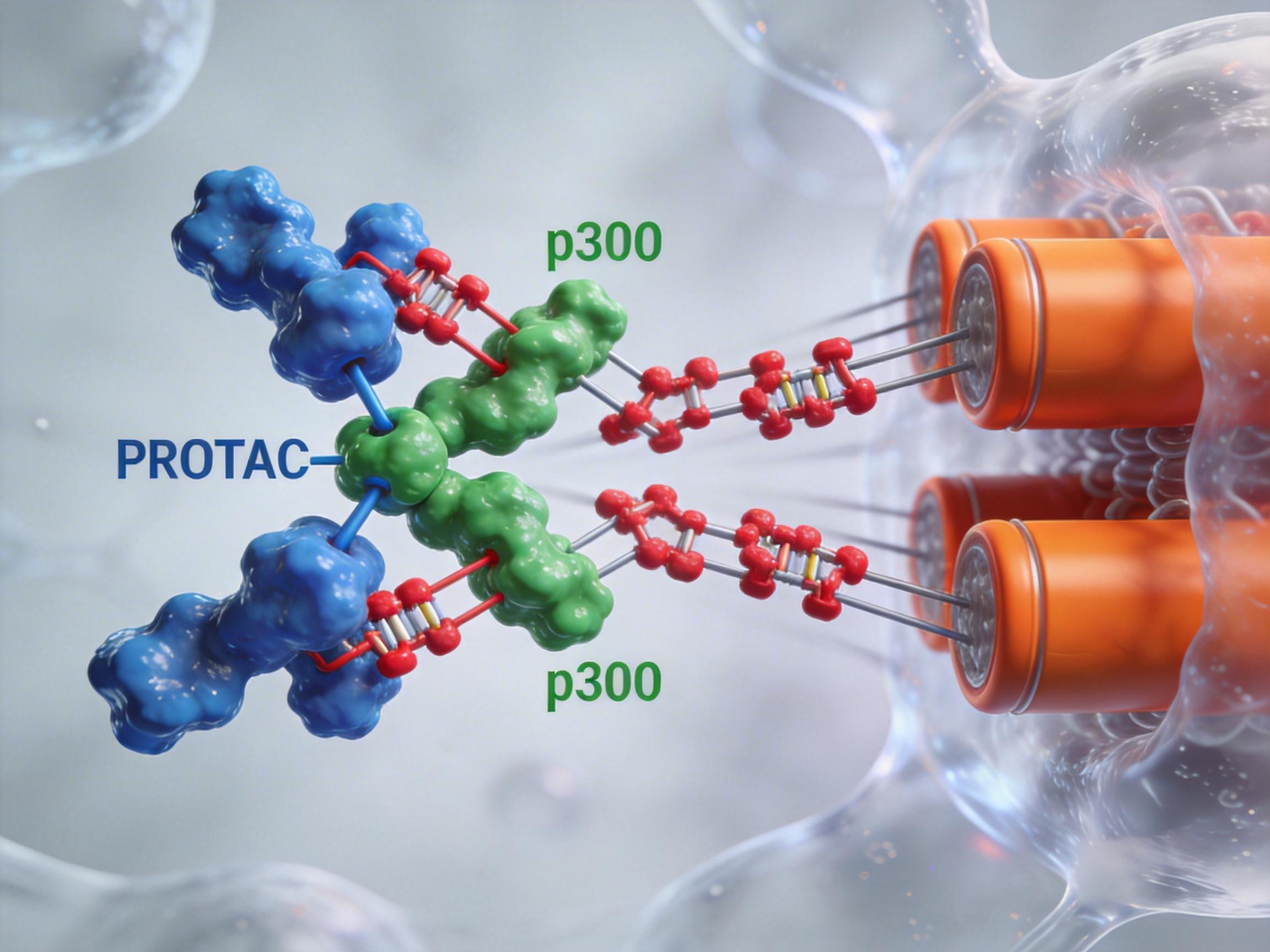
目前,包括瑞士Tolremo Therapeutics公司开发的TT125-802在内的多款p300/CBP抑制剂已进入临床试验阶段,初步数据显示了良好的安全性和克服耐药的潜力。这些新一代药物的目标并非取代化疗,而是与之协同作战,让那些因耐药而治疗选择枯竭的患者,能够重新对可耐受剂量的化疗产生反应。
“带伤生产”策略的成功,刷新了我们对DNA损伤反应的认知:真正的危险,有时并非来自损伤本身,而是来自细胞拒绝按下“暂停键”后引发的连锁灾难。
这为未来的肿瘤治疗描绘了一幅更智慧的蓝图:
从强力攻坚到智取软肋,人类对抗癌症的战争正在进入一个新纪元。通过揭示并利用癌细胞在生存压力下暴露出的内在缺陷,我们或许终将学会如何让这些最狡猾的敌人,在自身的混乱与失序中走向灭亡。