对抗知识焦虑,从看懂这条开始
App 下载
猪瘟病毒的隐秘协作:DHODH如何成为帮凶
分子机制|南京农业大学|线粒体自噬|DHODH|猪瘟病毒|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
分子机制|南京农业大学|线粒体自噬|DHODH|猪瘟病毒|感染性疾病|医学健康
当猪瘟病毒悄悄潜入猪的细胞,它没有忙着直接复制,而是先找到了一个住在线粒体内膜上的“车间主任”——二氢乳清酸脱氢酶,简称DHODH。这个DHODH本来是给细胞生产“核酸积木”嘧啶核苷酸的关键角色,却被病毒策反,成了帮凶。南京农业大学和东北农业大学的团队刚揭开这场分子勾结的细节:病毒不仅能把DHODH绑到线粒体上干活,还能让它激活细胞的“垃圾处理系统”线粒体自噬,为病毒复制扫清障碍。更有意思的是,这套手段只对瘟病毒管用,换了登革病毒这类黄病毒,反而会起反效果。为什么DHODH会成为病毒的“专属内应”?
你可以把DHODH想象成细胞里的“核苷酸车间主任”——它守在线粒体内膜上,催化嘧啶核苷酸合成的关键一步,而嘧啶是病毒复制遗传物质的核心原料。但这次的研究发现,它还有个隐藏身份:自噬流的“检票员”。
自噬就像细胞的垃圾回收系统:先把受损线粒体、错误蛋白这些“垃圾”装进自噬体的“垃圾袋”,再送到溶酶体这个“垃圾站”降解。而DHODH就是管着垃圾袋和垃圾站能不能顺利对接的人——它通过维持嘧啶代谢的平衡,保证自噬体和溶酶体能正常融合,让自噬流顺畅运行。
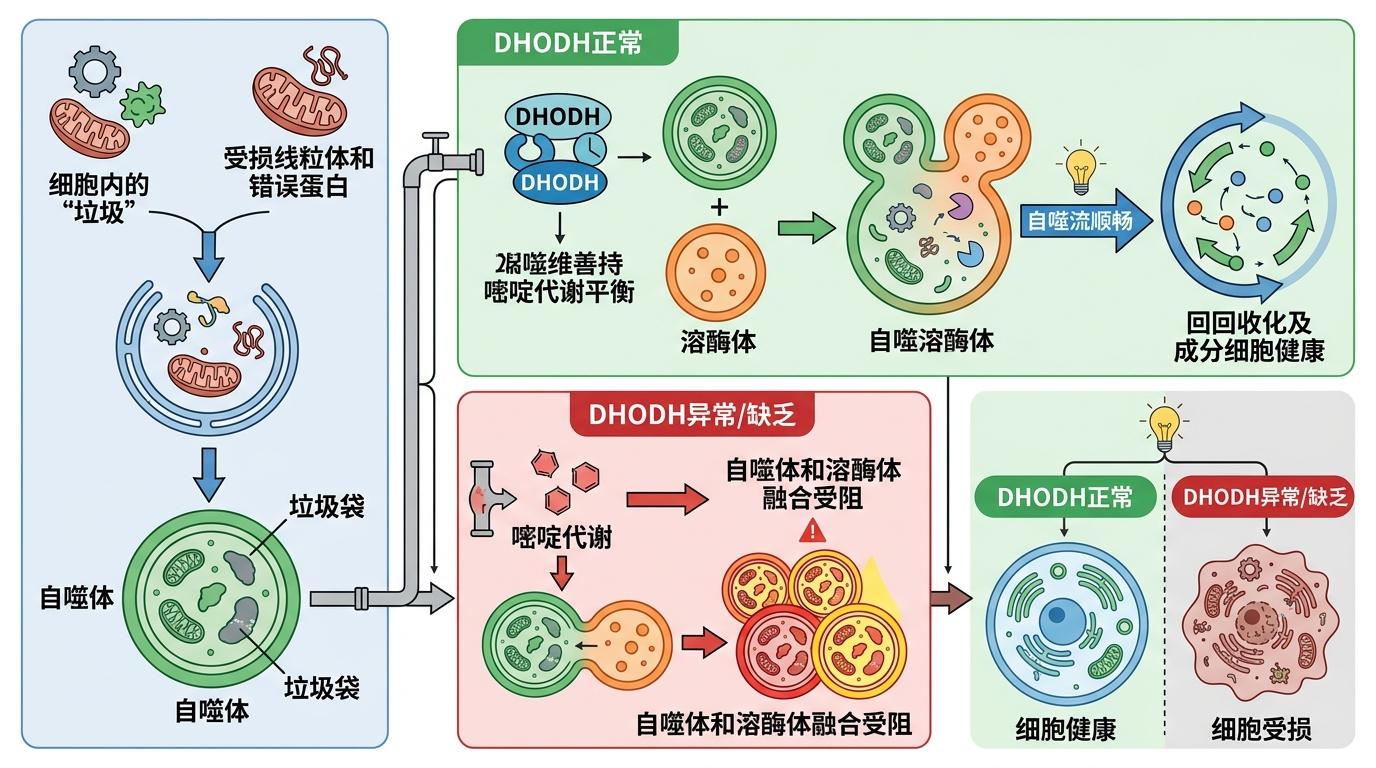
但真实的机制比这更精确:当DHODH缺失,嘧啶核苷酸供应不足,自噬体和溶酶体的融合就会卡住,自噬流断了。对依赖自噬的猪瘟病毒来说,这等于断了它的“复制厂房”;可对登革病毒这类抑制自噬的黄病毒,自噬流被卡反而帮它逃避免疫清除。这就是为什么DHODH的调控会有病毒属特异性。
猪瘟病毒策反DHODH的手段,精准得像一场提前彩排的阴谋。它的非结构蛋白NS4A,就像病毒派出的“联络员”,有两个关键技能:
第一,它能精准找到DHODH,把它牢牢绑定在线粒体膜上——这相当于把车间主任锁在了生产线上,逼着它持续供应嘧啶核苷酸。第二,NS4A自带一个叫LIR的结构域,这个结构域能帮DHODH和自噬标记蛋白LC3牵线搭桥,让DHODH激活线粒体自噬。
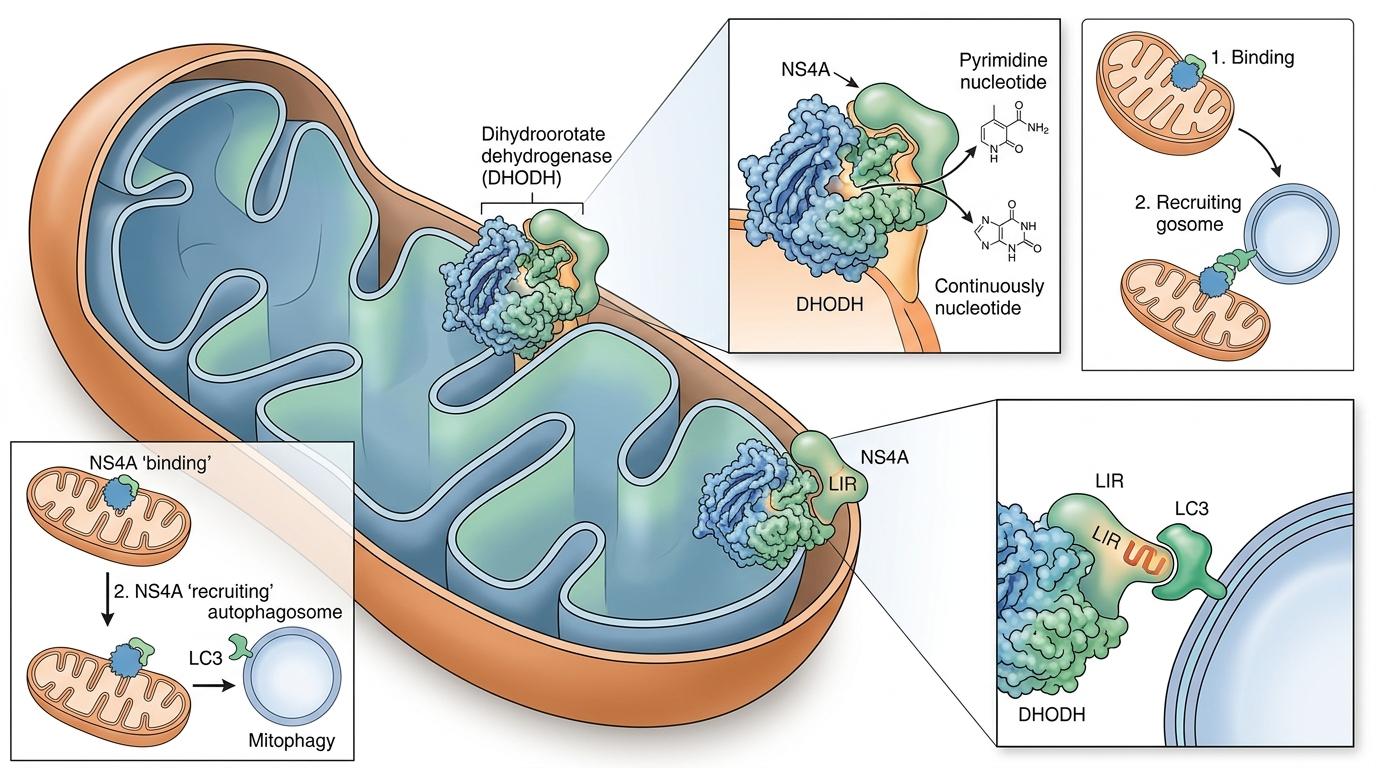
直给逻辑链:
当研究人员敲低DHODH,或者突变NS4A的LIR结构域,线粒体自噬水平直接下降,猪瘟病毒的复制效率也跟着暴跌。而如果外源性补充嘧啶前体,被卡住的自噬体-溶酶体融合又能恢复,病毒复制也跟着“活”过来——这直接坐实了DHODH通过嘧啶代谢调控自噬的核心机制。
DHODH作为抗病毒靶点的潜力,看起来很诱人:它是宿主细胞的蛋白,病毒不容易通过突变产生耐药性,而且已有现成的抑制剂如来氟米特、特立氟胺。但研究也暴露了它的局限:
首先是病毒属特异性。同样是黄病毒科,瘟病毒依赖自噬,DHODH抑制能断它生路;黄病毒有的抑制自噬,DHODH抑制反而会帮它。这意味着不能用同一种DHODH抑制剂对付所有黄病毒,必须精准区分病毒类型。
其次是代谢补偿问题。细胞有嘧啶补救途径,当DHODH被抑制,细胞可以通过回收胞内的嘧啶核苷酸来“补票”,削弱抑制剂的效果。研究显示,联合嘧啶补救途径的抑制剂,能增强DHODH抑制剂的抗病毒效果,但这也意味着药物组合的复杂度会提升。
更现实的挑战是副作用:DHODH是正常细胞代谢的关键酶,长期抑制可能影响免疫细胞增殖,导致免疫抑制。如何让抑制剂精准作用于病毒感染的细胞,而不影响正常细胞,是后续研发必须解决的问题。
当我们把镜头拉远,这场发生在细胞内的分子勾结,其实是病毒与宿主亿万年共演化的缩影——病毒总能找到宿主细胞的“软肋”,而人类的每一次发现,都是在为下一场对抗攒筹码。
DHODH的发现,不是给所有病毒准备的“万能解药”,而是给瘟病毒这类依赖自噬的病原体,量身定做了一把“代谢钥匙”。它提醒我们,抗病毒治疗的未来,从来不是找一个通用靶点,而是精准破解每一种病毒的“生存诡计”。
代谢为轴,自噬为刃,方破病毒诡计。