
11 天前

11 天前
凌晨两点,32岁的李芸盯着天花板流泪——腰椎间盘突出的疼已经缠了她四个月,吃了三种止痛药还是没法平躺。而她丈夫上周摔断肋骨,不到两周就敢抱着孩子举高高。"女人就是怕痛",婆婆的话像根针,但李芸知道,这不是矫情。2026年密歇根州立大学的一项研究,终于把藏在男女身体里的疼痛密码摊开:我们以为的"脆弱",其实是两套完全不同的疼痛缓解系统在运转。为什么男性疼得快好得也快?答案藏在一种叫白介素-10的细胞因子和雄激素的联手里。
你可以把身体的炎症疼痛想象成一场小区火灾——促炎细胞因子是四处蔓延的火苗,而白介素-10(IL-10)就是专门浇灭疼痛的消防水枪。它是一种抗炎细胞因子,能直接按住TNF-α、IL-1β这些"纵火犯"的活性,还能降低感觉神经元的兴奋性,相当于切断了火灾报警的电线。
但真实的机制比这个比喻更精准:IL-10的主要来源是一种叫"IL-10单核细胞"的免疫细胞,它们会在炎症部位聚集,通过向表达IL-10受体1(IL-10R1)的感觉神经元发送信号,直接下达"停止疼痛"的指令。密歇根州立大学的团队在小鼠实验中发现,雄性小鼠皮肤炎症部位的IL-10单核细胞数量,比雌性小鼠多了近一倍——这就是男性疼痛缓解更快的核心原因。
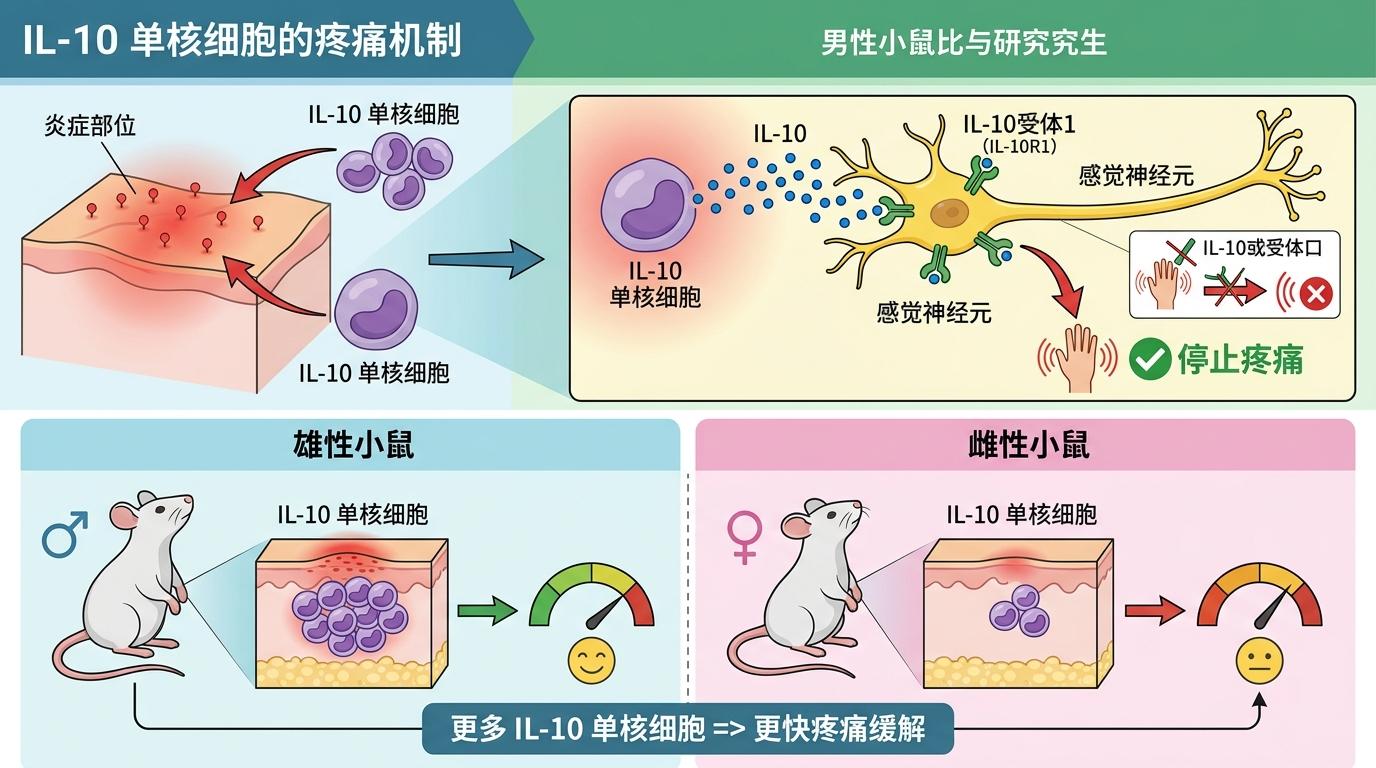
更关键的是,这个机制在人类身上同样成立:AURORA创伤后疼痛研究显示,男性受伤后血液中的IL-10水平比女性高37%,单核细胞数量多22%,对应的疼痛缓解速度比女性快41%。
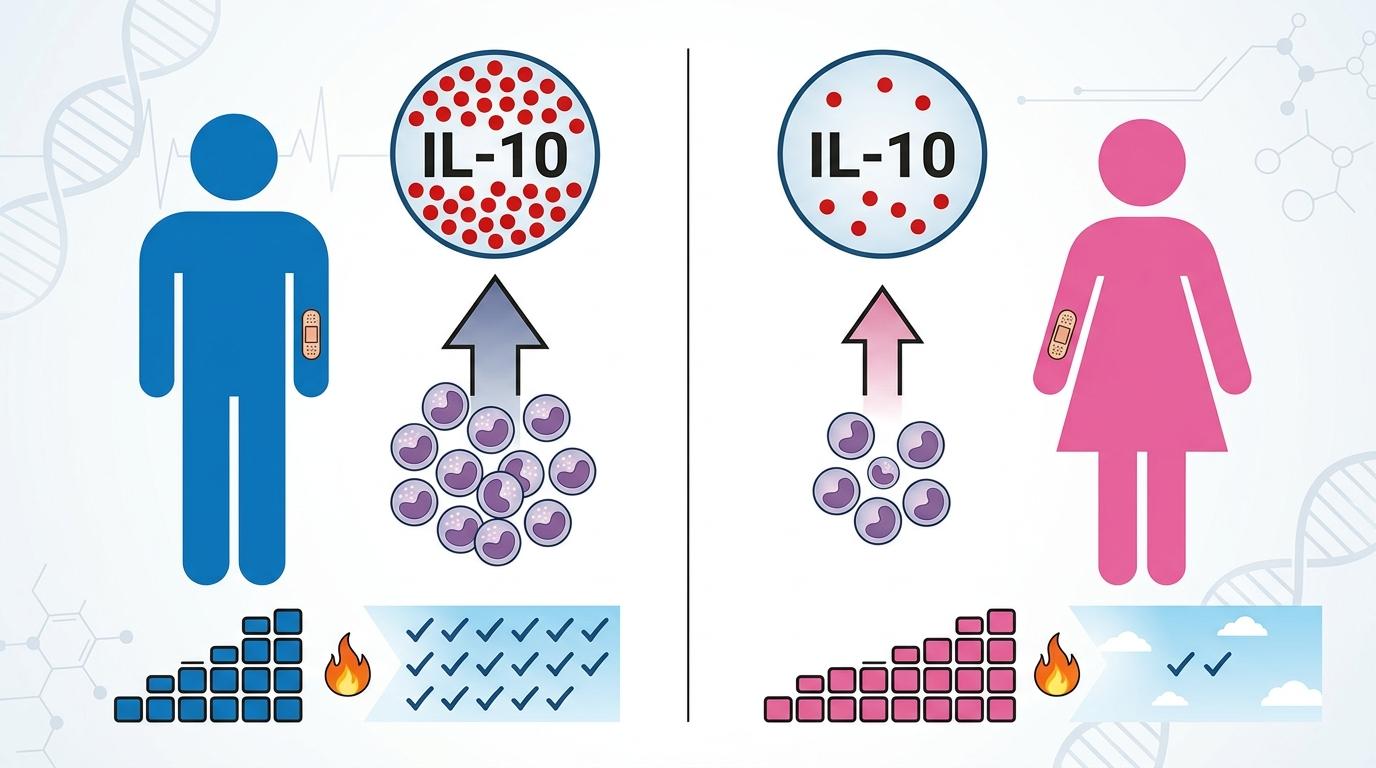
如果说IL-10单核细胞是救火队,那雄激素就是调度指挥官。研究团队通过小鼠实验证实,正是雄激素信号调控着IL-10单核细胞的数量:
具体的分子路径很清晰:雄激素会结合单核细胞表面的雄激素受体,激活一系列基因表达,促使单核细胞大量分泌IL-10。同时,雄激素还能调控脂质介质的生成,比如促进Resolvin D1这种"炎症消退因子"的产生,进一步放大IL-10的止痛效果。
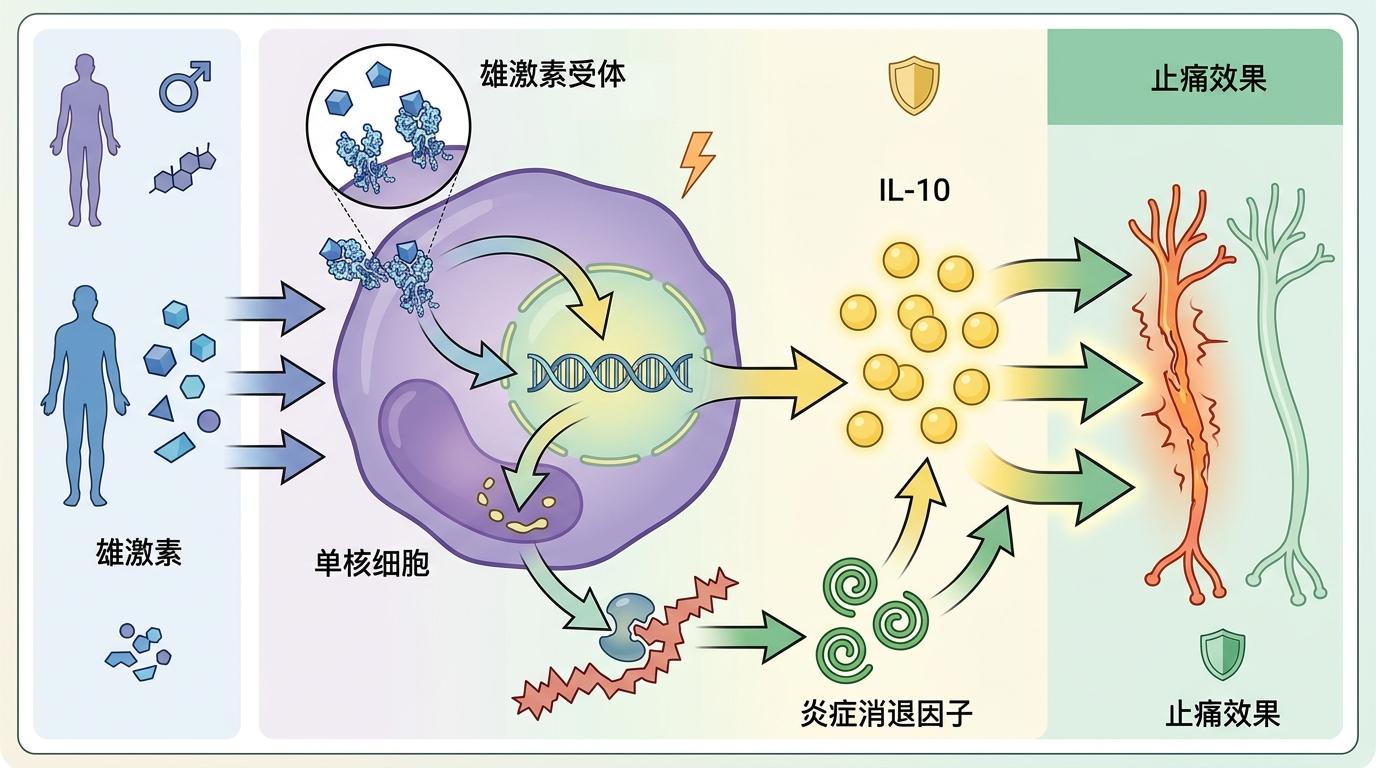
这里有个容易被忽略的细节:雄激素的止痛作用不分性别——男性体内的天然高水平雄激素让他们自带优势,而女性如果体内睾酮水平较低,疼痛持续时间会明显更长。临床数据显示,低睾酮的女性慢性疼痛患者,疼痛评分比睾酮水平正常的女性高2.3分(10分制)。
但生物学差异只是硬币的一面,女性的疼痛负担还叠加了社会偏见的重量。2024年《美国科学院院刊》的研究分析了2万份疼痛患者出院记录,发现了扎心的事实:
更讽刺的是,当研究人员给医护人员提供除性别外完全相同的患者资料时,他们给男性患者打出的疼痛评分平均比女性高1.2分——"女性更爱夸大疼痛"的刻板印象,正在让真实的疼痛被漠视。
值得警惕的是,这项新研究的价值不止于揭示生物学机制,更在于打破偏见:女性不是"怕痛",而是她们的身体天生缺少一支更强大的止痛救火队,同时还要在医疗系统中为自己的疼痛"证明真实性"。
当我们终于把"脆弱呵,你的名字叫女人"这句台词从疼痛话题中划去,真正的改变才刚刚开始。未来的疼痛治疗或许会出现性别定制的方案:给女性补充能促进IL-10分泌的脂质介质,或是用基因疗法增强单核细胞的止痛活性。
但更重要的是,我们需要把生物学的真相传递给每一个医护人员——当女性说"我疼"时,这不是情绪的表达,而是身体发出的真实信号。
疼痛有性别,止痛不该有偏见。
点击充电,成为大圆镜下一个视频选题!