对抗知识焦虑,从看懂这条开始
App 下载
疱疹病毒复制引擎被“锁死”:药物研发迎新突破?
EB病毒|耐药性|阿昔洛韦|疱疹病毒|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
EB病毒|耐药性|阿昔洛韦|疱疹病毒|感染性疾病|医学健康
在我们每个人的身体深处,可能都潜伏着一位古老的“访客”——疱疹病毒。这个庞大的病毒家族,从引发唇边水泡的单纯疱疹病毒(HSV),到童年记忆中的水痘,再到与某些癌症相关的EB病毒,它们以一种独特的方式与人类共存:一旦感染,终身潜伏。它们藏匿于我们的神经元中,如同休眠的火山,在人体免疫力下降时便会伺机喷发,引发恼人的、有时甚至是致命的疾病。
几十年来,人类与疱疹病毒的斗争从未停歇。以阿昔洛韦为代表的抗病毒药物,曾是我们手中的利器。但病毒在不断的进化中学会了“闪躲”,耐药性问题日益严峻,尤其是在免疫力低下的人群中,这场战斗的天平似乎正在向病毒倾斜。我们迫切需要新的武器,一种能够精准打击病毒要害,且让其难以逃脱的新策略。现在,一扇通往未来的大门似乎正在被打开。
就在2025年12月29日,国际顶尖期刊《细胞》(Cell)发表的一篇研究,为这场旷日持久的战争带来了突破性的曙光。由哈佛医学院Jonathan Abraham教授领导、博士后于子朔博士(本科毕业于山东大学)作为第一作者的团队,利用尖端的单颗粒冷冻电子显微镜(cryo-EM)技术,首次“拍摄”到了单纯疱疹病毒1型(HSV-1)核心复制机器在工作时,被一类新型药物“锁死”的决定性瞬间。
这项研究的核心,是一种被称为**解旋酶-引物酶抑制剂(HPIs)**的新型抗病毒药物。它们的前景广阔,部分药物已进入临床试验阶段,甚至已在日本获批上市。但在此之前,它们究竟如何让病毒“刹车”,其精确的作用机制一直是个谜。而Abraham团队的研究,则像一部高分辨率的慢动作摄像机,清晰地揭示了这一切:
要理解这一突破的深刻含义,我们必须将视线深入到分子层面,看看病毒是如何疯狂复制自身的。病毒的DNA复制过程,就像一条高速运转的工厂流水线。
流水线的起点,是解旋酶-引物酶(H/P)复合物。它由三个蛋白亚基(UL5、UL52和UL8)组成,其核心部件UL5解旋酶,就像一个分子马达,负责解开病毒双链DNA的“拉链”,为后续的复制提供模板。这个马达的动力来自ATP能量,其内部的两个结构域(1A和2A)需要像钳子一样不断开合,才能拉着DNA前行。
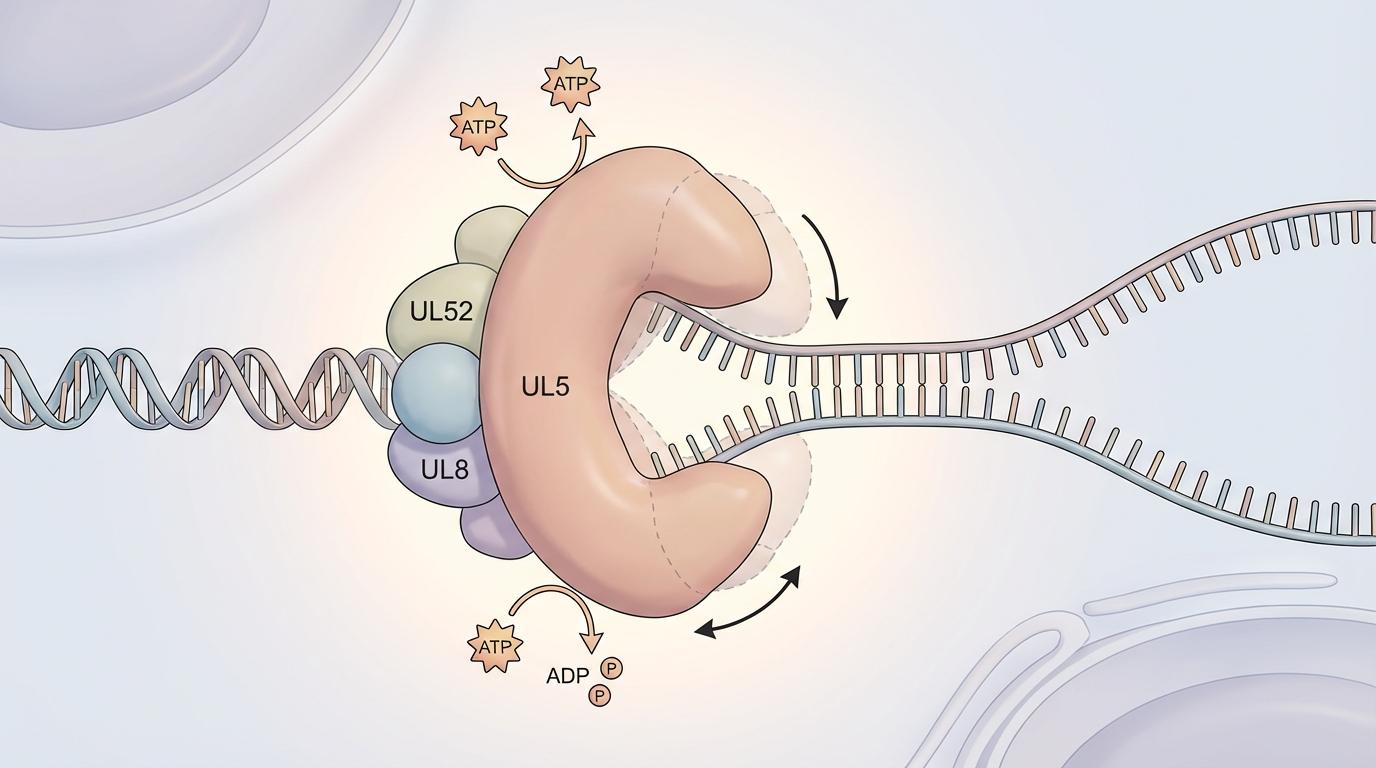
而这项新研究的第一个震撼发现,就是揭示了HPIs药物的“刹车”机制。尽管三种药物的化学结构各不相同,但它们不约而同地结合到了H/P复合物上同一个**“刹车槽”**里。这个“刹车槽”恰好位于UL5解旋酶1A和2A两个结构域的关节处。
药物分子一旦嵌入,就如同在钳子的转轴处打入了一个楔子,阻止了钳子的闭合。马达的关节被卡住,无法进行开合运动,自然也就无法水解ATP获取能量,更无法沿着DNA移动。整个复制的“火车头”就这样被强行熄火,卡死在了轨道上。
为了动态验证这一“锁死”效应,研究团队还动用了另一项“黑科技”——单分子光镊。他们将单个DNA分子像琴弦一样拉直,然后观察H/P复合物在上面的运动。实验结果完美印证了结构学的发现:加入药物后,解旋酶的行进速度明显变慢,并且频繁地“走走停停”,暂停的时间随着药物浓度增加而变长。这无疑是病毒复制引擎被“锁死”的直接证据。
这项研究的意义远不止于解释一种药物的作用机制,它为未来的抗病毒药物研发描绘了一幅精准的“蓝图”。
首先,它解释了现有HPIs药物的局限性。为什么Pritelivir对单纯疱疹病毒有效,但对同家族的水痘-带状疱疹病毒效果不佳,对巨细胞病毒(HCMV)更是几乎无效?答案就藏在那个“刹车槽”的细微差别里。研究发现,虽然UL5解旋酶上的关键氨基酸在不同疱疹病毒中高度保守,但参与构成“刹车槽”边缘的UL52引物酶上的氨基酸却存在差异。在HCMV中,一个关键的氨基酸变化破坏了药物的结合位点,导致药物失效。看清了这一点,科学家们便可以针对不同病毒的“刹车槽”特征,“量身定制”更具靶向性的药物分子,从而有望开发出广谱抗疱疹病毒药物。
其次,它为理解耐药性提供了直接的结构证据。研究确认,许多已知的临床耐药突变,正好发生在“刹车槽”内部。这些突变改变了“刹车槽”的形状,使得药物这个“楔子”无法严丝合缝地插入,从而导致药效下降。
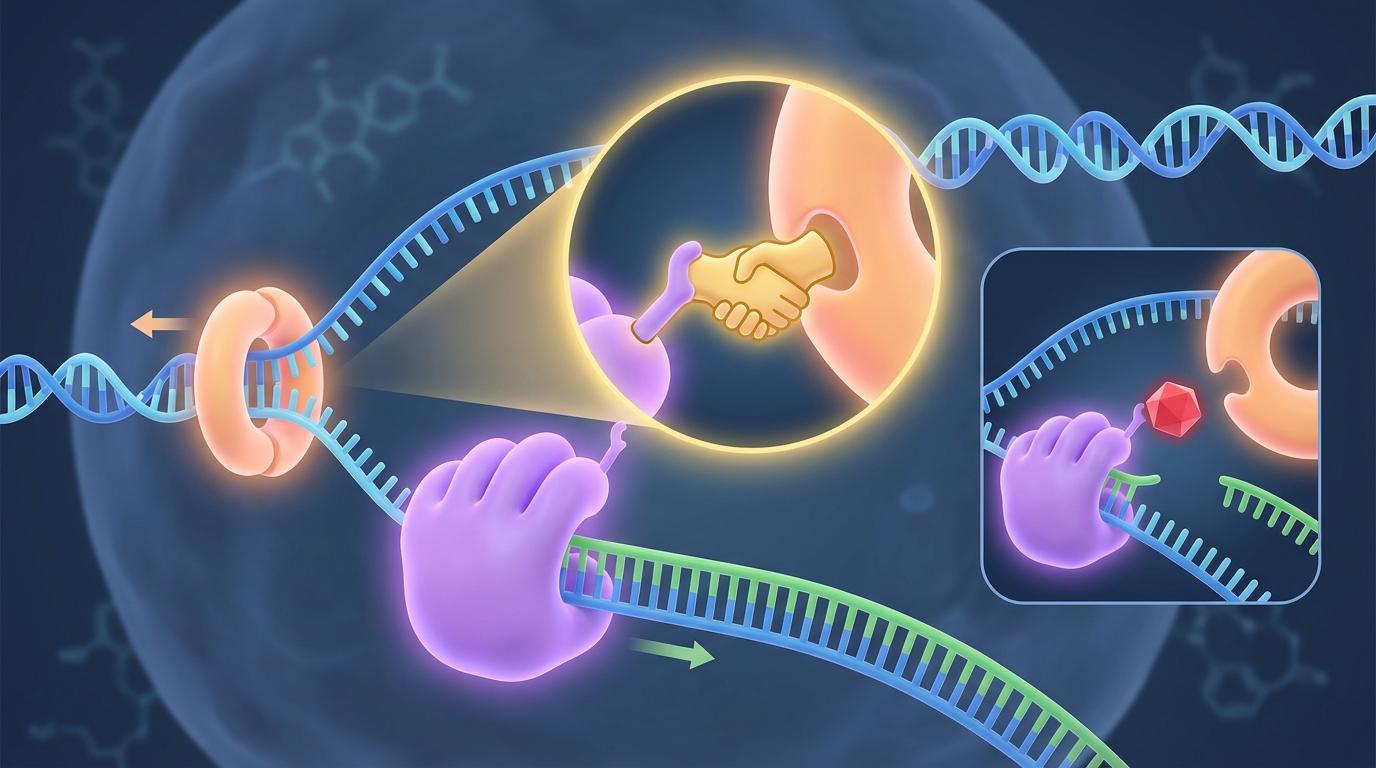
更令人兴奋的是,这项研究还揭示了一个全新的、前所未知的药物靶点。在解析完整的病毒复制叉复合物(包含H/P复合物和DNA聚合酶)结构时,团队发现,负责合成新DNA链的DNA聚合酶(UL30蛋白),会通过其末端一个特殊的FYNPYL序列,与解旋酶(UL5蛋白)进行一次关键的**“握手”**,形成一个稳定的桥梁,从而确保“解拉链”和“造新链”两个步骤的完美协同。这个“握手”界面是病毒复制所必需的。这意味着,科学家们可以开发一类全新的抑制剂,专门用来破坏这次“握手”,从而瓦解整个复制机器的协同工作。这将是一种全新的抗病毒策略。
从基础研究的突破到临床应用的药物,道路依然漫长。哈佛团队的这项工作,是从“看见原理”到“精准设计”的飞跃,它将药物研发从传统的“大海捞针”式的筛选,带入了基于结构的理性设计新时代。
未来的方向已经清晰:
然而,我们必须清醒地认识到,目前所有的抗病毒复制药物,都只能在病毒活跃期发挥作用。对于那些潜伏在神经元中、处于“休眠”状态的病毒,它们依然无能为力。如何安全、有效地清除潜伏病毒,实现对疱疹病毒的彻底治愈,依然是摆在全世界科学家面前的终极挑战。
尽管如此,每一次这样的基础科学突破,都让我们向最终的胜利迈出了坚实的一步。它不仅加深了我们对这个古老对手的理解,更为我们铸造了更锋利的武器。在这场持续了数万年的人类与病毒的战争中,我们正凭借智慧与科技,以前所未有的清晰度,洞察敌人的核心机密,并描绘出终结其威胁的未来蓝图。