
2 个月前

2 个月前
在医学的战场上,癌症与阿尔茨海默病(AD)无疑是两头最令人畏惧的猛兽。然而,一个长期困扰流行病学家的谜团是:这两大顽疾似乎在同一个战场上刻意回避着对方。多年来的数据显示,癌症幸存者患上阿尔茨海默病的风险显著降低,而阿尔茨海默病患者确诊癌症的概率也更低。这奇异的“跷跷板效应”是纯属巧合,还是隐藏着某种深刻的生物学联系?过去,人们猜测这或许是残酷的“生存竞争”,但真相远比想象的更为精妙和主动。
长达十五年的漫漫求索,华中科技大学鲁友明教授带领一支由16名研究人员组成的团队,终于为这个谜团带来了曙光。他们发表在国际顶尖期刊《Cell》上的研究,颠覆了以往的认知:外周癌症并非被动地与AD争夺生存资源,而是主动分泌出一种“信使”蛋白,跨越遥远的血脑屏障,向大脑发起了一场精准的“救援行动”。
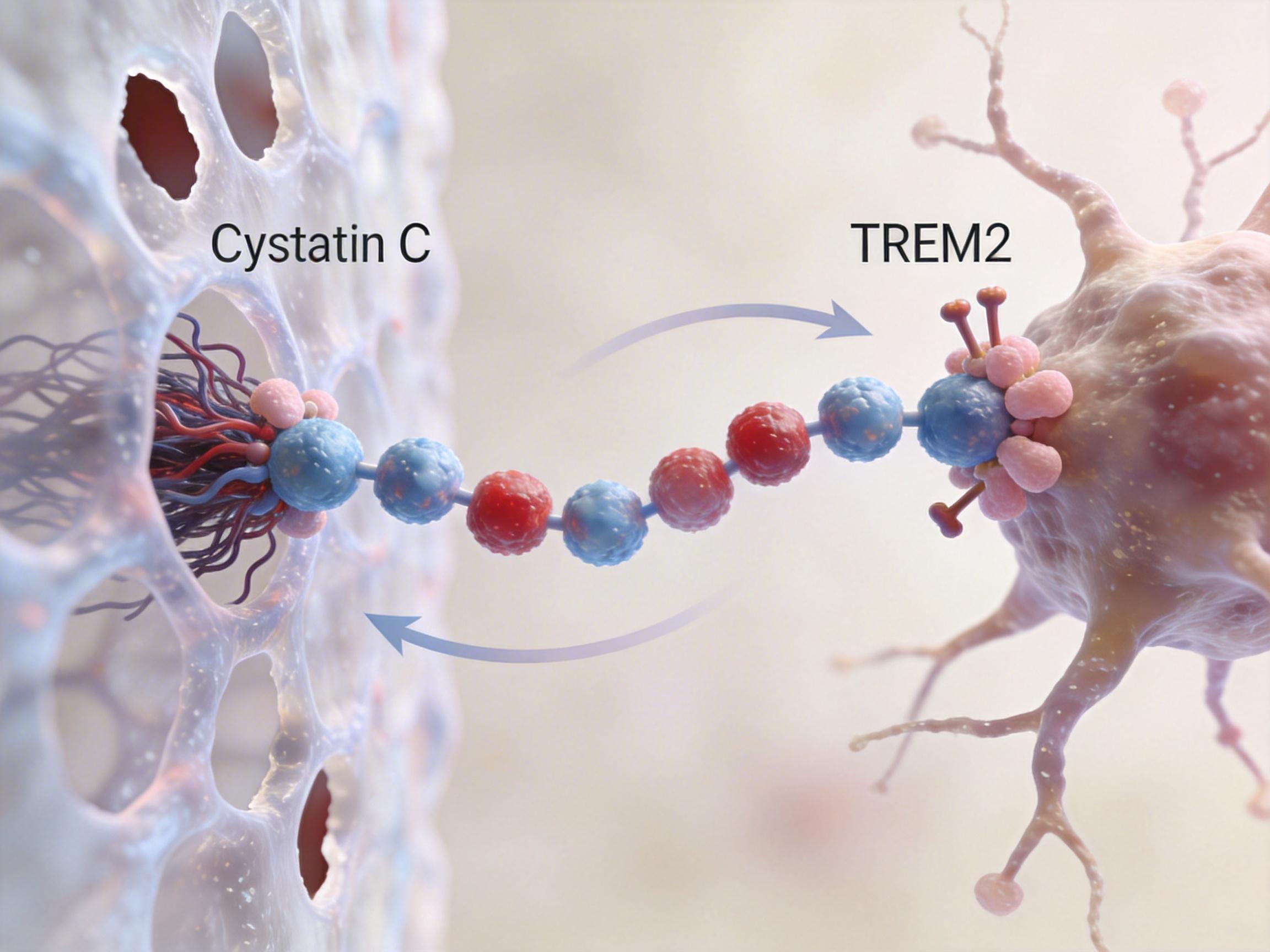
研究团队通过对7种不同肿瘤患者的血浆进行分析,从33种候选分泌蛋白中,最终锁定了一个关键角色——胱抑素C(Cystatin C)。这个通常被用作肾功能评估指标的小分子蛋白,竟是连接癌症与大脑保护的神秘信使。实验证实,无论是肺癌、前列腺癌还是结肠癌,当它们在AD模型小鼠体内生长时,小鼠大脑中标志性的β淀粉样蛋白(Aβ)斑块竟被显著清除,一度衰退的认知记忆能力也得到了惊人的改善。
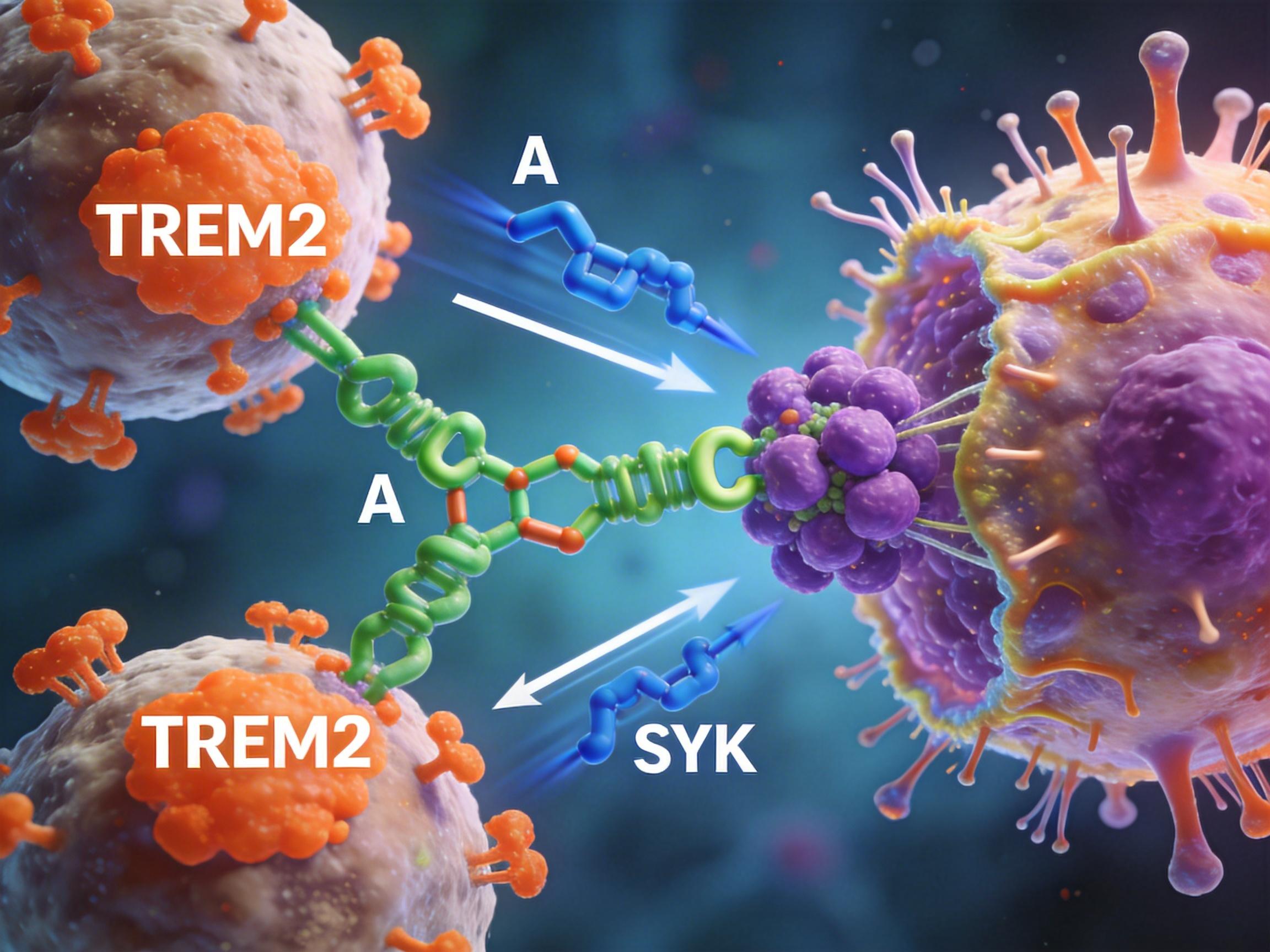
这背后,是一场由癌细胞远程指挥,在大脑中上演的精妙“清扫行动”。其核心,是一个被称为**“三方握手”**的优雅机制。
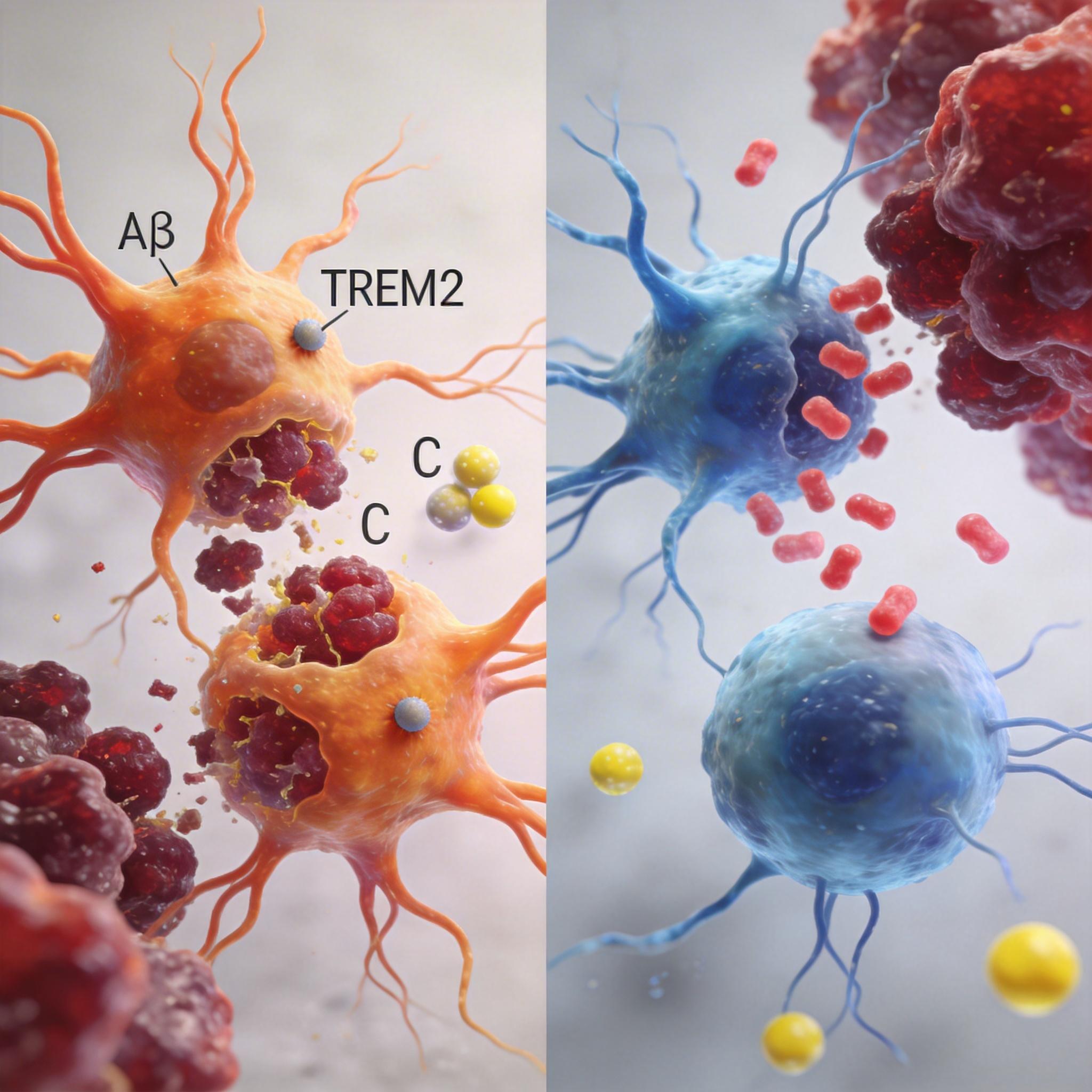
大脑中有一群被称为“小胶质细胞”的免疫卫士,它们本应负责清除Aβ这类有害“垃圾”。但在AD患者的大脑中,这些细胞常常变得“懈怠”,对堆积如山的Aβ斑块视而不见。而胱抑素C的到来,彻底改变了这一局面。
这一发现的颠覆性意义,在于它为阿尔茨海默病的治疗带来了根本性的**“范式转移”**——从被动的“围堵”转向主动的“清扫”。
过去三十年,AD药物研发的主流思路是基于“淀粉样蛋白级联假说”,致力于阻止Aβ的产生或清除可溶性Aβ,如同试图关闭“垃圾工厂”的源头。虽然仑卡奈单抗(lecanemab)等药物在此方向上取得了一定突破,但它们对已经形成的大量致密斑块效果有限,且主要适用于疾病早期。
而胱抑素C开创的新策略,则是增强大脑自身的“垃圾清运”能力。它直接激活内源性的小胶质细胞,让大脑自己的免疫系统去解决问题,这为那些已有大量斑块积累的中晚期患者带来了全新的希望。这不仅是传统“以毒攻毒”智慧的科学例证,更是在分子层面实现了这一理念的现代转化。
然而,这场由癌症发起的“跨界救援”并非没有边界。研究明确指出,胱抑素C的保护作用仅针对Aβ病理,对AD的另一核心病理特征——tau蛋白异常缠结则无明显影响。这也精准地解释了为何流行病学上的“跷跷板效应”具有特异性。同时,这项研究目前主要基于小鼠模型,其在人类中的普适性仍需进一步验证。
尽管如此,它已经为未来开辟了一条充满希望的道路。我们当然不能通过患癌来预防AD,但我们可以“师夷长技以制夷”。未来的研究方向将聚焦于:
从癌症分泌的“副产品”到大脑的“斑块清洁工”,胱抑素C的故事深刻揭示了生命系统的复杂与精妙。它告诉我们,在一个器官中引发灾难的过程,可能在另一个器官中扮演着守护者的角色。疾病之间的相互作用,并非总是简单的叠加或对抗,而是充满了意想不到的跨界调控与动态平衡。
这项研究不仅为攻克阿尔茨海默病这一世纪顽疾提供了全新的武器,更启发我们以一种更宏大、更系统的视角去理解健康与疾病。通过深入解析这些隐藏在疾病“互逆机制”背后的秘密,我们或许能将更多看似“有害”的生物学过程,转化为治愈生命的强大力量。
点击充电,成为大圆镜下一个视频选题!