对抗知识焦虑,从看懂这条开始
App 下载
癌症RNA密码被破解?FOCAS技术揭秘m6A调控
基因表达调控|北京大学刘君团队|RNA化学修饰|N6-甲基腺苷|FOCAS技术|肿瘤学|分子细胞生物学|生命科学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
基因表达调控|北京大学刘君团队|RNA化学修饰|N6-甲基腺苷|FOCAS技术|肿瘤学|分子细胞生物学|生命科学|医学健康
如果说DNA是生命的静态蓝图,那么RNA就是将这份蓝图付诸实践的动态指令集。然而,在这份指令集上,还存在着一层鲜为人知却至关重要的“密码”——RNA化学修饰。其中,**N6-甲基腺苷(m6A)**是最普遍的一种,如同在指令上贴满的“便利贴”,悄无声息地改变着指令的解读方式。长期以来,科学家们知道这些“便利贴”的存在,却苦于没有一副足够精细的“放大镜”,去逐一解读每一张“便利贴”的具体含义,尤其是在癌症这个基因表达极度混乱的复杂疾病中。
就在2025年12月31日,这片迷雾被一道强光刺破。北京大学的刘君团队联合多家顶尖机构,在国际顶级期刊《Cell》上发表了一项里程碑式的研究。他们成功开发出一种名为**FOCAS(Functional m6A Sites Detection by CRISPR-dCas13b-FTO Screening)**的全新高通量筛选技术。
这项技术的本质,是创造了一把“分子手术刀”。它巧妙地将能够精准定位RNA的CRISPR-dCas13b系统(如同一个高精度GPS)与m6A的“擦除器”蛋白FTO相结合。通过这把“手术刀”,研究人员可以在不改变基因序列、不大规模影响全局修饰水平的前提下,对细胞内成千上万个m6A位点进行逐一、精准的“擦除”,并实时观察这一行为对细胞命运,尤其是癌细胞生存与增殖的影响。这标志着m6A研究从宏观的“关联性”分析,迈入了微观的“因果性”验证新纪元。
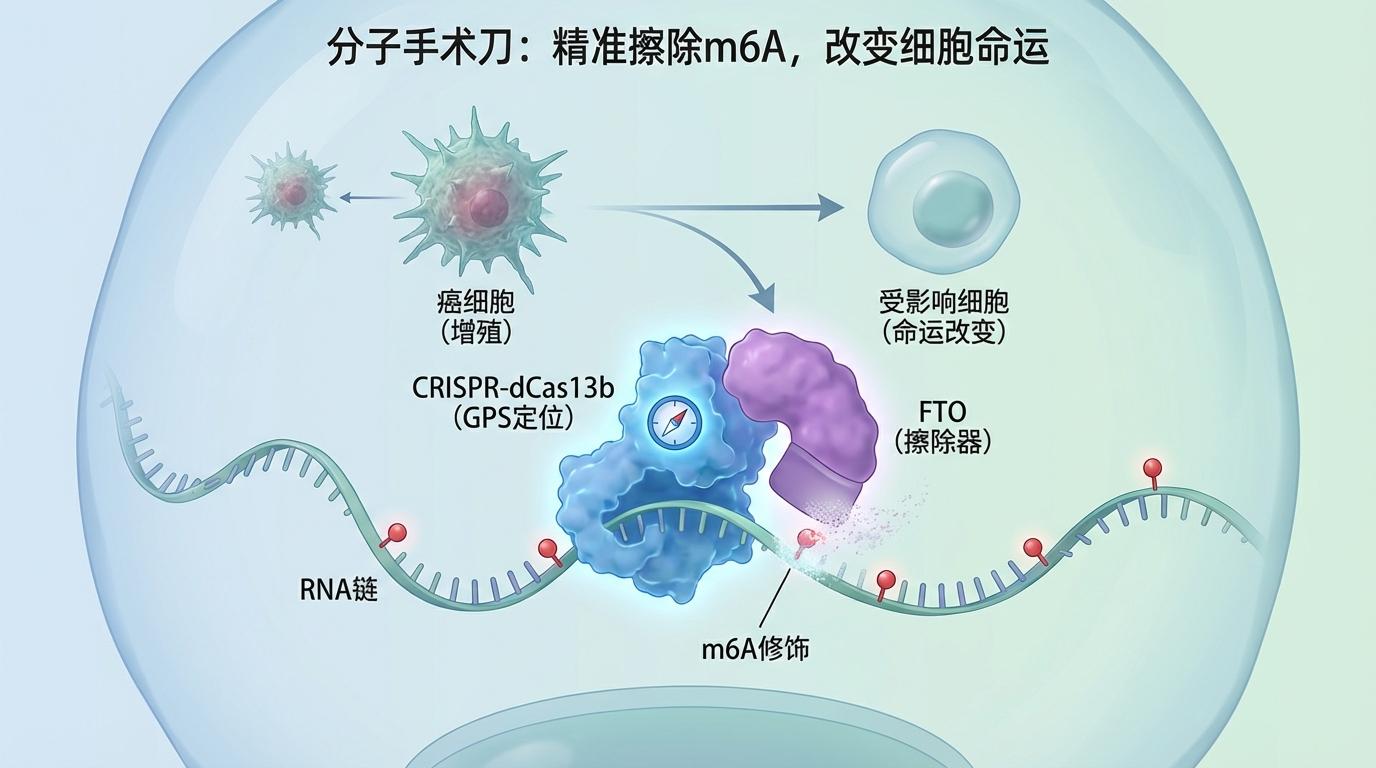
FOCAS技术的应用,揭示了一幅远比想象中更为复杂的m6A调控图景。在针对四种不同癌细胞系的筛选中,研究团队取得了惊人发现:
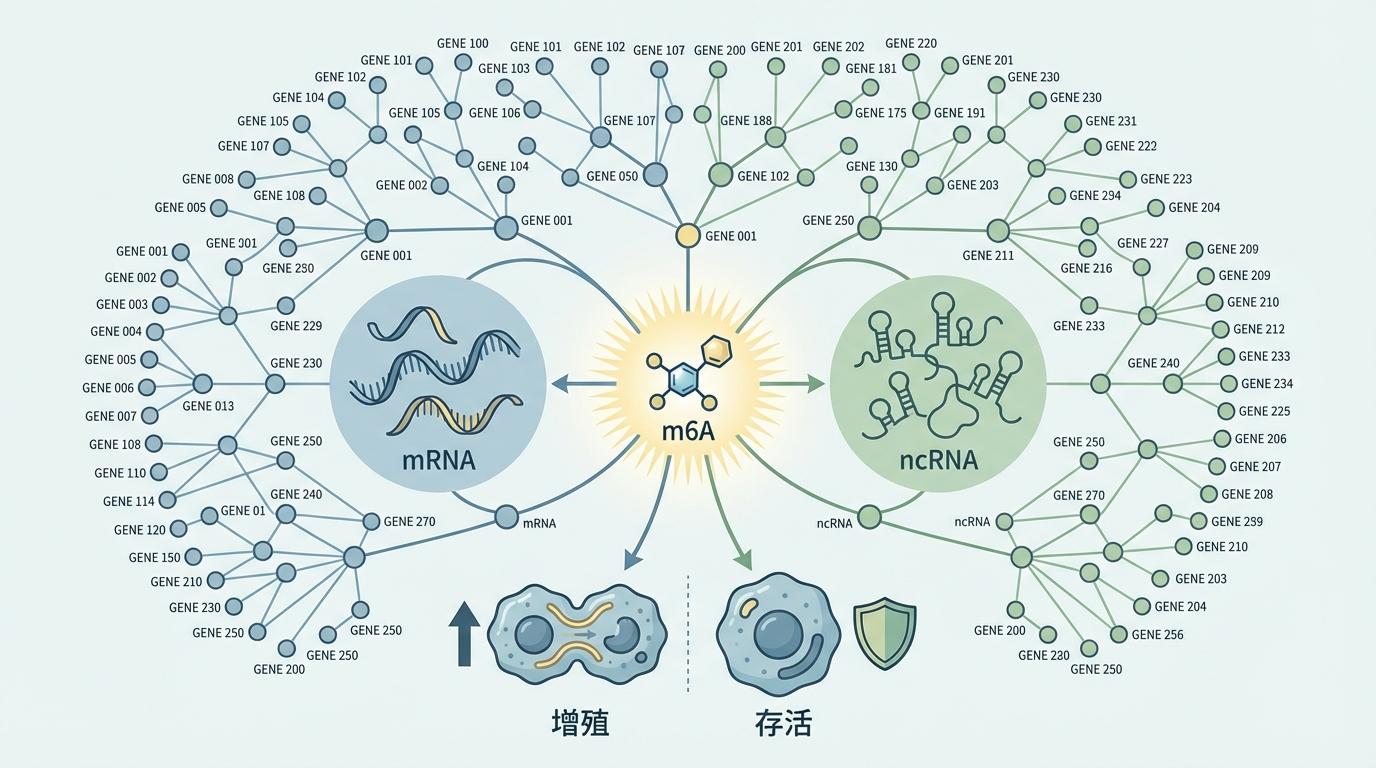
“上下文”决定一切:研究最颠覆性的发现之一,是m6A的功能并非一成不变。同一个基因上的同一个m6A修饰,在不同的癌细胞环境中,或者被不同的“阅读器”蛋白识别时,可能产生截然相反的效果——有时促进癌症,有时抑制癌症。这就像同一条指令,在不同部门会被解读出完全不同的执行方案,揭示了m6A调控的极端情境依赖性和精确性。
通用法则与特异性策略:研究还发现,m6A的调控存在“通用”和“特异”两种模式。一些“通用”的修饰模式普遍存在于多种癌细胞中,多见于与转录等基础生命活动相关的基因上。而另一些“特异”的模式则仅在特定类型的癌细胞中出现,尤其是在非编码RNA上,这暗示着它们可能在特定癌症的发生发展中扮演着“关键棋子”的角色。
跨层级的“对话”:在人类肝癌细胞中,团队进一步揭示了m6A修饰(表观转录组)与基因表达(转录组)之间广泛而深刻的相互作用。更令人兴奋的是,他们发现了一个此前未被报道的潜在抑癌因子KCTD1,其表达受到m6A的调控,并且能进一步影响到染色质层面的组蛋白修饰。这证实了m6A是连接细胞内多层级基因调控网络的核心枢纽。
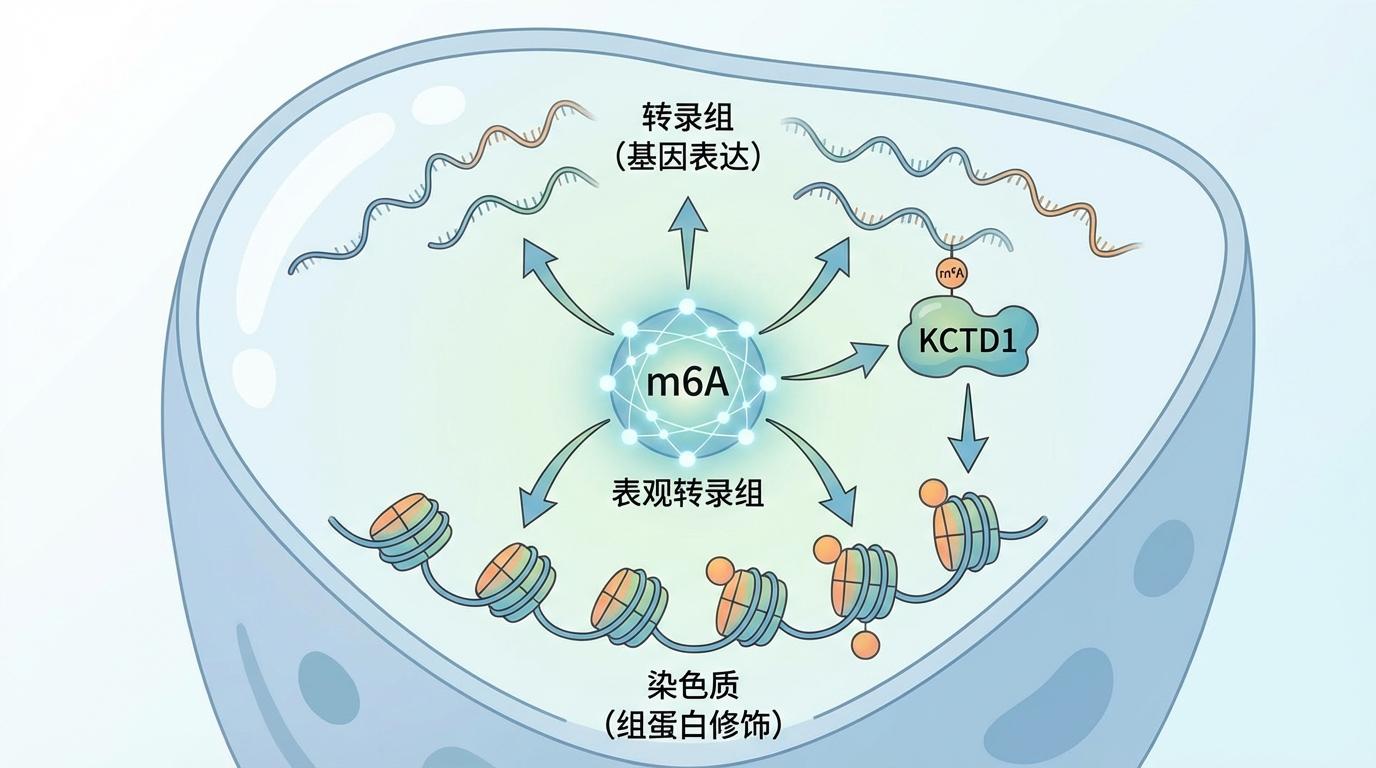
FOCAS技术的突破,其意义远不止于基础科学的认知深化,它为癌症治疗打开了一扇全新的大门。传统的癌症靶向药,大多针对的是基因突变或蛋白异常。而m6A修饰作为一种动态、可逆的调控机制,为药物干预提供了全新的靶点。
过去,针对m6A的药物开发思路主要是抑制全局性的“书写器”或“擦除器”蛋白,但这可能带来“杀敌一千,自损八百”的副作用。FOCAS的出现,使我们能够精准识别那些真正对癌细胞生死存亡起决定性作用的关键m6A位点。未来的癌症治疗,或许不再是笼统地抑制某个蛋白,而是开发出能够精准干扰特定m6A位点与其“阅读器”蛋白结合的药物,从而实现对癌细胞的“精准打击”,同时最大程度地减少对正常细胞的影响。
毫无疑问,FOCAS技术开启了一个m6A研究的黄金时代。然而,前方的道路依然充满挑战。这4475个功能性位点只是冰山一角,它们背后的具体分子机制、它们在真实肿瘤组织和患者体内的功能,以及如何将这些知识转化为安全有效的临床疗法,都是亟待解答的问题。
从一张模糊不清的地图,到如今拥有一幅高分辨率的导航图,我们对癌症基因表达调控的理解正在经历一场深刻的变革。FOCAS技术就像那支点亮黑暗的火炬,它不仅照亮了m6A这个长期被忽视的复杂世界,更为我们最终战胜癌症这一顽疾,指明了一条充满希望的精准之路。