
9 天前

9 天前
西非的雨夜,一只多乳鼠在村落的粮仓旁留下带毒的尿液——这是拉沙病毒最常见的传播起点。这种被列为生物安全四级的致命病毒,每年悄无声息夺走数千人的生命,却因为必须在最高等级实验室研究,让科学家们的抗病毒探索举步维艰。直到2026年4月,中国科学院武汉病毒研究所王薇团队的一篇论文,突然给这场僵局撕开了一道口子:他们不仅找到了病毒入侵人体的关键‘帮凶’,还证实一款已上市的抗癌老药,能精准卡住病毒的命门。为什么人类细胞里的普通蛋白,会成为病毒的致命帮凶?这款老药又如何完成跨界逆袭?
要研究拉沙病毒,必须进入像太空舱一样的P4实验室——穿正压防护服、呼吸靠外接氧气,每一个操作都要经过三重验证。为了绕开这个障碍,王薇团队先拿温和的模式病毒LCMV练手,这种病毒和拉沙病毒有着几乎一样的入侵逻辑。

他们给LCMV装上拉沙病毒的‘表面钥匙’GP蛋白,让它模拟致命病毒的入侵过程。通过磷酸化抗体芯片筛选,团队发现:病毒一接触细胞,人类细胞里的Src家族激酶就像接收到指令的内应,瞬间活跃起来。
你可以把Src家族激酶想象成细胞里的‘信号开关’——平时负责调节细胞的生长、迁移,一旦被激活,就会启动一连串的细胞反应。团队用RNA干扰技术逐个‘关掉’这些开关,结果发现,只有Fyn和Lyn这两个开关被关掉时,病毒的入侵、复制和释放全被卡住了:病毒基因组没法进入细胞,蛋白合成彻底停滞,连子代病毒都没法释放。而关掉其他激酶,病毒照样畅行无阻。
免疫沉淀实验更直接:病毒一靠近,Fyn和Lyn就会发生酪氨酸磷酸化——相当于被病毒直接按动了激活按钮。进一步研究证实,这两个激酶只在病毒入侵的早期阶段起作用,负责调控病毒的内吞和膜融合,就像给病毒打开了细胞的‘后门’,等病毒进入细胞开始复制后,它们就功成身退了。
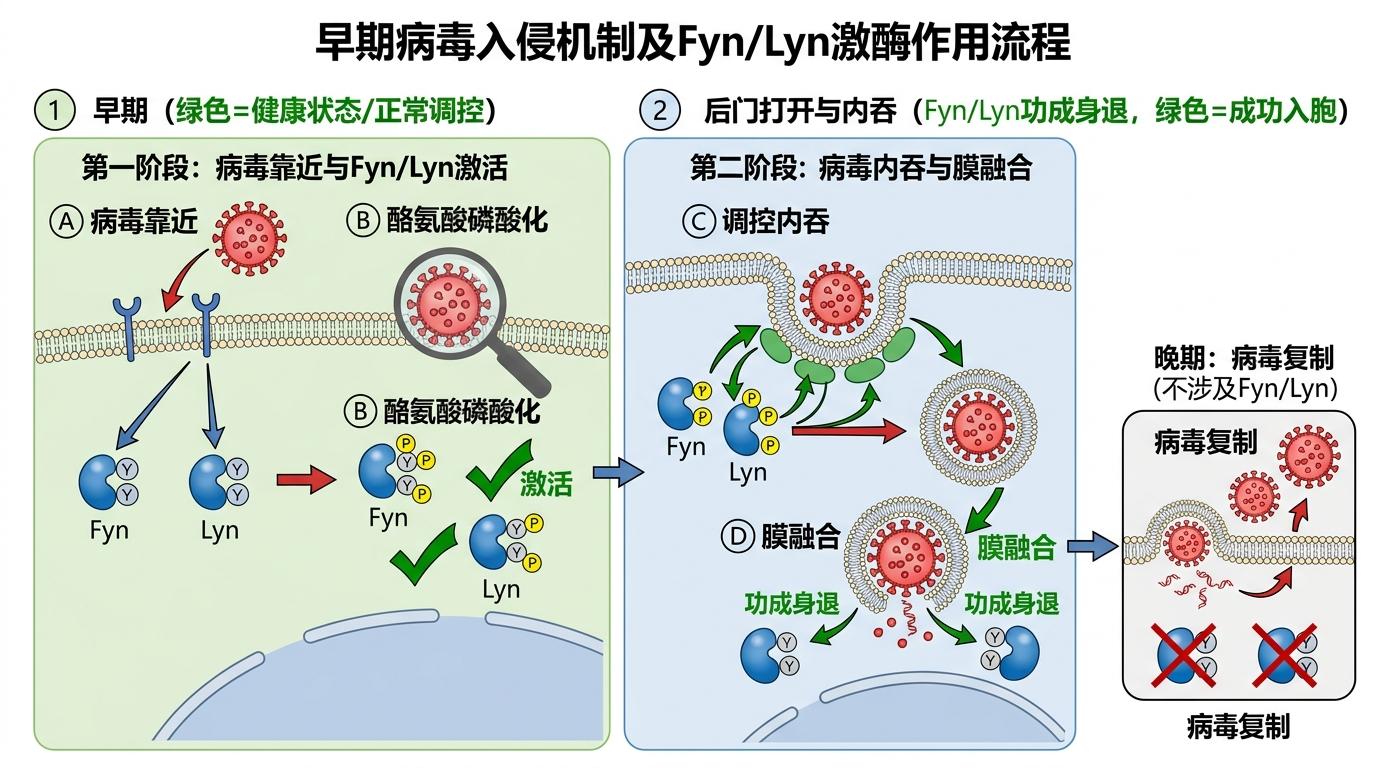
既然找到了病毒的关键内应,接下来就是找能锁住这个内应的‘手铐’。团队把目光投向了已经上市的Src激酶抑制剂塞卡替尼——原本这款药是用来治疗癌症的,通过抑制激酶活性阻止肿瘤细胞增殖。
细胞实验显示,塞卡替尼能以剂量依赖的方式抑制LCMV不同毒株,甚至在P4实验室里用活的拉沙病毒测试,也能高效阻断感染,半抑制浓度IC50在11-14μM之间,这个浓度对细胞的毒性极低。小鼠实验更让人振奋:给感染病毒的小鼠注射塞卡替尼后,脾脏和肝脏里的病毒载量大幅下降,原本会出现的组织病理损伤也明显减轻。
这不是偶然的跨界。塞卡替尼的作用原理,就是精准抑制Fyn和Lyn的激酶活性——相当于把病毒的‘内应’给绑了起来,让它们没法给病毒开门。更重要的是,这款药已经通过了临床安全性验证,不需要从零开始做毒理实验,能大大缩短抗病毒药物的研发周期。
不过,研究也留下了需要警惕的细节:Fyn和Lyn不仅是病毒的内应,也是人体免疫细胞的关键调控者——它们在浆细胞样树突状细胞里负责启动干扰素的产生,帮人体对抗病毒。如果过度抑制,可能会削弱人体自身的免疫反应。这意味着未来的临床应用,必须精准控制剂量,在阻断病毒和保留免疫功能之间找到平衡。
Fyn和Lyn的故事,其实是一场病毒和宿主的攻防拉锯战。
在正常情况下,这两个激酶是人体免疫系统的‘哨兵’:它们在浆细胞样树突状细胞里保持着基础激活状态,一旦发现病毒核酸,就会启动TLR信号通路,诱导大量干扰素产生,召唤免疫细胞来清除病毒。但狡猾的拉沙病毒,恰好利用了它们的激活机制——病毒的GP蛋白能直接触发这两个激酶的磷酸化,把原本用来防御的信号通路,变成了自己入侵的‘绿色通道’。
这也解释了为什么拉沙病毒能实现免疫逃逸:它一边利用激酶打开细胞大门,一边通过自身的NP蛋白降解宿主的双链RNA,抑制干扰素的产生,相当于一边闯门,一边把警报器给拆了。
这种双重角色,给药物研发带来了挑战:如果只是单纯抑制Fyn和Lyn,虽然能阻断病毒入侵,但也可能削弱人体的免疫防御。未来的方向,或许不是完全抑制,而是‘精准调控’——比如只阻断病毒利用激酶的那部分功能,保留它们激活免疫的作用。
当我们谈论抗病毒药物时,总在寻找能直接杀死病毒的‘魔法子弹’,但拉沙病毒的故事告诉我们:有时候最有效的武器,藏在病毒和宿主的互动里。
王薇团队的研究,不仅找到了拉沙病毒的致命弱点,更验证了‘老药新用’的潜力——在突发公共卫生事件面前,这种基于宿主靶点的药物再利用,可能是最快的应对方案。毕竟,我们和病毒的战争,从来不是简单的你死我活,而是一场关于利用与反利用的博弈。
病毒借宿主的手入侵,我们借宿主的盾防御。 这或许是人类对抗致命病毒最朴素,也最有效的逻辑。
点击充电,成为大圆镜下一个视频选题!