对抗知识焦虑,从看懂这条开始
App 下载
巨噬细胞“过度翻译”:炎症风暴背后的真凶?
炎症风暴|巨噬细胞|细胞因子释放综合征|CAR-T细胞治疗|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
炎症风暴|巨噬细胞|细胞因子释放综合征|CAR-T细胞治疗|肿瘤学|医学健康
当癌症的阴霾笼罩,免疫疗法如CAR-T细胞治疗,曾被视为一道划破绝望的曙光。它赋予患者自身的T细胞以精准识别并歼灭癌细胞的能力,让无数生命得以重燃希望。然而,这道光芒背后,却常常潜藏着一道致命的暗影——细胞因子风暴,医学上称之为细胞因子释放综合征(CRS)。它像一场突如其来的海啸,让免疫系统失去控制,以“玉石俱焚”的方式,在清除病灶的同时,也可能危及生命,导致多器官衰竭。高达50%至90%的CAR-T治疗患者,都曾与这场风暴擦肩而过。长久以来,科学家们都在追问:究竟是什么点燃了这场失控的炎症之火?
就在2025年12月31日,一个振奋人心的答案浮出水面。西湖大学医学院胡小玉团队与解放军总医院韩为东团队(清华大学刘倖衔博士、博士生李佳琦为论文第一作者)合作,在《细胞》子刊《Cell Reports Medicine》上发表了一项突破性研究。他们发现,单核细胞/巨噬细胞的“过度翻译”(Monocyte/macrophage hyper-translation, MHT)正是驱动细胞因子释放综合征(CRS)的核心机制。这一发现不仅揭示了炎症失控的全新病理学特征,更为干预CRS开辟了一条前所未有的治疗路径。
这项研究的核心在于指出,在CRS患者样本中,单核细胞和巨噬细胞存在显著的“过度翻译”现象。这意味着,即便基因指令(mRNA)的转录正常,这些细胞内的蛋白质合成机器却异常活跃,超量制造促炎细胞因子,特别是臭名昭著的白细胞介素-6(IL-6),最终引爆了那场毁灭性的细胞因子风暴。此前,胡小玉团队与韩为东团队在2023年8月16日《Journal of Experimental Medicine》上发表的研究中,就曾发现常用心血管药物美托洛尔能通过抑制IL-6的蛋白质翻译来缓解CAR-T引发的CRS,这为此次更深层次的机制探索奠定了基础。
炎症,本是生命赖以生存的基本生理过程。它像一位忠诚的卫士,在机体发育、免疫防御、组织重塑和代谢适应等广泛生物功能中扮演着至关重要的角色。当组织遭遇外伤、感染或入侵时,炎症反应迅速启动,通过红肿、发热、疼痛等信号,调集免疫大军奔赴前线,清除病原体和受损细胞。在这个过程中,细胞因子扮演着“通讯员”的角色,它们是免疫细胞分泌的信号蛋白,负责协调免疫反应的强度和方向。
正常情况下,促炎细胞因子和抗炎细胞因子之间维持着精妙的平衡,确保炎症反应在完成任务后能及时“鸣金收兵”,避免对自身组织造成过度损伤。然而,一旦这种平衡被打破,促炎细胞因子大量且持续地释放,便会引发一场灾难性的“炎症风暴”——细胞因子释放综合征。在CAR-T治疗中,被激活的T细胞大量增殖并杀伤肿瘤细胞,同时释放出海量的细胞因子(如IL-1、IL-6、TNF-α、IFN-γ等),这些细胞因子反过来又会激活单核细胞、巨噬细胞等其他免疫细胞,形成一个恶性正反馈循环,导致全身性炎症反应,表现为高热、低血压、呼吸困难、多器官功能障碍,甚至危及生命。
长期以来,科学界在探索炎症调控机制时,焦点主要集中在基因转录层面——即如何控制基因“抄写”出mRNA指令。人们普遍认为,编码炎症介质的mRNA的转录速率是决定炎症反应强弱的“限速步骤”。然而,此次胡小玉团队的研究却将目光投向了基因表达的另一个关键环节:翻译。翻译是mRNA指令在核糖体上被“解读”并合成蛋白质的过程。这个过程对细胞而言,是巨大的能量消耗者,几乎占据哺乳动物细胞总能量消耗的一半。这种资源密集性强烈暗示,翻译并非一个被动的执行者,它可能与转录协同作用,作为炎症反应中一个积极受调控的“检查点”。
这项研究首次明确指出,在细胞因子风暴中,单核细胞/巨噬细胞的异常活跃并非源于mRNA指令的增多,而是这些指令被“过度翻译”成了过量的蛋白质。就好比工厂里收到的订单数量正常,但生产线却以超负荷的速度,不计后果地生产出远超需求的商品,最终导致市场(机体)混乱。这一“过度翻译”的视角,颠覆了我们对炎症调控的传统认知,揭示了炎症失控背后一个此前被低估的关键环节。
为了解开“过度翻译”背后的分子密码,研究团队运用CRISPR筛选技术,精准定位了关键调控因子——BCAP。BCAP,全称为B细胞PI3K衔接蛋白,此前已知其在免疫细胞信号传导中扮演重要角色,能将Toll样受体(TLR)信号与PI3K激活联系起来,并影响巨噬细胞的代谢重编程。但它在炎症过度翻译中的具体作用,却是首次被揭示。
研究发现,BCAP如同一个“启动器”,它激活了RSK-EIF4B信号轴。RSK(核糖体S6激酶)家族是一组重要的丝氨酸/苏氨酸激酶,作为Ras/Raf/MEK/ERK信号通路的下游效应子,广泛参与细胞生长、运动、存活和增殖等过程。而eIF4B(真核翻译起始因子4B)则是翻译起始复合体eIF4F的关键辅助因子,直接参与mRNA在核糖体上的定位和蛋白质合成效率的调控。当BCAP激活RSK-EIF4B轴时,这个通路就如同被拧开了水龙头,导致巨噬细胞内的翻译机器火力全开,超负荷运转,合成并释放出大量的促炎细胞因子,特别是IL-6,从而点燃了细胞因子风暴。此前的研究也曾发现RSK对eIF4B的磷酸化可增加其活性,从而促进翻译和蛋白质合成,这与本次研究的发现不谋而合。
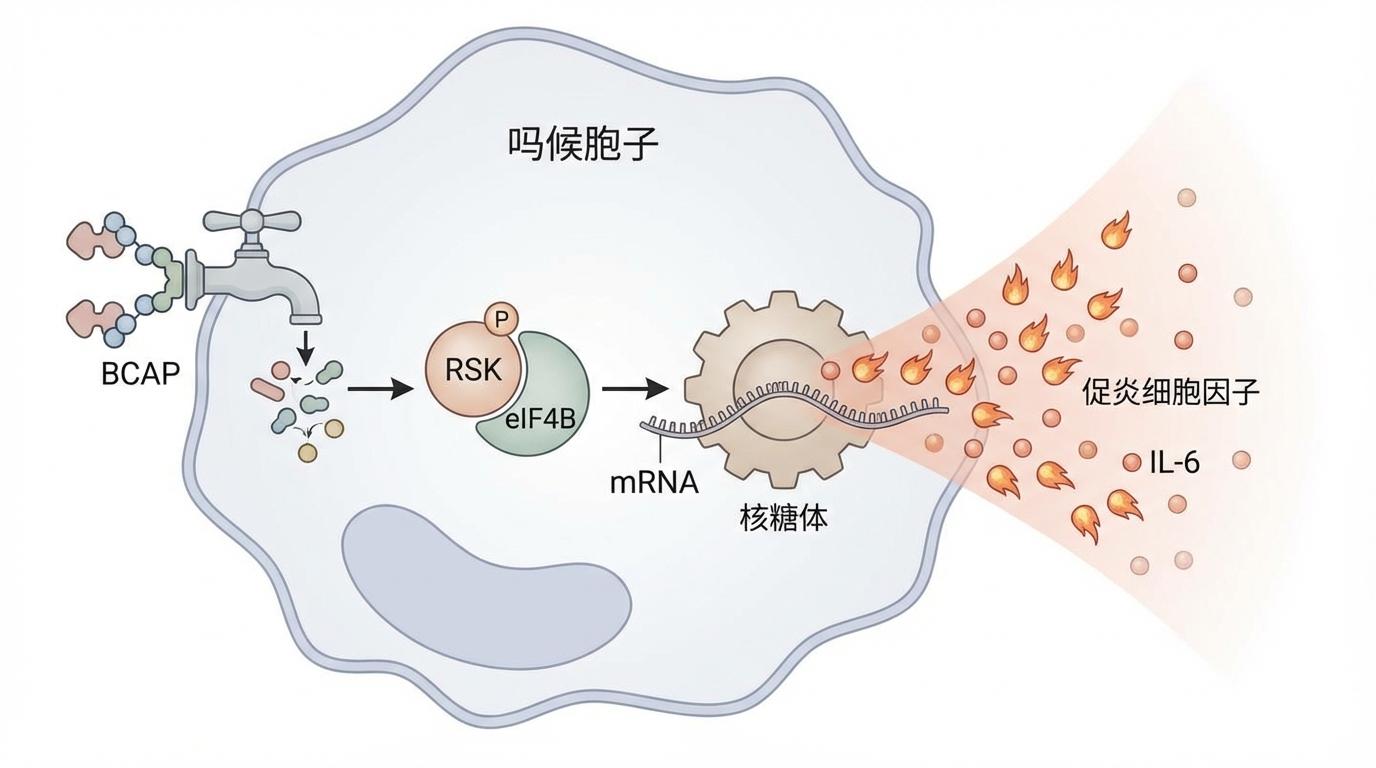
此次对BCAP-RSK-EIF4B信号轴的揭示,为CRS及其他炎症性疾病的治疗带来了全新的策略。如果说过去我们主要通过“减少订单”(抑制转录)来控制炎症,那么现在,我们有了“调控生产线”(抑制翻译)的新工具。
研究团队通过实验证实了这一策略的有效性:当RSK基因被敲除时,CRS相关的炎症反应显著减轻;而通过药理学手段抑制RSK,例如使用RSK抑制剂LJH685,不仅在人源化小鼠模型中有效缓解了CRS症状,如发热和神经毒性,更重要的是,它并未影响CAR-T细胞的抗肿瘤活性。这表明,我们可以精准地“关闭”炎症的过度生产线,而不会“误伤”免疫疗法的核心功能。
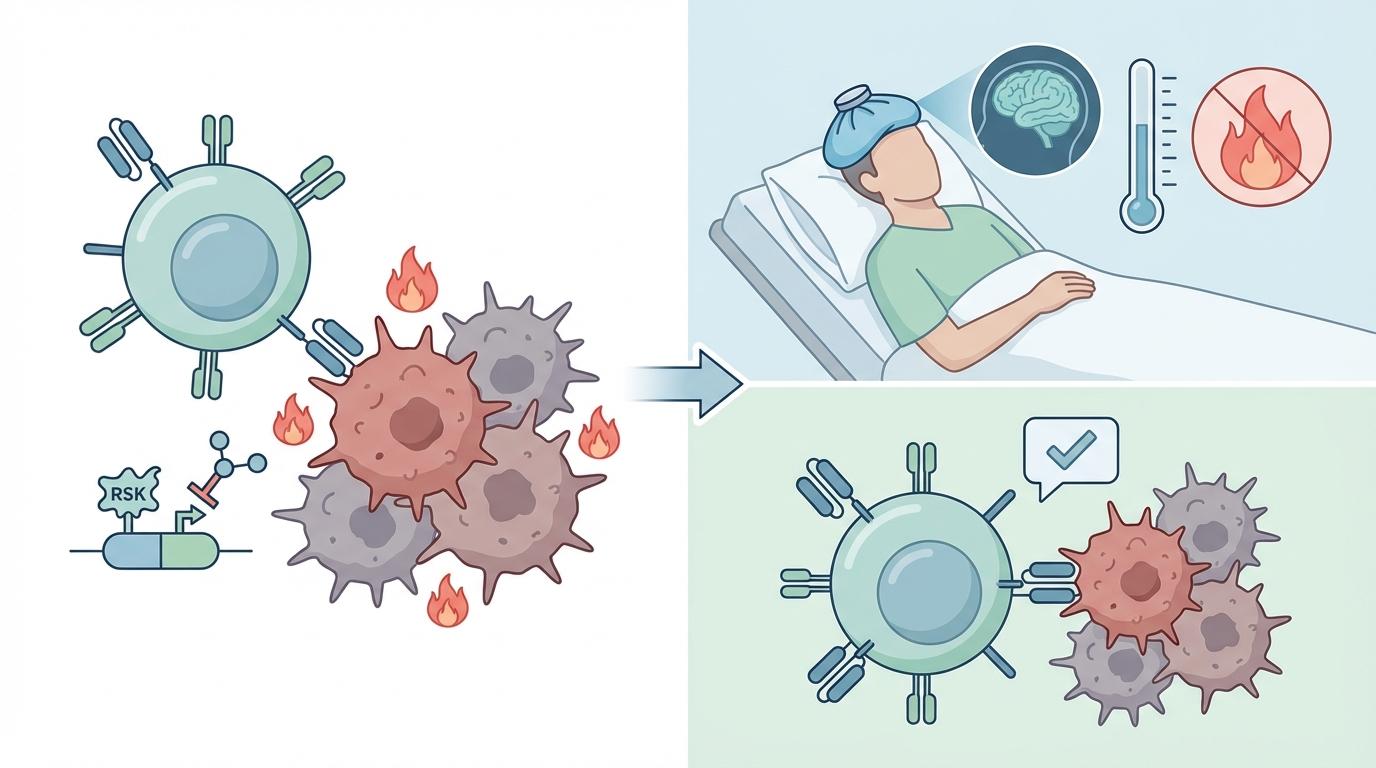
这一发现与胡小玉团队在2023年的另一项研究形成呼应。当时他们发现,美托洛尔通过加强eEF2K-eEF2信号轴介导的分子制动,抑制IL-6的翻译延伸效率,从而减少IL-6蛋白质的产生,缓解CRS。两次研究都指向了蛋白质翻译层面的调控,共同构筑了一个全新的炎症治疗靶点图景。这些成果不仅为CAR-T治疗的安全性提供了新的保障,也为多种炎症性疾病的干预开辟了广阔前景。RSK抑制剂,如LJH685和LJI308,此前已被证明能抑制衣原体感染,并与阿奇霉素有协同作用,这进一步验证了其作为潜在药物的价值。
靶向过度翻译的策略,如同在复杂而庞大的免疫调控网络中,找到了一把精巧的“调速器”。未来的炎症治疗,将不再仅仅停留在抑制炎症因子的产生或阻断其作用,而是可以更深入地干预蛋白质合成的微观层面。这一思路的拓展,预示着精准调控炎症的“新篇章”正在开启。
除了翻译水平的调控,对蛋白质翻译后修饰(PTM)的研究也正蓬勃发展。衣康酸化、S-羰基化、S-亚硝基化等多种PTM被发现能够精细地影响免疫细胞的激活与抑制,调节炎症介质的产生,成为潜在的药物靶点。例如,衣康酸及其衍生物能抑制NLRP3炎症小体激活,虾青素通过抑制STING羰基化增强抗病毒防御,这些都代表了更精细化的炎症干预方向。
此外,免疫治疗领域也在不断涌现新的策略:
全球抗炎治疗市场规模预计到2032年将达到数万亿元,其中抗炎生物制剂是增长最快的类别。这些新兴疗法和技术将共同推动炎症性疾病的治疗迈向更高效、更安全、更个性化的未来。
胡小玉和韩为东团队的这项研究,无疑为我们理解和对抗炎症失控打开了一扇新的窗户。它将我们对炎症的认识从宏观的“火力”强度,深入到微观的“生产线”调控,提供了一个全新的干预视角。对于CAR-T细胞治疗而言,这意味着未来或许能通过精准靶向巨噬细胞的过度翻译,在不削弱其抗肿瘤威力的前提下,大幅降低细胞因子风暴的风险,让更多患者安全地获得治愈的机会。
然而,科学的征途永无止境。尽管我们揭示了过度翻译的驱动作用,但其更深层次的调控网络,以及在不同炎症性疾病中的特异性表现,仍有待进一步探索。例如,BCAP如何精确激活RSK-EIF4B轴的分子细节,不同RSK亚型(如RSK1、RSK2、RSK4)在炎症中的具体角色,以及如何开发出更具特异性、更低毒性的翻译抑制剂,都是未来需要攻克的难题。此外,翻译过程的巨大能量消耗,是否也为代谢干预提供了新的机会?这些未解之谜,正等待着全球科学家们去逐一破解。这场关于炎症的“翻译”革命,才刚刚开始,它预示着一个更加精准、更加安全的免疫治疗新时代的到来。