内容由AI生成,思考得你完成
App 下载
内容由AI生成,思考得你完成
App 下载
随着岁月流转,我们的身体会发出一些微妙的信号:步伐不再像年轻时那般稳健,反应似乎慢了半拍,手脚偶尔会感到麻木。这些看似寻常的衰老现象,背后可能隐藏着一场发生在中枢神经系统内部的“线路老化”危机。我们的神经系统,如同一张遍布全身的超高速信息网络,而脊髓,正是连接大脑与身体的“信号主干线”。这条主干线的畅通,依赖于包裹在神经纤维外的“绝缘层”——髓鞘。
髓鞘如同电线外的塑料包皮,确保神经信号能够高速、精准地跳跃式传递。一旦这层绝缘层变薄、松动甚至脱落,信号传输就会“漏电”或“短路”,导致动作迟缓、感觉异常。长期以来,我们笼统地将这些变化归因于衰老。但一个更深层的问题是:在这条漫长的“信号主干线”上,是否存在某些特别脆弱的“路段”?其维护机制又有何不同?最近,一项突破性研究为我们揭开了冰山一角,指向了一个令人惊讶的发现:我们体内的免疫系统,在这场关于衰老与守护的博弈中,扮演着一个出人意料的双面角色。
这场探索始于瑞典卡罗林斯卡医学院。研究团队在国际顶尖期刊 《自然·神经科学》(Nature Neuroscience) 上发表了一项研究成果,将目光精准地投向了衰老过程中小鼠的脊髓。通过高精度的透射电子显微镜,他们发现了一个令人不安的规律:并非所有区域的髓鞘都以相同的速度老化。脊髓中一个名为 “背柱” 的特定区域,其髓鞘在衰老过程中显得异常脆弱,更容易发生“松散老化”等结构性破坏。

脊髓背柱,是传递触觉、振动感和身体位置感等精细感觉信息的关键上行通路。它的脆弱性意味着,随着年龄增长,我们感知世界的能力可能会从这个“薄弱环节”开始衰退。这一发现首次揭示了神经系统衰老的区域特异性,它不仅是一个普遍的过程,更像是一场有着明确“主攻方向”的精准打击。那么,是什么让脊髓背柱成为了一个如此特殊的“靶点”?答案,出人意料地指向了驻扎在此地的“免疫哨兵”。
在中枢神经系统的广袤疆域里,小胶质细胞 扮演着“免疫哨兵”的角色。它们时刻保持警惕,巡视着神经元和髓鞘的健康状况,一旦发现损伤或入侵者,便会立即被激活,清除有害物质,修复组织。它们是神经系统不可或缺的守护者。
然而,守护与毁灭,往往只有一线之隔。小胶质细胞的激活必须受到极其精密的调控,如同训练有素的特种部队,行动必须精准、适度。一旦这种调控失衡,过度激活的“哨兵”就会从守护者变为破坏者,释放大量炎症因子,“无差别”攻击健康的神经组织,加剧多种神经退行性疾病的病理进程。研究人员在脆弱的脊髓背柱区域,恰恰发现了这些“哨兵”的异常动态:它们在衰老过程中呈现出一种特殊的 “预激活” 状态,仿佛时刻处于一触即发的临界点。
为了维持平衡,神经系统为小胶质细胞配备了一套“免疫刹车”系统。其中,一种名为 TGF-β 的信号分子扮演了核心角色。它能有效抑制小胶质细胞的过度激活,防止免疫反应失控。按理说,在衰老脊髓背柱这个“高危区域”,这套刹车系统应该全力工作。研究也证实了这一点:该区域的小胶质细胞确实在衰老时大量分泌TGF-β,试图踩住刹车,维持一种脆弱的平衡。这是一种被称为 “炎症性衰老”(inflammaging) 的适应状态——身体在低度炎症和免疫抑制之间艰难地走着钢丝。
然而,最令人震惊的发现来自于一个大胆的实验。研究人员通过基因技术,在小鼠中人为地“松开”了这道免疫刹车——特异性地阻断了小胶质细胞的TGF-β信号。结果是灾难性的。刹车一旦失灵,脊髓背柱区域的小胶质细胞瞬间“暴走”。它们不再是守护者,而是变成了一群失控的吞噬者,对周围的髓鞘发起了猛烈攻击。大面积的髓鞘被剥离、吞噬,实验小鼠迅速出现严重的神经功能障碍,从步态不稳、肌力减弱,一步步走向四肢瘫痪。
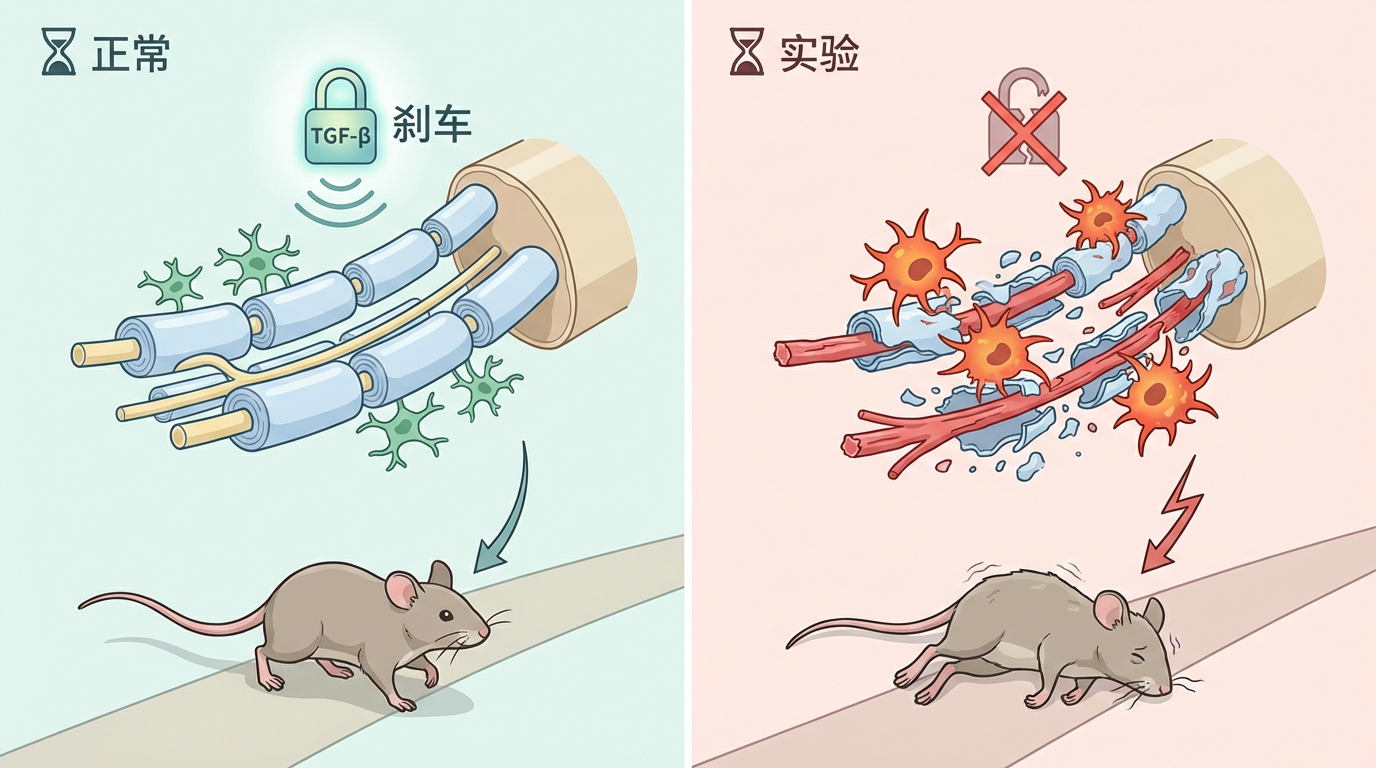
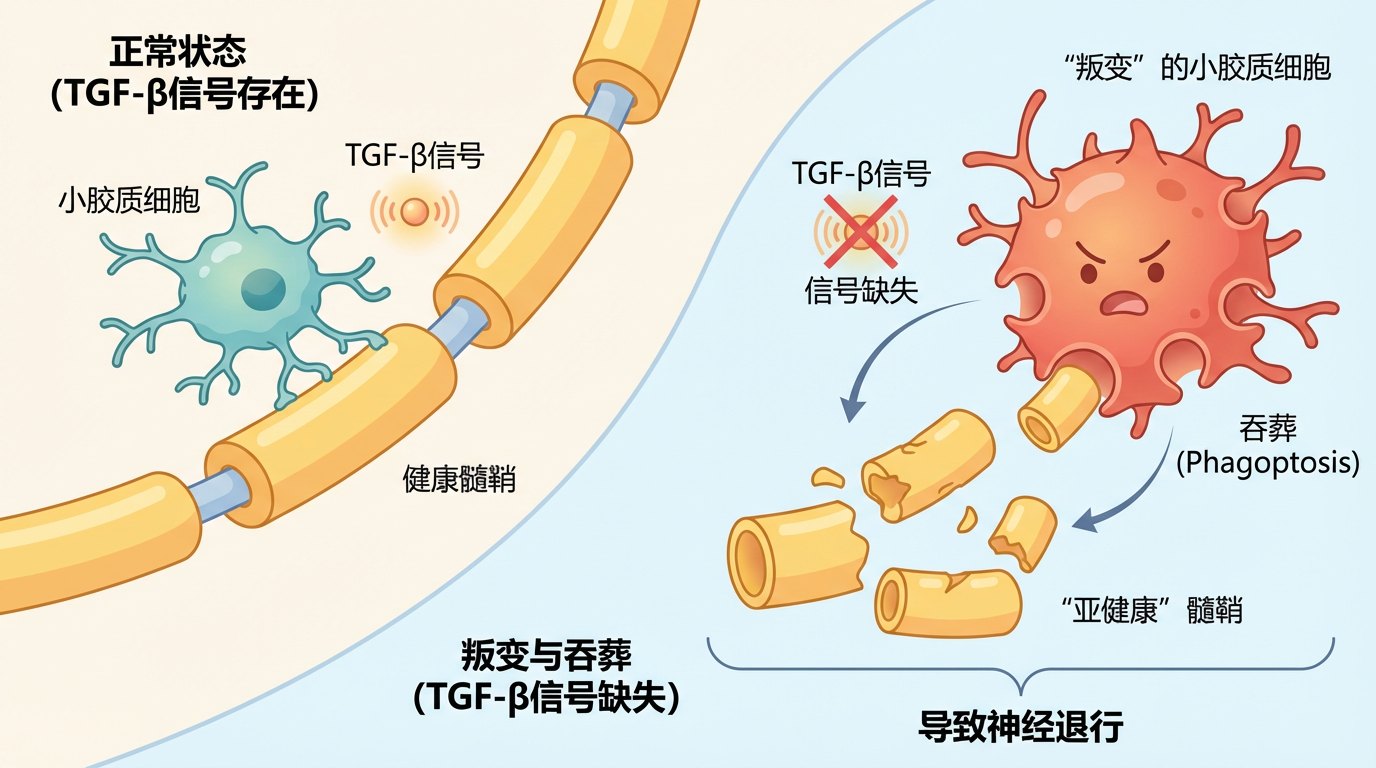
通过单细胞测序,科学家们精准定位了这群“叛变”的细胞亚群。在TGF-β信号缺失后,一类具有极强吞噬能力和炎症反应的特殊小胶质细胞被诱导产生。它们疯狂吞噬那些仅仅是“亚健康”但仍可存活的髓鞘。这一过程与近年来提出的 “吞葬”(phagoptosis) 概念不谋而合,即免疫细胞的主动性、攻击性吞噬行为,是导致神经退行的重要元凶。
这项研究还揭示了一个与临床观察高度相关的现象:在“免疫刹车”失灵后,雌性小鼠的疾病进展比雄性小鼠严重得多。这一发现为理解多发性硬化(MS)和视神经脊髓炎(NMO)等自身免疫性脱髓鞘疾病为何在女性中发病率更高,提供了强有力的机制解释。
这提示我们,在这些疾病的背后,可能存在着由性别决定的不同免疫调控模式。女性患者体内的免疫系统或许对TGF-β这套“刹车系统”的依赖性更强,或是在某些因素影响下更容易出现刹车失灵。未来的治疗策略,必须充分考虑到这种性别差异,开发更具针对性的个体化防治方案。
这项研究的意义远不止于揭示衰老的又一个秘密。它为神经退行性疾病的治疗打开了一扇全新的大门。复旦大学附属华山医院的全超主任医师评论道,这一发现为理解MS等疾病为何好发于脊髓后索(即背柱)提供了关键线索,并为临床诊疗带来三大启示:
从“广泛抑制”到“精准调控”:传统的治疗方法多为广泛抑制整个免疫系统,副作用大且效果有限。新发现提示,未来的策略应该是精准地调节免疫平衡,例如,通过药物增强TGF-β信号通路的“刹车”功能,或者靶向性地抑制那群过度吞噬的“叛变”小胶质细胞亚群。
重视性别差异化治疗:既然性别在疾病模型中表现出显著差异,那么临床上就应为女性患者制定更具针对性的预防和治疗策略,这可能是提高疗效的关键。
强调早期干预:在髓鞘损伤和小胶质细胞保护性适应尚处于脆弱平衡的“炎症性衰老”阶段进行干预,可能以最小的代价,最大程度地保护神经功能,防止其滑向不可逆的损伤深渊。
这项研究如同一束光,照亮了衰老与神经退行性疾病中一个被长期忽视的角落。它告诉我们,衰老并非简单的线性衰退,而是一场复杂、动态的平衡之舞。我们的免疫系统,在漫长的生命历程中,不断进行着适应与调整。TGF-β信号,正是这场舞蹈中维持平衡的关键舞步。
当舞步精准、节奏和谐时,免疫系统是髓鞘最忠实的守护者。然而,当平衡被打破,刹车失灵,守护者便会瞬间反噬,成为最凶猛的破坏者。理解并学会如何调控这场精妙的平衡之舞,不仅将重塑我们对衰老的认知,更将为全球数以千万计的神经退行性疾病患者,带来精准治疗的希望,让他们有机会在生命的乐章中,跳出更长久、更稳健的舞步。