
2 个月前

2 个月前
晚育,已成为现代社会的常态。当人们为事业、为生活奔波,将组建家庭的计划一再推迟时,一个关乎代际健康的谜题也随之浮现:为何高龄父亲的后代,出现代谢紊乱、自闭症、精神分裂症等健康问题的风险会显著增加?传统观点将矛头指向精子中累积的DNA损伤,但这似乎并未完全解开谜团。仿佛有一份更隐秘的“父代密码”在传递着岁月的信息,而我们此前一直未能破译。
近年来,科学家们将目光投向了精子中一群曾被忽视的信使——小非编码RNA(sncRNA)。它们不编码蛋白质,却像精密的分子开关,调控着基因的表达。然而,这些RNA分子身上布满了复杂的化学修饰,如同给信件加了密,让传统测序技术难以读取。父亲年龄的秘密,似乎就藏在这片充满迷雾的分子世界中。
直到一项名为**PANDORA-seq**的革命性测序技术问世,迷雾才开始散去。这项由研究团队自主研发的技术,如同一把万能钥匙,能够“解锁”RNA上的化学修饰,让那些曾经“隐身”的大量tsRNA(tRNA衍生小RNA)和rsRNA(rRNA衍生小RNA)首次完整地呈现在科学家面前。
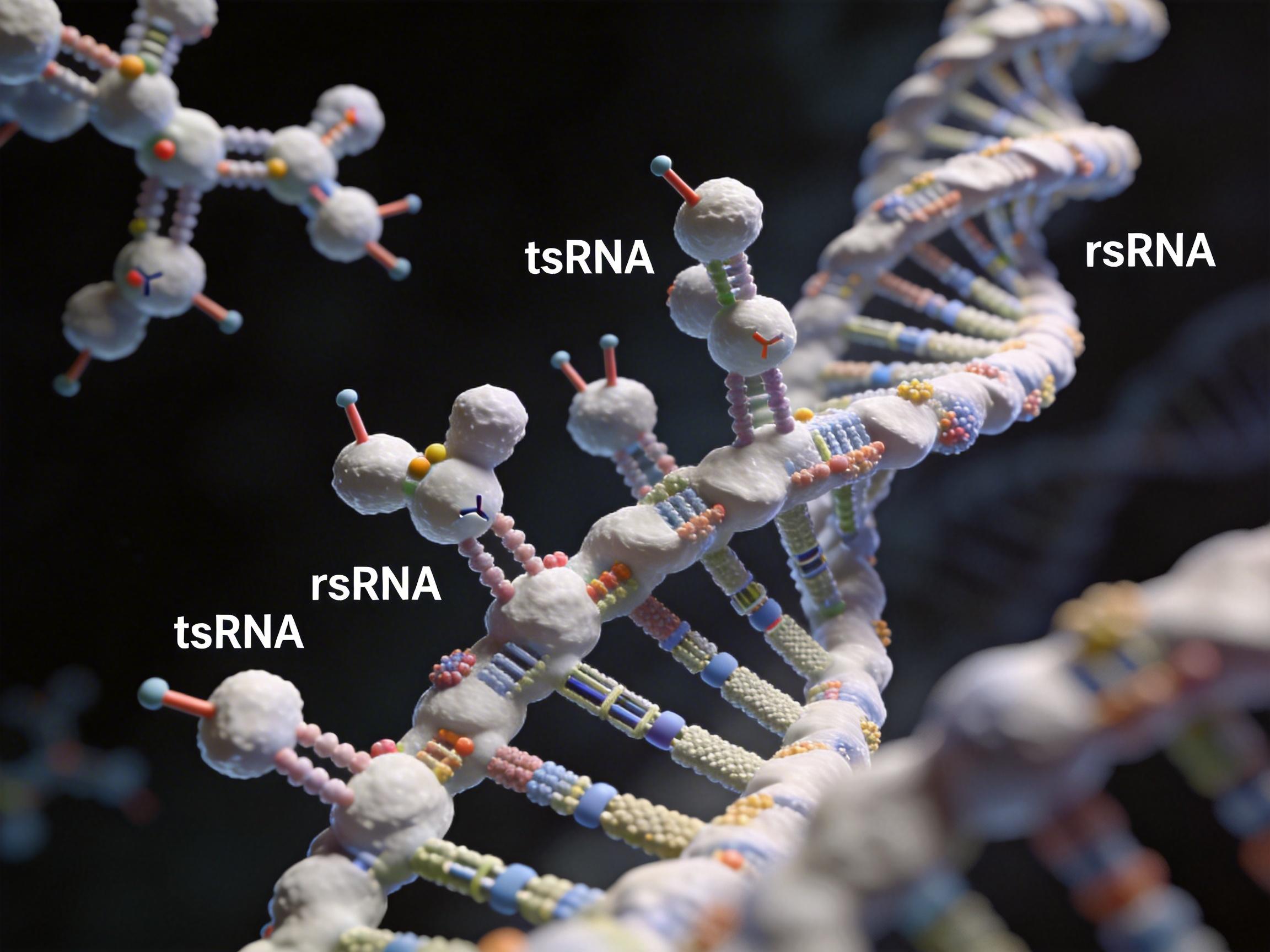
借助这把钥匙,一项发表于《The EMBO Journal》的研究,对小鼠和人类的精子进行了一场贯穿生命周期的深度探索。研究人员系统分析了从10周龄到90周龄(相当于人类从青春期到老年)小鼠的精子,试图绘制一幅前所未有的精子衰老分子图谱。他们发现的,远不止是平缓的线性变化。
研究结果令人震惊。在小鼠生命历程中,精子RNA的图谱并非平稳地老化,而是在50至70周龄之间(约等于人类40至50岁的中年阶段)出现了一个剧烈的“断崖式”转变。tsRNA和rsRNA的整体组成在这一时期发生了彻底重塑,清晰地划分出早期衰老与晚期衰老的界限。这个“衰老悬崖”的存在,是传统测序方法从未捕捉到的惊人景象。
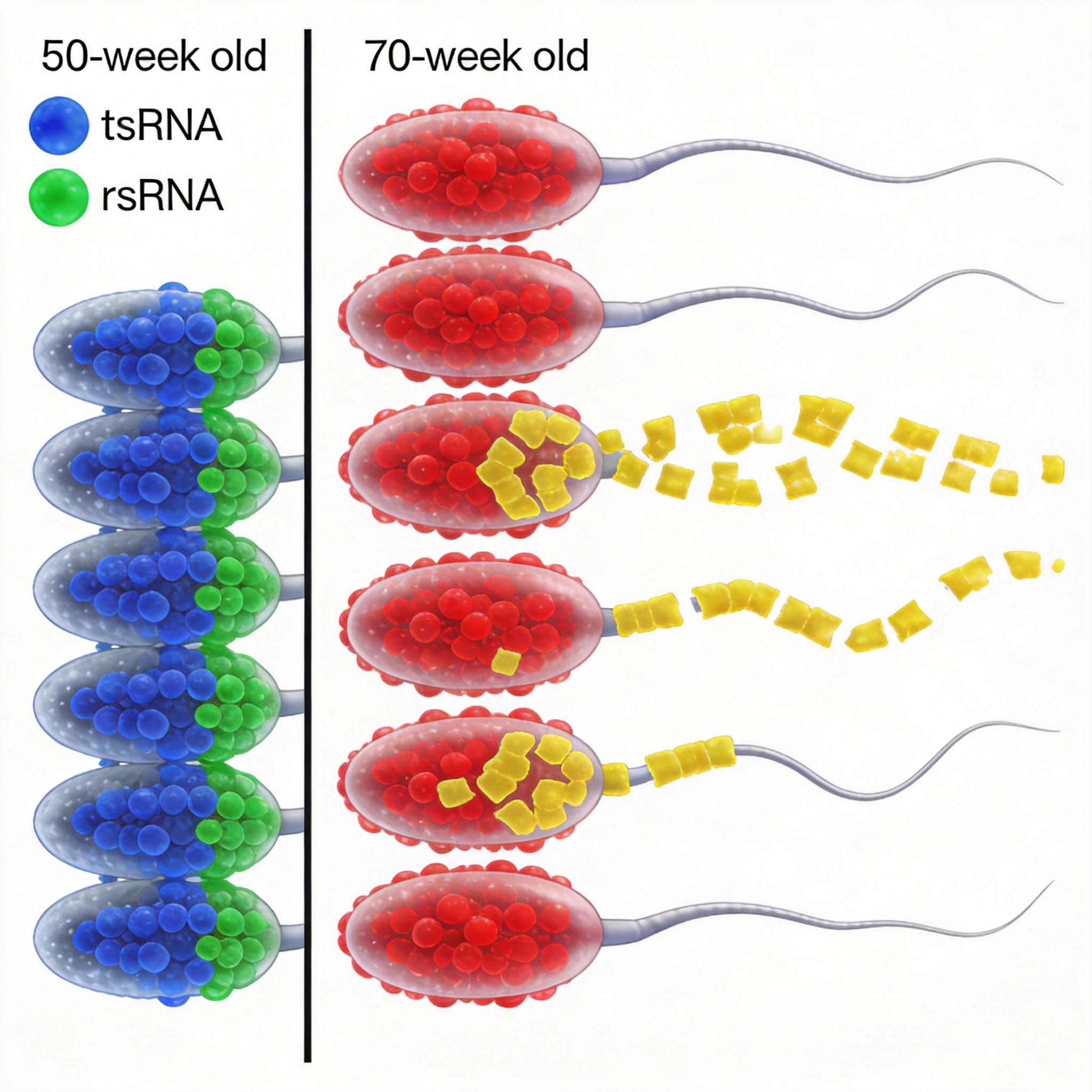
更深入的分析揭示了一个更精妙、更具普遍性的规律。当研究人员将目光聚焦于真正传递遗传物质的精子头部时,一个与年龄高度相关的线性变化浮出水面:
这种“越老越长”的趋势,如同一个在精子内部悄然走动的分子时钟。为了验证这是否是生命共通的规律,团队分析了两个独立的人类精子队列。结果完美复现了小鼠中的发现——人类精子头部的rsRNA也遵循着完全相同的长度变化模式。这表明,rsRNA长度的漂移,是哺乳动物精子衰老过程中一个进化上高度保守的分子特征。
这些变化的RNA分子,仅仅是衰老的标记,还是会主动影响下一代?这是解开整个谜题的关键。为了回答这个问题,研究团队在实验室中进行了一项巧妙的功能验证实验。
他们人工合成了两组分别模拟“年轻”和“年老”精子RNA特征的sncRNA混合物,并将其导入小鼠胚胎干细胞中——这些细胞在某种程度上代表了生命的最初阶段。结果清晰地显示:“年老”的RNA组合显著改变了胚胎干细胞的基因表达网络。被激活或抑制的基因通路,精准地指向了:
这些变化与现实世界中高龄父亲后代所表现出的代谢和神经系统健康风险高度吻合。这强有力地证明,衰老精子中特定sncRNA图谱的变化,具备了重编程早期胚胎基因表达、并潜在影响后代一生的健康轨迹的能力。它们不只是时间的记录者,更是跨代信息的传递者和执行者。
这项研究的意义远不止于揭示了一个深刻的生物学机制。它为我们提供了一扇观察和干预父系衰老遗传效应的全新窗口。
首先,rsRNA长度变化这一稳定、保守的生物标志物,有望被开发为评估男性精子“年龄”和生育质量的新型临床检测工具。这对于面临生育抉择的高龄男性及其家庭而言,将提供前所未有的科学依据。
更重要的是,它指明了潜在的干预方向。既然我们知道了衰老的分子密码,那么能否改写它?未来的研究将致力于寻找驱动这些RNA变化的“上游开关”,例如累积的氧化应激或特定的RNA加工酶。一旦找到这些靶点,就有可能通过药物或生活方式干预,延缓甚至部分逆转精子的“RNA衰老”,从而降低高龄父亲给后代带来的健康风险。
从一个普遍的社会现象,到一组隐藏在精子头部的RNA分子,科学的探索为我们揭示了生命传承中一条精妙而隐秘的通路。它告诉我们,父亲传递给孩子的,远不止于DNA序列,还有他生命历程中积累的时光印记。而理解并干预这条通路,正为促进更健康的跨代传承带来新的曙光。
点击充电,成为大圆镜下一个视频选题!