对抗知识焦虑,从看懂这条开始
App 下载
胰腺癌的隐秘共谋:表观遗传如何驯化免疫系统
清华大学|上海交通大学仁济医院|免疫细胞驯化|表观遗传失调|胰腺癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
清华大学|上海交通大学仁济医院|免疫细胞驯化|表观遗传失调|胰腺癌|肿瘤学|医学健康
你或许听过“癌王”胰腺癌的恐怖:5年生存率不到10%,超过80%的患者确诊时已到晚期,连最热门的免疫疗法都对它束手无策。医生们曾以为,是癌细胞的基因突变太顽固,才让治疗屡屡失效。直到最近,上海交通大学仁济医院薛婧团队与清华大学陈默团队的联合研究,撕开了“癌王”的另一层伪装——真正让胰腺癌在体内横行无阻的,可能不是基因本身,而是一种能“改写基因使用手册”的机制:表观遗传失调。它不仅操控癌细胞的恶性生长,还能悄悄驯化肿瘤周围的免疫细胞和基质细胞,把整个身体变成癌细胞的“后勤基地”。为什么这种看不见的调控,会比基因突变更难对付?
你可以把细胞的基因组想象成一本厚厚的菜谱——每个基因都是一道菜的配方,而表观遗传就是决定“哪些菜能被端上桌”的厨师。它不改变菜谱上的文字(也就是基因序列),却能通过给某些配方盖上“禁止使用”的印章(比如DNA甲基化),或者给某些配方贴上“重点推荐”的标签(比如组蛋白乙酰化),直接控制细胞能合成哪些蛋白质。
在胰腺癌中,这本“菜谱”的编辑权彻底乱了套:高达97%的患者体内,负责表观遗传的调控因子出现了突变。比如ARID1A基因,它本是负责“解锁”抑癌基因的钥匙,突变后却成了“锁死”抑癌基因的枷锁;再比如KDM6A基因,它本该清除“促进癌细胞转移”的标签,缺失后却让癌细胞的侵袭性翻倍。
更棘手的是,这些“隐形编辑”还会看时机下菜——同一个调控因子,在肿瘤早期可能帮着癌细胞躲避免疫系统,到了晚期却转而帮着癌细胞耐药。这种“见风使舵”的时空特异性,让传统的靶向治疗彻底扑空。
如果说表观遗传失调是癌细胞的“内部政变”,那它对肿瘤微环境的操控,就是一场精准的“统战”。癌细胞不仅自己改头换面,还能通过表观遗传信号,给周围的细胞“洗脑”:
它会给免疫抑制性髓系细胞发“邀请函”——通过异常分泌细胞因子,把这些本应攻击癌细胞的“警察”,变成保护癌细胞的“保镖”,还会压低癌细胞表面的“通缉令”(MHC分子),让免疫细胞彻底认不出敌人;它还会给癌症相关成纤维细胞(CAF)“分配工作”——把这些本应维持组织稳定的“建筑工人”,改造成专门给癌细胞提供营养的“后勤兵”,甚至让一部分CAF变成“燃料库”,储存脂质供癌细胞随时取用。
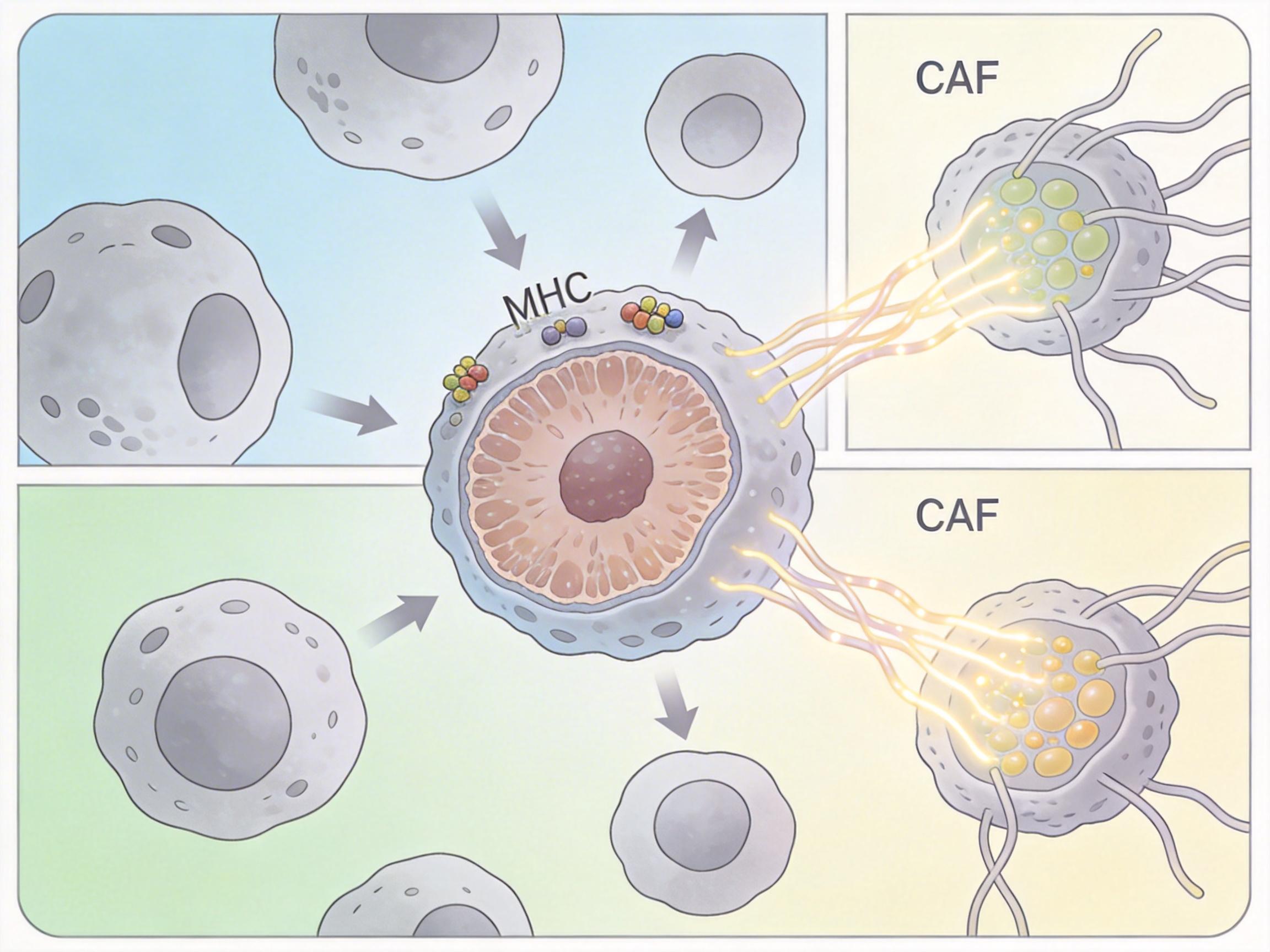
最可怕的是,这种“统战”是双向的:肿瘤微环境里的代谢压力(比如乳酸堆积、谷氨酰胺匮乏),又会反过来加剧癌细胞的表观遗传失调。就像一个恶性循环的闭环:癌细胞越强大,微环境越“友好”;微环境越“友好”,癌细胞越嚣张。
举个直观的例子:当胰腺癌组织里的乳酸浓度升高,会直接给癌细胞的组蛋白贴上“促进耐药”的标签,让化疗药物彻底失效。这也是为什么胰腺癌对传统化疗的响应率不到20%的核心原因之一。
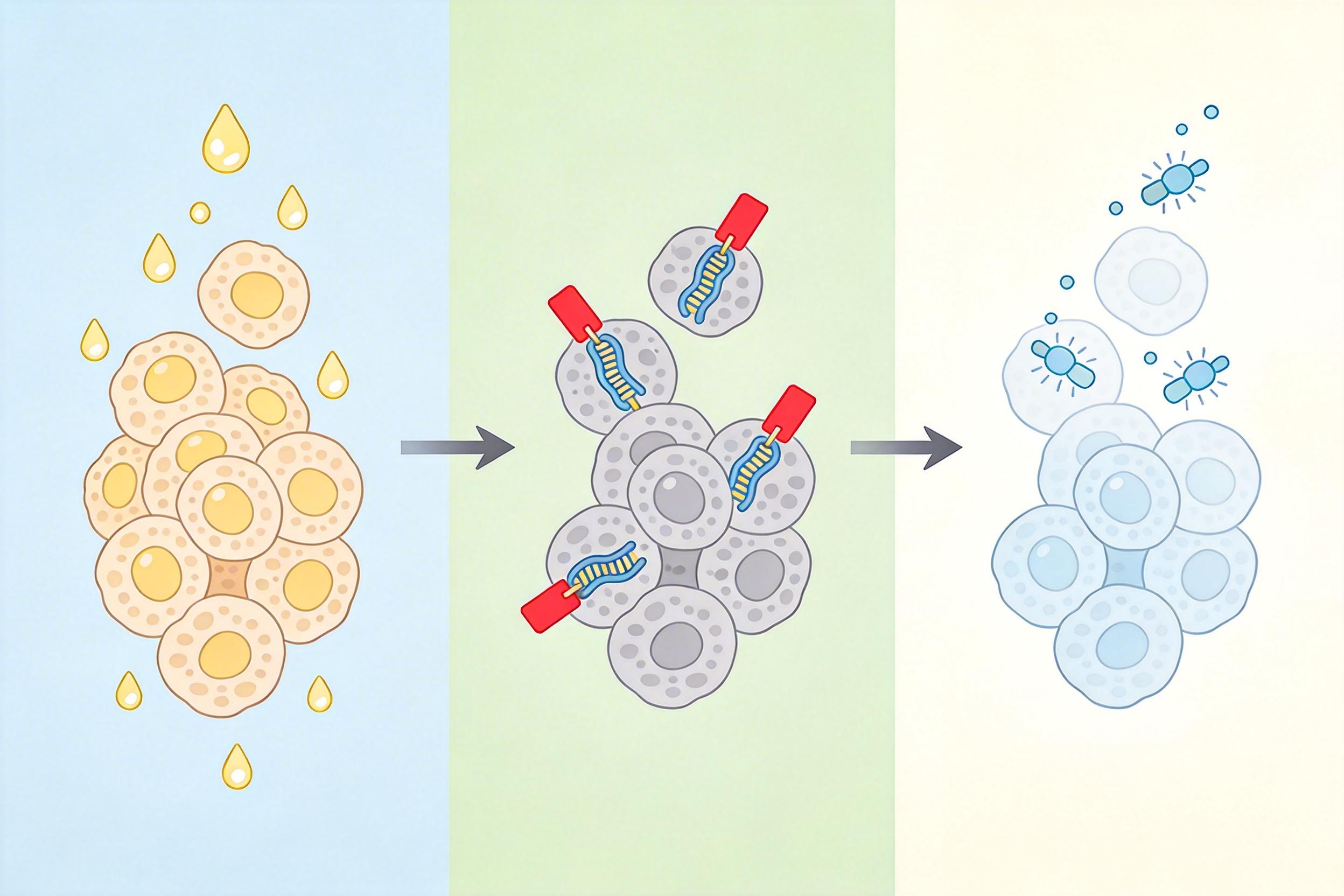
过去,医生们尝试用“广谱轰炸”的方式对付表观遗传失调——比如用DNMT抑制剂擦掉所有“禁止使用”的印章,用HDAC抑制剂撕掉所有“重点推荐”的标签。但这种不分好坏的治疗,不仅会误伤正常细胞,还会因为癌细胞的“应变能力”而迅速耐药。
现在,新的治疗思路终于从“乱打”转向了“精准斩首”:
一是瞄准癌细胞的“致命弱点”——比如针对KDM6A缺失的癌细胞,科学家找到了能让它们“自我毁灭”的合成致死靶点,就像给有特定缺陷的炸弹装上了引爆器;二是打断癌细胞和微环境的“通讯”——比如靶向SIN3B-HDAC1复合物,阻止癌细胞给免疫细胞发“洗脑信号”;三是联合治疗“内外夹击”——用表观遗传药物重新激活癌细胞表面的“通缉令”,再用免疫检查点抑制剂唤醒被驯化的免疫细胞,让它们一起围攻癌细胞。
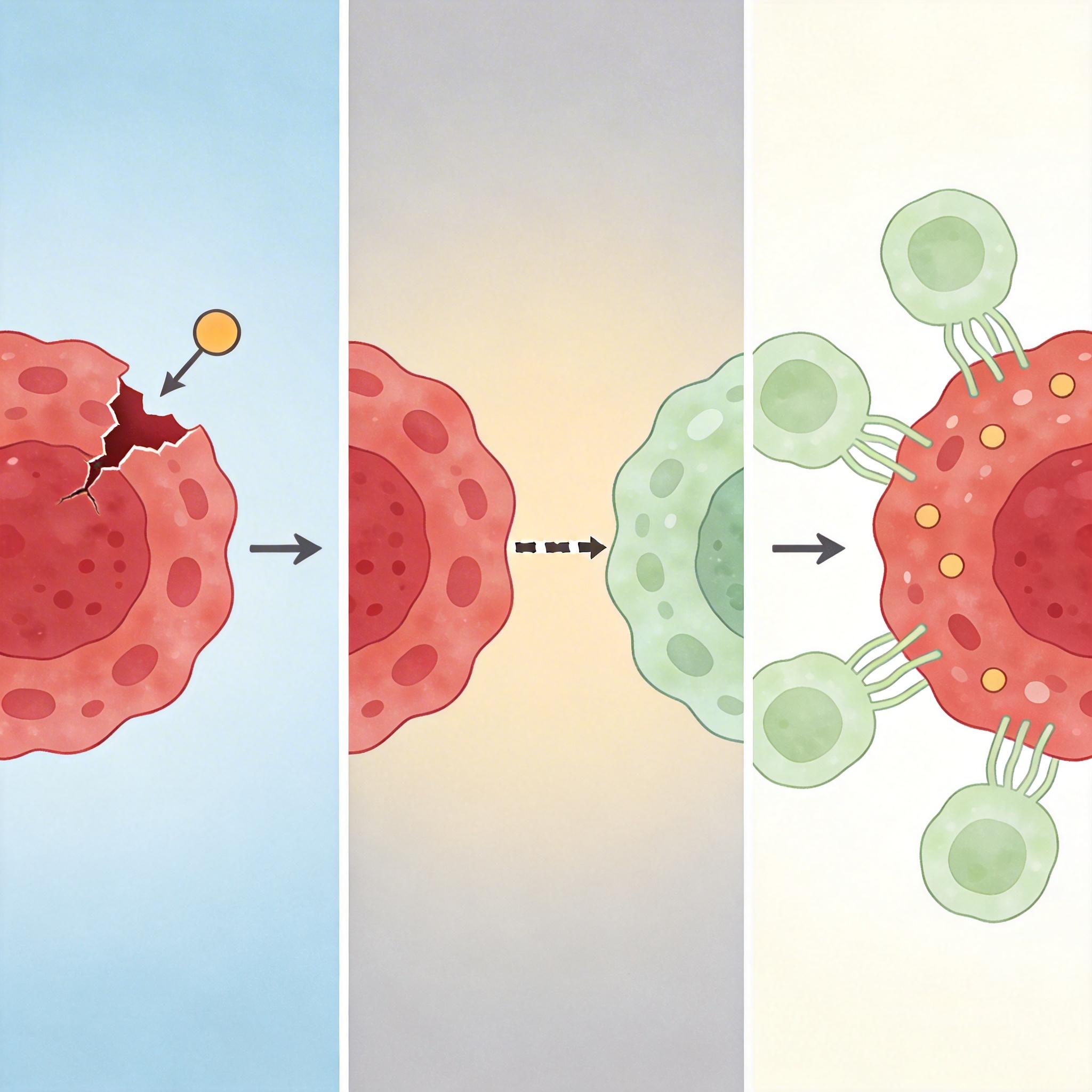
更值得期待的是,液体活检技术的进步,让我们能通过血液里的表观遗传标志物(比如SFRP1甲基化、miR-21),提前半年甚至更早发现胰腺癌,还能预测患者对哪种治疗最敏感。这意味着,未来的胰腺癌治疗,可能会像高血压、糖尿病一样,实现真正的“个性化管理”。
当我们终于看清胰腺癌的“阴谋”——它不是一个孤军奋战的“暴君”,而是一个懂得“团结一切可以团结的力量”的“政客”——我们的治疗思路也终于从“消灭敌人”转向了“瓦解同盟”。
表观遗传研究的意义,从来都不只是找到新的药物靶点,而是让我们重新理解癌症:它不是细胞的“基因突变事故”,而是一场涉及整个身体的“表观遗传政变”。这场政变的可怕之处,不在于它修改了基因,而在于它修改了基因的“使用规则”。
真正的抗癌战争,是一场改写规则的战争。 而我们现在,终于拿到了改写规则的第一笔草稿。