对抗知识焦虑,从看懂这条开始
App 下载
四种难治癌症的共同软肋,被双药组合击中了
难治性肿瘤|杜克-国大医学院|新加坡国家癌症中心|双药联用疗法|BAP1基因突变|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
难治性肿瘤|杜克-国大医学院|新加坡国家癌症中心|双药联用疗法|BAP1基因突变|肿瘤学|医学健康
全球每年超40万新发肾癌患者,胆管癌、间皮瘤、葡萄膜黑色素瘤虽然少见,却凭着极高的侵袭性让医生束手无策——这些癌症对化疗、免疫治疗响应极差,患者生存期往往以月计算。
没人想到,这四种看似毫无关联的绝症,竟共享着同一个致命弱点:它们的细胞里,负责给蛋白质“纠错”的BAP1基因几乎都突变失活了。新加坡国家癌症中心和杜克-国大医学院的研究团队,顺着这个线索摸到了癌症命门,还掏出了一套双药联用的“组合拳”,让这些难治性肿瘤第一次露出了软肋。
你可以把细胞看成一座24小时运转的工厂,蛋白质就是流水线上的工人。当工人被贴上“废弃”标签——也就是泛素化修饰时,就会被送去降解销毁。而BAP1,就是工厂里的质检员:它会仔细检查每一个被标记的工人,把那些只是沾了点灰、还能干活的工人身上的错误标签撕掉,让他们重返岗位。
这个“撕标签”的动作,就是去泛素化。BAP1的本职,是通过去泛素化保护关键蛋白不被误降解,尤其是那些负责DNA修复的蛋白。一旦BAP1突变失活,质检环节彻底瘫痪:本该保留的DNA修复蛋白被胡乱丢弃,有害蛋白却能留在工厂里捣乱。DNA损伤越积越多,细胞分裂彻底失控,癌症就是这样发生的。
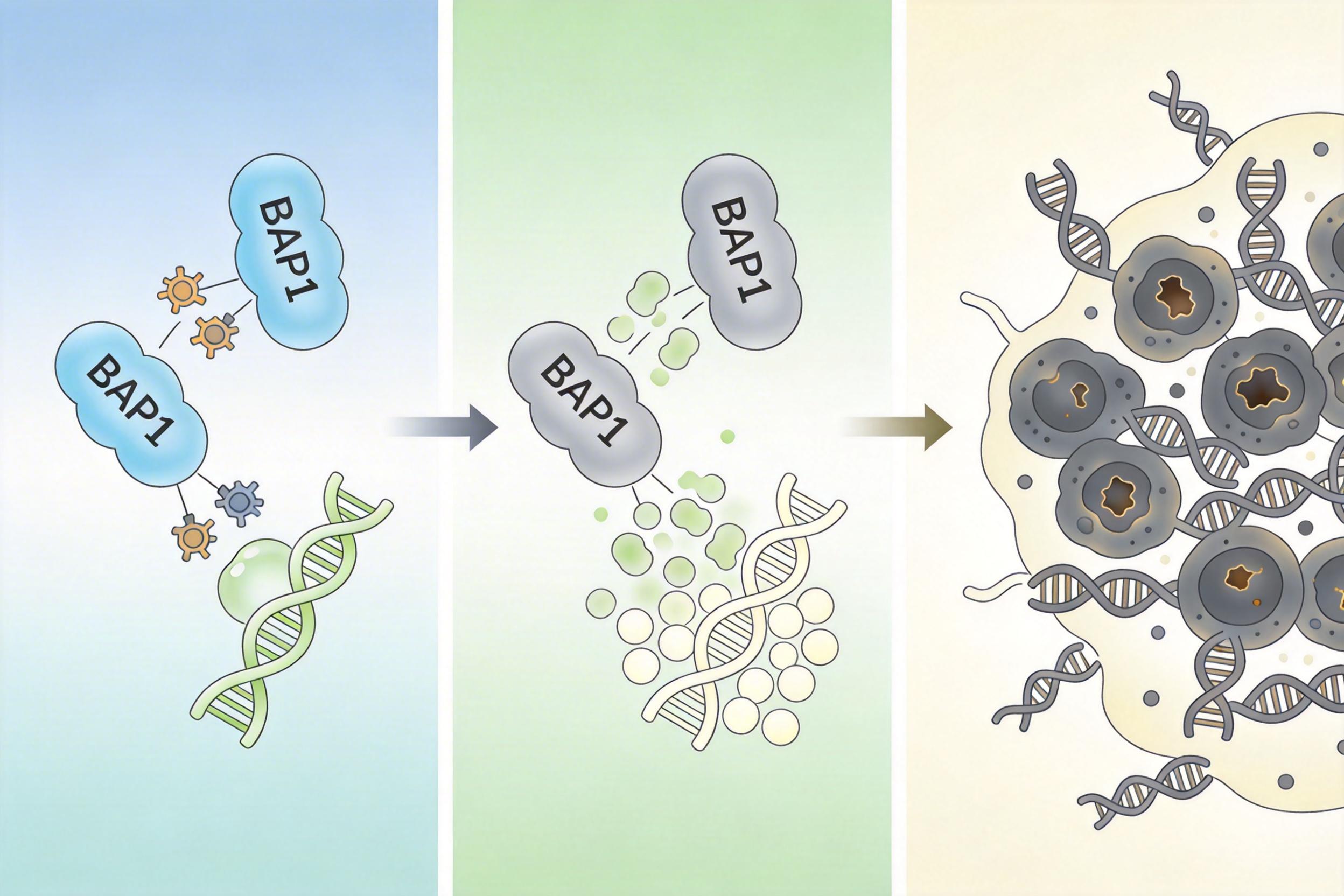
过去的研究只盯着单一癌种,没人发现BAP1的失活,是这四种癌症共同的“病根”。
研究团队横跨四种癌症做了系统性研究,终于摸清了BAP1失活后的细胞漏洞:它会导致全基因组核苷酸切除修复(GG-NER)通路失效——这是细胞修复DNA损伤的核心通路之一。更关键的是,他们通过422种抗肿瘤药物的高通量筛选,找到了两个能精准打击这个漏洞的靶点:LSD1和PARP1。
LSD1的作用是松弛染色质结构,辅助DNA修复;PARP1则负责识别DNA损伤。当BAP1失活后,癌细胞本就依赖这两个蛋白勉强维持修复能力。此时用LSD1抑制剂SP2509和PARP1抑制剂奥拉帕利联合治疗,相当于把癌细胞仅剩的两条修复退路也彻底切断。
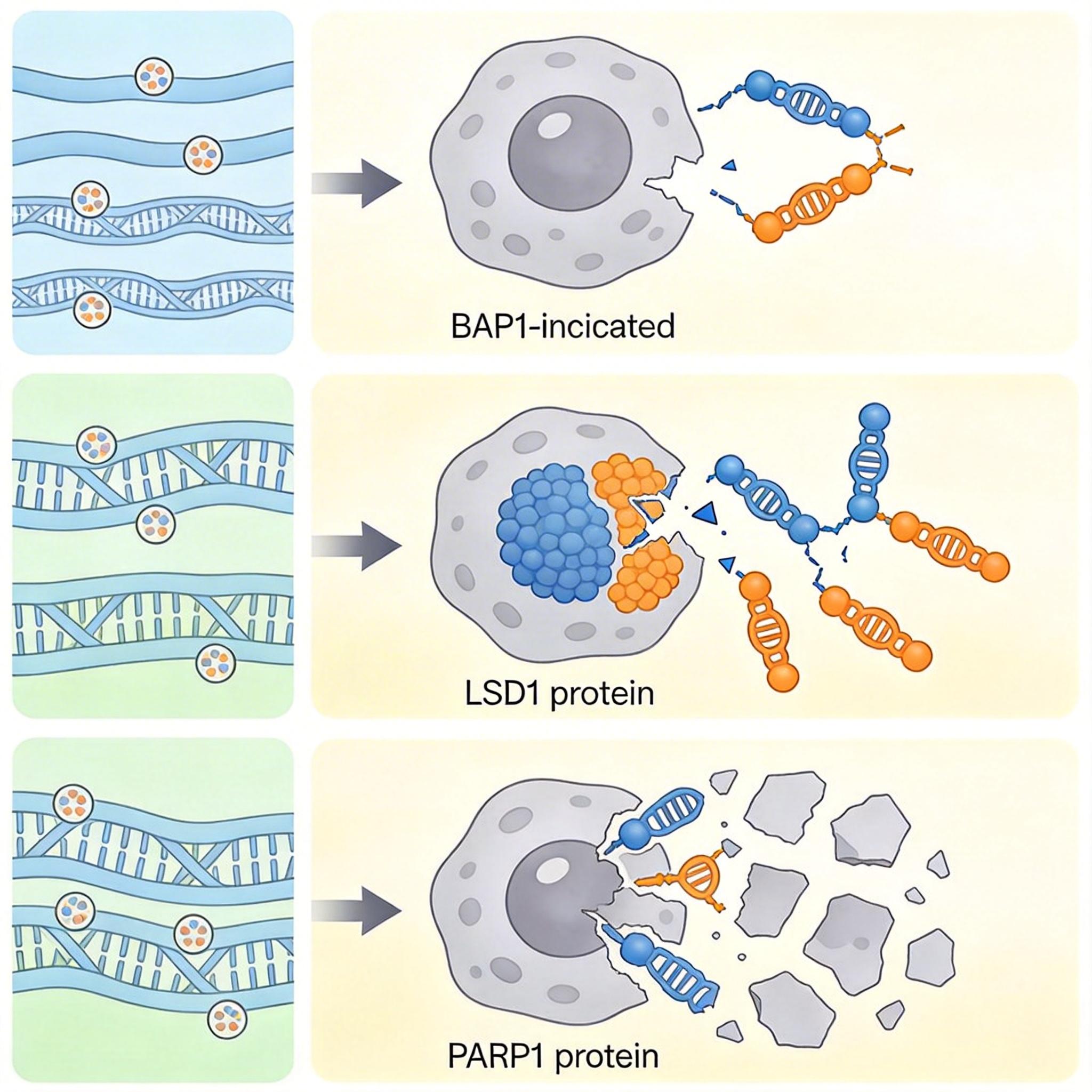
实验室数据显示:在细胞系、患者来源类器官和小鼠模型中,这对组合能让BAP1缺陷的肿瘤体积缩小80%以上,小鼠生存期从25天延长到55天,而且对正常细胞几乎没有影响——因为正常细胞的BAP1功能完好,不需要依赖这两条备份通路。
这项研究的意义,不止是找到了一套新疗法,更在于它打破了过去“单一癌种单一研究”的局限。研究团队发现,BAP1失活在不同癌种里的作用机制高度一致,这意味着这套双药组合可能成为覆盖多癌种的“广谱”精准疗法。
当然,它也并非完美。目前的研究还停留在临床前阶段,人体试验的安全性和疗效还需要验证;而且并非所有BAP1缺陷的癌症都会对这套组合响应,未来还需要更精准的生物标志物来筛选患者。但不可否认的是,它给那些被宣判“无药可治”的患者,第一次带来了明确的希望。
更重要的是,它让我们看到:癌症的“难治”,往往只是因为我们还没找到它们共享的“软肋”。当我们跳出单一癌种的框架,从分子机制的底层逻辑出发,就能找到一网打尽的机会。
过去,我们对付癌症的思路是“见招拆招”——哪种癌难治,就盯着哪种癌找新药。但BAP1的研究告诉我们,有时候更高效的方式,是找到不同癌症背后共通的“病根”。
找对软肋,绝症也有破局之日。
对于那些被间皮瘤、葡萄膜黑色素瘤折磨的患者来说,这不是什么“革命性突破”的空话,而是从“无药可用”到“有路可走”的切实转折。或许用不了多久,这套双药组合就会走进临床,让更多患者能握住那根救命的稻草。