对抗知识焦虑,从看懂这条开始
App 下载
给小鼠做全身CT,看清每一个细胞的位置
Cell期刊|小鼠模型|细胞三维定位|全身透明化CT|Hiroki R. Ueda团队|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
Cell期刊|小鼠模型|细胞三维定位|全身透明化CT|Hiroki R. Ueda团队|分子细胞生物学|生命科学
当病理学家用切片机把小鼠的肝脏切成10微米厚的薄片时,他们其实放弃了99%的真相——那些细胞在三维空间里的依偎、迁徙和聚集,全成了玻璃片上的残影。东京大学的Hiroki R. Ueda团队花了12年,终于把这些残影拼回了完整的生命。他们给新生小鼠做了一次「全身透明化CT」,精准定位了每一个细胞的坐标,甚至能把不同小鼠的全身细胞分布叠在一起对比。这不是科幻片里的场景,而是发表在《Cell》上的现实技术。为什么这项技术能让生物学家集体兴奋?因为它终于把「观察生命」的窗口,从门缝改成了落地窗。
你可以把生物组织想象成一块浸了油的海绵——光线进去就会被散乱的脂肪、色素和细胞成分折射,根本穿不透。CUBIC技术的本质,就是给这块海绵做一次深度清洁:先用氨基醇和尿素的混合液把脂肪「溶」掉,再用去色素剂把血红素这类会吸收光线的成分清除,最后用折射率和细胞一致的溶液填充空隙。
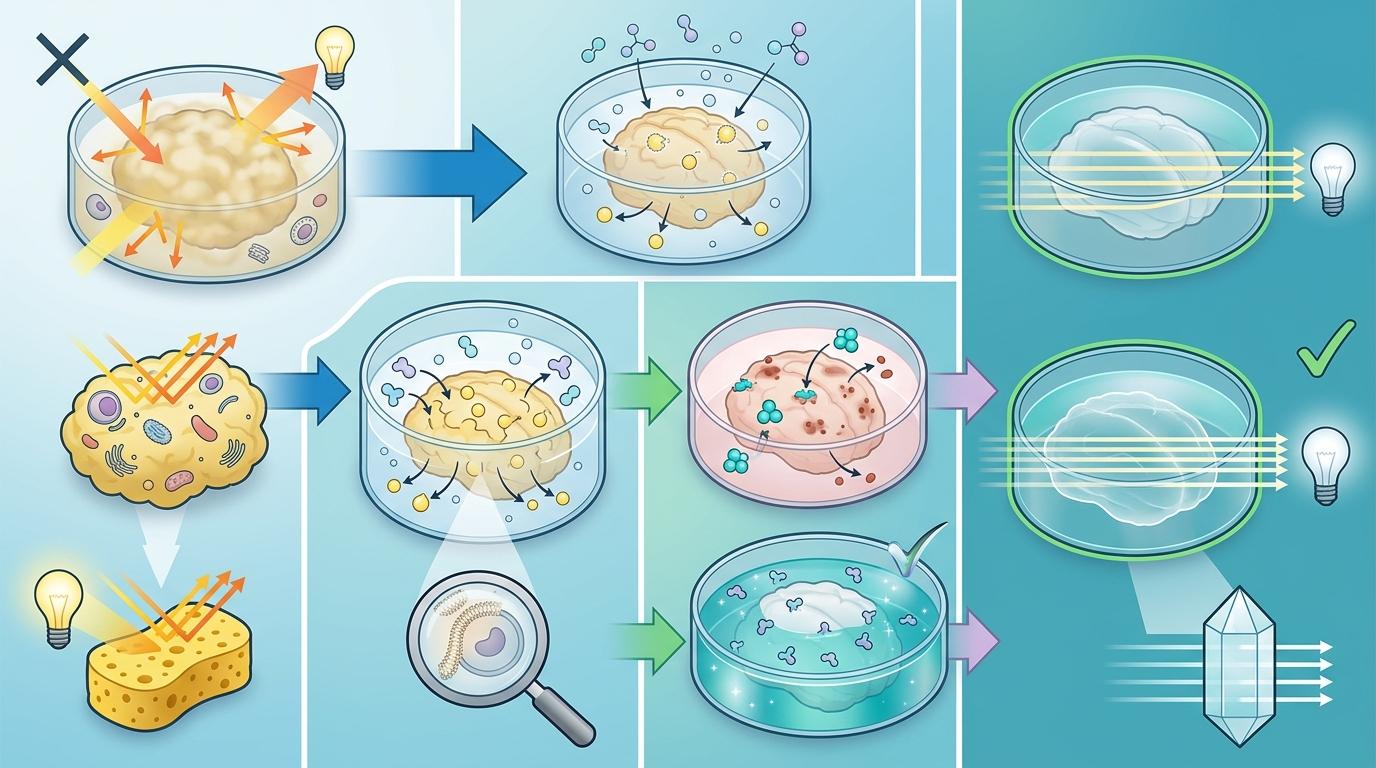
但真实的机制比这更精确。
Ueda团队从2014年就开始迭代这套配方,最新的版本能让整只新生小鼠在3天内变成近乎完全透明的「玻璃小鼠」,同时还能保住细胞上的荧光标记——这意味着后续可以用荧光抗体给特定细胞「上色」。传统的透明化技术要么会让荧光蛋白失效,要么只能处理小块组织,而优化后的CUBIC做到了「鱼与熊掌兼得」:既支持全身尺度,又能保留细胞的分子标记。
接下来是成像环节。他们开发的exMOVIE光片显微镜,能像切面包一样用薄光层逐层扫描透明小鼠,每一层都能捕捉到单个细胞的清晰图像。最终生成的单通道数据就能达到数十TB,足够精确到记录下每一个细胞的三维坐标。
拿到所有细胞的坐标后,团队做了一件更关键的事:给所有小鼠建立了统一的三维坐标框架。
以前的生物研究就像在不同城市的地图上找同一个地址——你说「XX街XX号」,但每个城市的街道都不一样,根本没法对比。现在有了统一的坐标,不同小鼠、不同实验条件下的细胞分布,可以像叠地图一样精准叠加:给小鼠喂了某种药物?直接看全身哪些细胞的位置和数量发生了变化;研究疾病模型?对比健康和患病小鼠的细胞分布差异,就能找到病变的精准区域。
更重要的是,这套系统能和现有的基因表达数据、空间转录组数据对接。比如你知道某个基因在肝脏里高表达,但不知道具体在哪些细胞里——现在只要把三维细胞图谱和空间转录组数据叠加,就能直接定位到表达该基因的细胞群,甚至能看到这些细胞和周围细胞的空间关系。
当然,这项技术还没到完美的地步。目前它只能处理新生小鼠这类体型较小的样本,成年小鼠的组织因为更致密,透明化时间会拉长到数周;而且透明化过程中,部分细胞会出现轻微的体积膨胀,可能影响坐标的绝对精度。
现在,这套技术已经开始向临床应用靠拢。
在肿瘤研究中,科学家可以用它观察癌细胞在全身的转移路径——以前只能在切片里看到孤立的转移灶,现在能完整看到癌细胞从原发肿瘤脱落、进入血液、定植到其他器官的全过程。美国莱斯大学的团队甚至用类似的思路开发了3D打印肿瘤模型,模拟癌细胞在转移过程中的集群行为,发现癌症相关成纤维细胞会像「保镖」一样保护癌细胞,这为开发抗转移药物提供了新靶点。
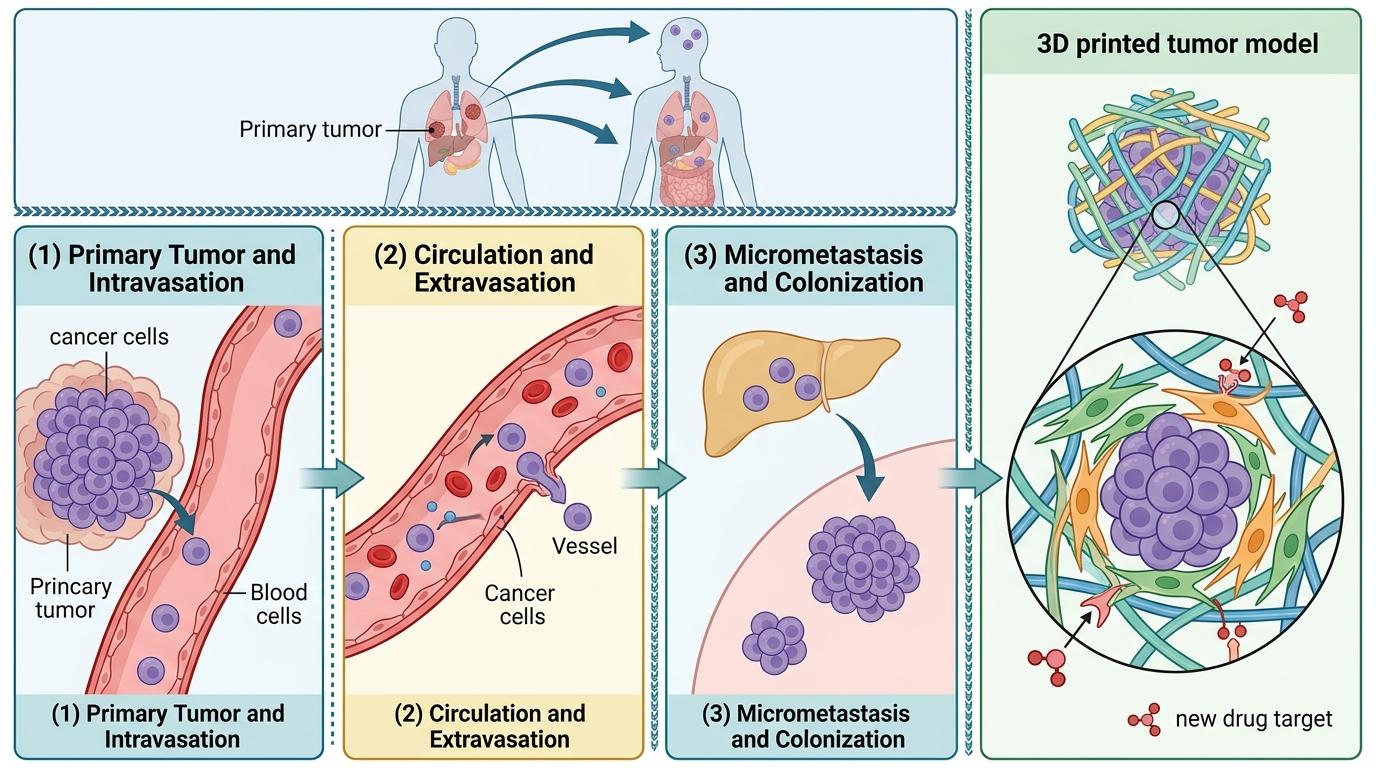
在药物研发领域,它能精准评估药物的全身分布和副作用:以前只能通过血液检测间接判断药物是否到达靶器官,现在可以直接看到药物分子在全身细胞中的富集情况,甚至能量化每个器官里的药物浓度。这能大幅缩短药物筛选的时间,降低研发成本。
不过,要应用到人体样本,还有不少障碍需要跨越:人体组织更厚、更致密,透明化难度更大;而且临床样本的处理需要符合严格的伦理和标准流程,不能像实验室样本那样灵活操作。Ueda团队已经开始优化针对人体组织的CUBIC技术,预计未来5年内能实现人体部分器官的三维细胞图谱构建。
我们对生命的理解,一直被观察工具的边界限制着。从最早的光学显微镜看到单个细胞,到现在的三维细胞图谱看清全身细胞的分布,每一次工具的升级,都让我们离生命的真相更近一步。
「从局部碎片,到全景全貌」——这不仅是这项技术的核心价值,更是生命科学研究的永恒追求。当我们能像看地图一样看清每一个细胞在体内的位置和关系时,那些困扰了我们几十年的疾病机制,或许会在全景图中露出清晰的轮廓。毕竟,生命从来不是二维的切片,而是一场三维的舞蹈。