
21 天前
复旦团队破解跨膜蛋白降解,给难治靶点开了新门
想象一下:你的细胞膜上嵌着几十亿个“功能开关”,它们管着细胞的生死、信号的传递,甚至肿瘤的生长。但这些开关藏在脂质双层的“墙壁”里,传统药物要么够不着,要么碰一下就被细胞“回收”了——90%以上的跨膜蛋白,至今是药物研发的“无人区”。
2026年3月19日,复旦大学鲁伯埙与海军军医大学盛春泉团队在《Cell》上扔出了一颗“炸弹”:他们找到一把能精准拆这些“顽固开关”的分子钥匙,让那些躲在膜里的“不可药物化”靶点,第一次暴露在有效的降解机制下。这把钥匙,就是ERADEC。
细胞里的“垃圾处理站”,原来可以这么用
要懂ERADEC,得先搞懂细胞自带的“内质网相关降解系统”——ERAD,你可以把它看成内质网膜上的“垃圾分拣站”。平时它只处理那些折叠错误的“废品蛋白”:先由站里的核心分拣员SYVN1(一种E3泛素连接酶)给废品贴个“销毁标签”(泛素化),再由p97分子机把蛋白从膜里“拽”出来,最后送到蛋白酶体里拆成碎片。
过去的靶向蛋白降解技术,要么盯着细胞质里的蛋白(比如PROTAC),要么靠溶酶体慢慢“消化”(比如LYTAC),但对嵌在膜里的蛋白都束手无策:前者够不着膜,后者经常被细胞的“回收系统”截胡,降解效率低得可怜。
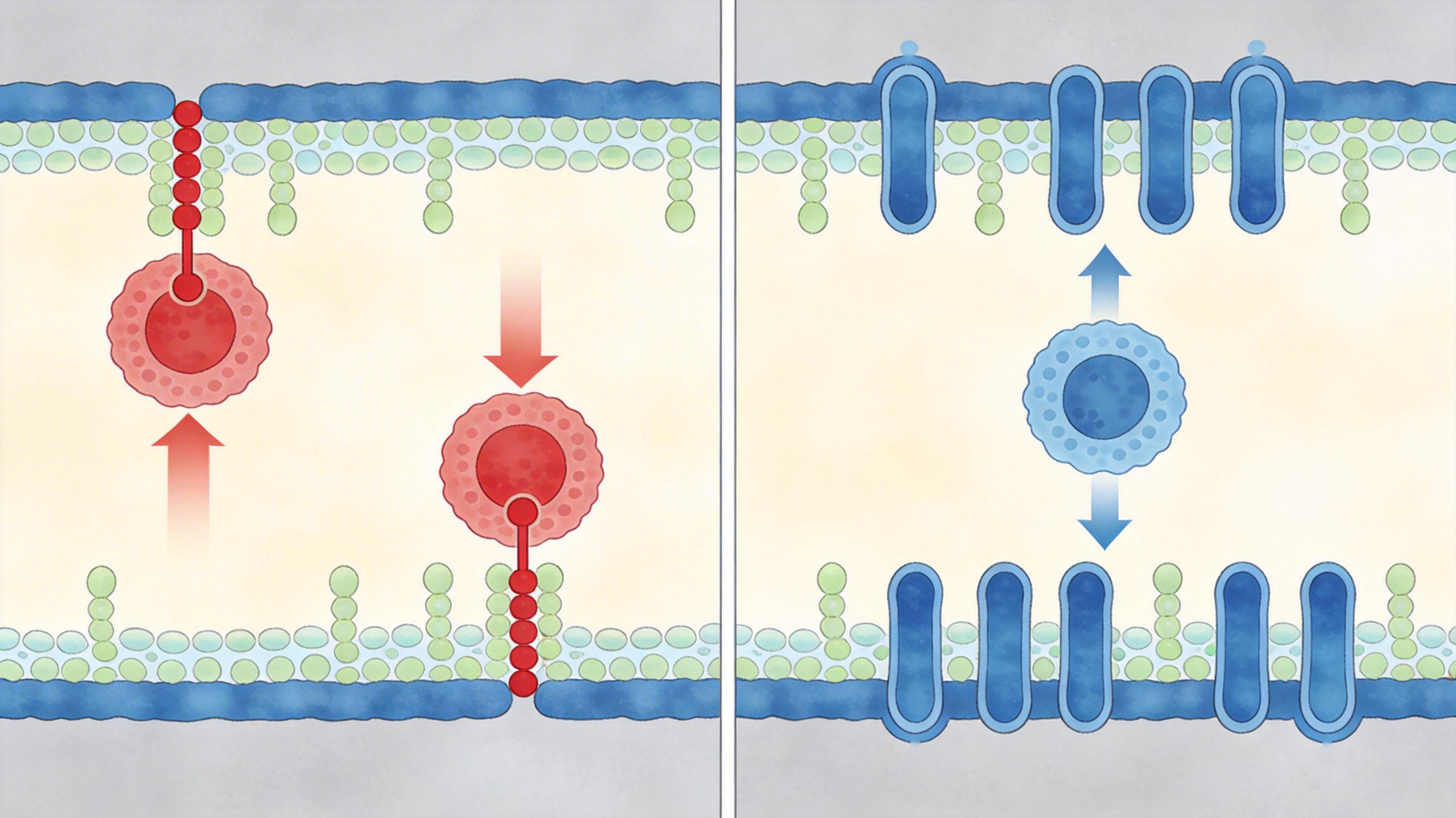
研究者做了一个大胆的决定:不如直接“劫持”ERAD这个现成的分拣站。他们设计出一种双功能小分子ERADEC,一头粘住目标跨膜蛋白,另一头死死勾住SYVN1——相当于给正常的功能蛋白也贴了个“销毁标签”,让ERAD把它当成废品处理。
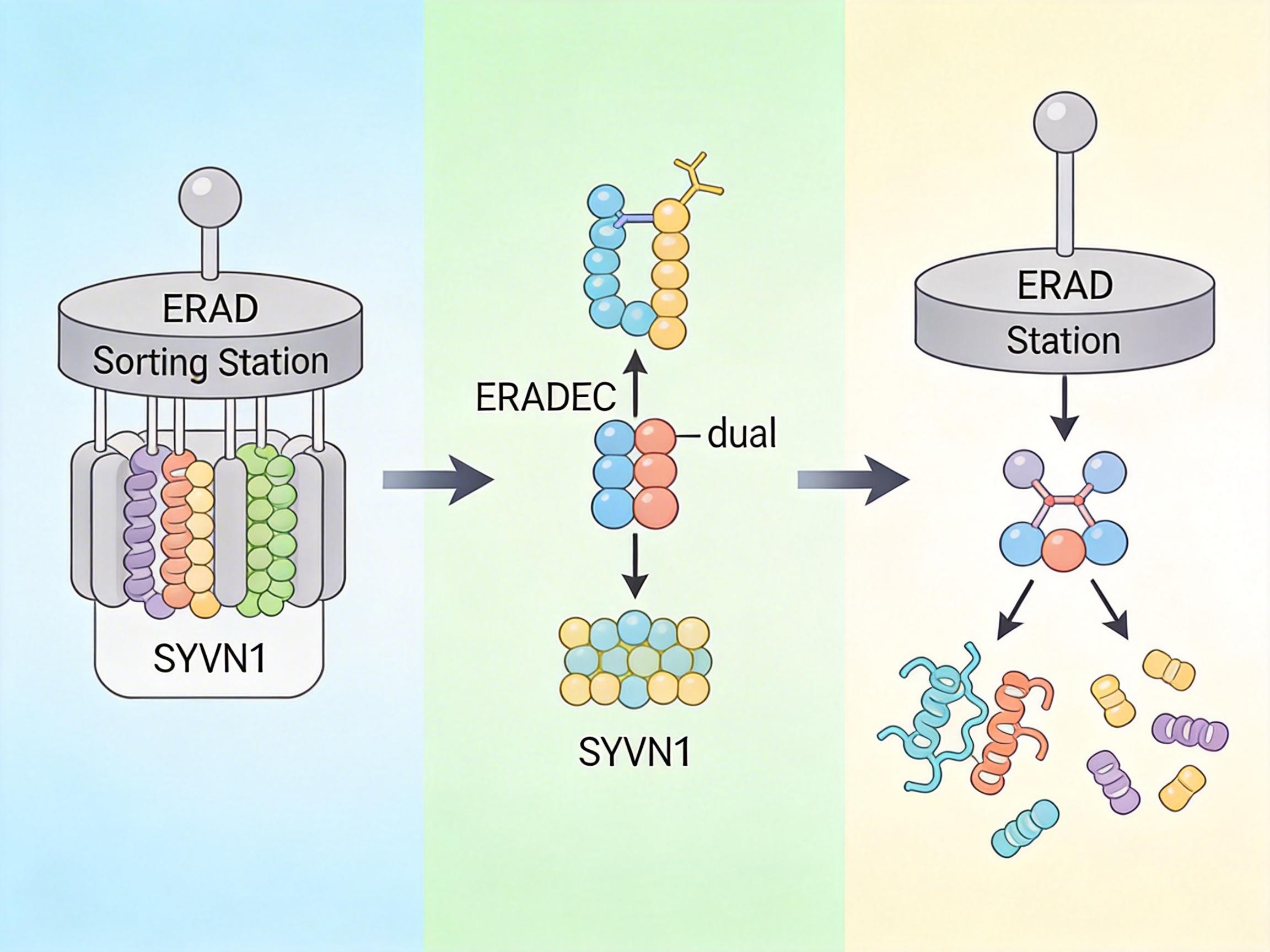
从实验室到小鼠,效率比抗体还高
他们先拿肿瘤免疫的关键靶点PD-L1开刀。PD-L1是肿瘤细胞膜上的“隐身斗篷”,能躲避免疫系统攻击,临床用的抗体药物只能结合它的表面部分,还容易被肿瘤细胞“回收再利用”。
研究者把能结合SYVN1的地塞米松,和已知的PD-L1配体连在一起,做成了针对PD-L1的ERADEC分子。结果让所有人意外:
在细胞实验里,ERADEC能在几小时内把PD-L1的水平打掉70%以上;在小鼠肿瘤模型里,它不仅能更彻底地清除肿瘤细胞表面的PD-L1,抑制肿瘤生长的效果居然比临床用的PD-L1抗体还要强。
更关键的是,ERADEC是小分子——它能轻松穿透细胞膜,不用像抗体那样靠复杂的递送系统,成本更低,也不会引发免疫反应。而且它绕开了溶酶体的回收陷阱,直接在内质网膜上完成标记和降解,新合成的蛋白刚到膜上,就会被ERADEC盯上。
不是万能钥匙,还有三道关要闯
当然,ERADEC不是完美的。
首先,它目前只绑定了SYVN1这一个“分拣员”,能处理的跨膜蛋白靶点还很有限——要是能找到更多内质网上的E3连接酶,ERADEC的适用范围才能真正打开。
其次,小分子的“双功能”设计是个技术活:既要精准粘住目标蛋白,又不能影响SYVN1的正常功能,稍有不慎就可能“错杀”无辜蛋白,引发副作用。
最后,细胞的ERAD系统本来是维持蛋白稳态的关键,长期“劫持”它会不会导致正常蛋白被误判?比如内质网里的折叠错误蛋白会不会因为SYVN1被占用而堆积,引发内质网应激?这些问题都得在临床前研究里一一验证。
用研究者的话说:“我们只是打开了一扇门,门后面的路还很长。”
从1999年PROTAC概念提出,到现在ERADEC破解跨膜蛋白的难题,靶向蛋白降解技术走了27年。这期间,科学家一直在和细胞的“自我保护机制”博弈:要么找更聪明的分子,要么“借”细胞自己的工具用。
ERADEC的意义,不止是给PD-L1这类靶点提供了新的治疗方案,更重要的是它证明了一个思路:细胞里那些被当成“基础功能”的系统,其实都可能成为药物研发的“新战场”。
能借的力,才是最省力的力。 未来的药物,或许不再是直接“攻击”靶点,而是学会“引导”细胞自己解决问题——这可能才是精准医疗最该有的样子。
点击充电,成为大圆镜下一个视频选题!