
8 天前

8 天前
当脊髓或神经被损伤,医生能做的往往只有固定脊柱、控制炎症——剩下的,只能靠患者自身那点微弱到可以忽略的再生能力。每年全球数百万神经损伤患者,从此被钉在轮椅或麻木的肢体上。但2026年4月,西奈山伊坎医学院的团队捅破了一层窗户纸:他们找到神经再生路上的那只「看不见的手」——芳香烃受体(AhR),只要松开这只手,受伤的神经轴突就能以快30%的速度重新生长。为什么一个原本用来感知环境毒素的蛋白,会成为神经修复的关键刹车?
你可以把AhR想象成神经元里的「应急总指挥」。它原本的工作是感知进入体内的环境毒素,比如多环芳烃、二恶英,然后启动解毒程序——让细胞优先合成清理毒素的蛋白,暂停一切非必要的生长活动。这在平时是保护机制,但当神经受伤时,这个机制就成了灾难。
神经损伤的瞬间,神经元会遭遇双重打击:一是物理断裂的轴突需要重新生长,二是损伤引发的炎症和氧化应激像洪水一样涌来。此时AhR会被迅速激活,它会下达死命令:停止合成新的生长蛋白,全力启动应激保护——修复受损蛋白、清理氧化废物、抑制炎症扩散。就像一场火灾里,大楼管理员下令关闭所有非必要电源,虽然保住了核心结构,却也切断了修复所需的电力。
实验数据最有说服力:在小鼠坐骨神经损伤模型中,被敲除AhR基因的小鼠,轴突最长再生长度从1.06毫米跃升至1.44毫米,提升了36%;运动功能恢复时间直接缩短了三分之一。更关键的是,这种效果在老年小鼠身上同样显著——原本因年龄增长而近乎停滞的神经再生,在松开AhR刹车后,恢复到了年轻小鼠70%的水平。
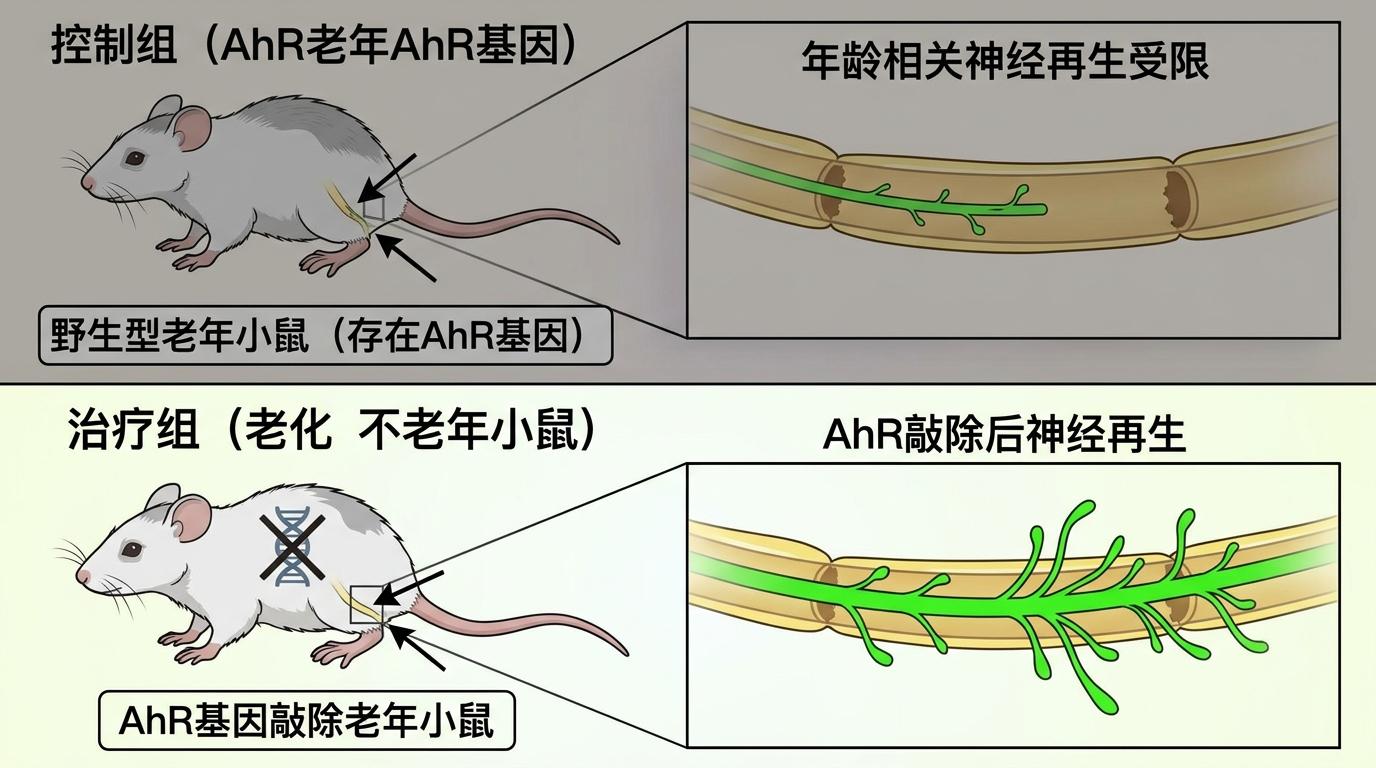
AhR的刹车之所以能起作用,核心是它和另一个叫HIF-1α的蛋白,在争夺同一个「搭档」——ARNT。
HIF-1α是细胞里的「生长总指挥」,平时在氧气充足的环境下会被快速降解,但一旦细胞需要生长或修复(比如神经损伤后),它就会稳定下来,和ARNT结合,启动一系列促生长基因:促进蛋白质合成、激活mTOR通路、调控代谢为生长供能。而AhR激活后,会抢先和ARNT结合,把这个关键搭档牢牢攥在手里,让HIF-1α找不到合作伙伴,只能待在细胞质里无所事事。
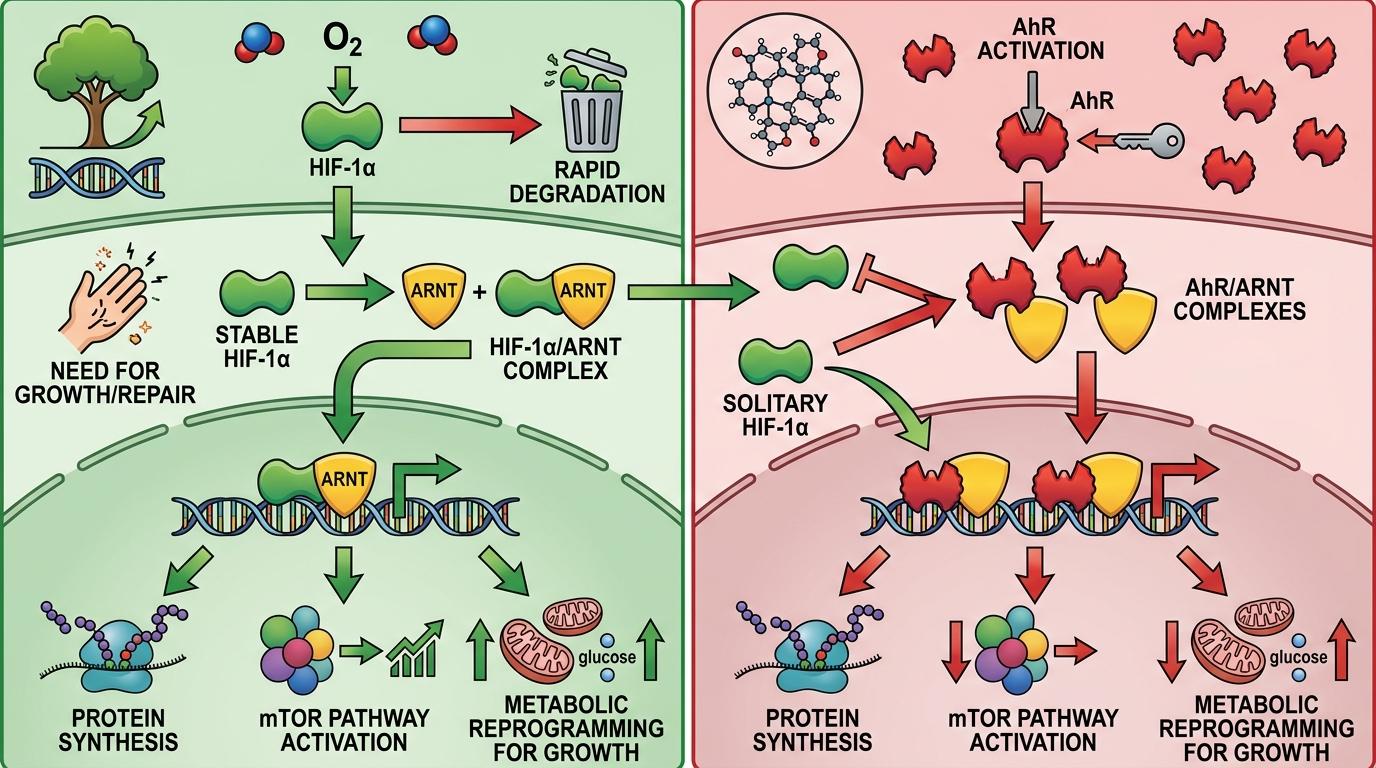
当研究人员用药物或基因敲除抑制AhR后,这场分子拉锯战的胜负瞬间逆转:被释放的ARNT立刻和HIF-1α结合,生长信号通路瞬间被点燃。神经元从「保命模式」切换到「修复模式」——原本被抑制的蛋白质合成机器重新启动,轴突尖端的生长锥开始疯狂延伸,沿着残留的神经通路寻找连接目标。
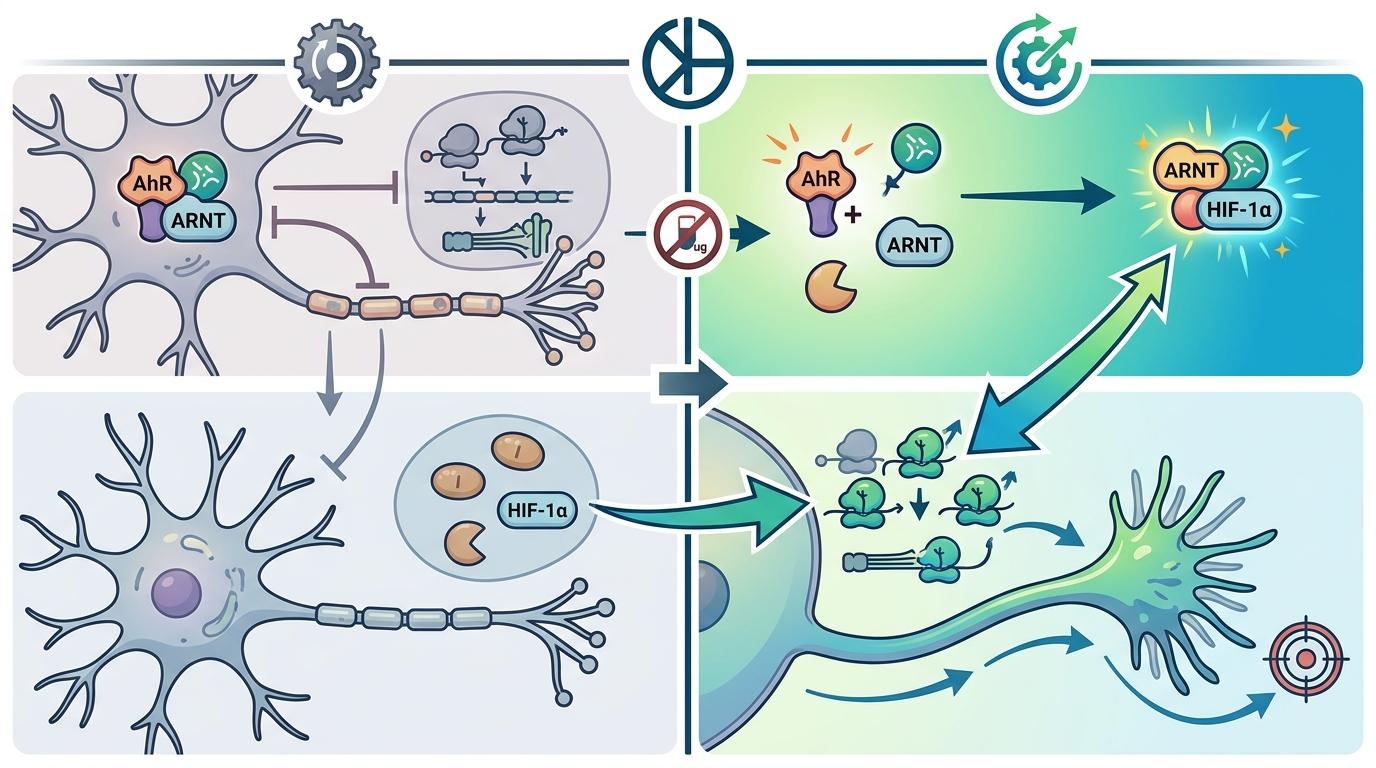
有意思的是,研究团队发现肠道菌群的代谢产物并没有参与这个过程,说明AhR的刹车作用完全是神经元内部的自主调控——这也为后续的临床转化减少了变量,不用考虑患者的肠道菌群差异对药效的影响。
现在最让人兴奋的是,AhR抑制剂并非全新的药物——已有多款针对AhR的拮抗剂正在癌症、免疫疾病的临床试验中,这意味着它们的安全性已经过初步验证,最快可能在3-5年内进入神经损伤的临床研究。比如已被证实能促进造血干细胞扩增的StemRegenin 1(SR1),在动物实验中能显著促进神经轴突再生,而且它的作用机制非常明确:就是通过阻断AhR和ARNT的结合,释放HIF-1α的生长信号。
但隐忧同样存在。AhR毕竟是体内的「应急总指挥」,长期抑制会不会导致细胞失去对环境毒素的抵抗力?研究团队在小鼠身上观察了6个月,发现敲除AhR的小鼠并没有出现明显的解毒功能障碍——这可能是因为体内还有其他解毒通路可以代偿,但人体的情况是否一样,还需要长期的临床试验验证。
更关键的是,神经再生不是单纯的「轴突变长」就够了——还需要新生的轴突准确连接到原来的靶细胞,形成有功能的神经回路。目前的研究只证明了AhR抑制能促进轴突生长,但能否帮助轴突找到正确的方向,重新建立功能连接,还是一个未解之谜。
过去我们总以为,神经损伤后无法再生是因为环境里充满了抑制因子——比如胶质瘢痕、髓鞘碎片。但AhR的发现让我们意识到,最大的障碍可能来自神经元自身:它为了保命,主动关闭了再生的开关。
「松开刹车,比踩油门更重要。」这句话放在神经再生领域再合适不过。未来的神经修复,可能不是给神经元注入多少生长因子,而是帮它卸下「保命优先」的包袱,让它敢重新生长。
当然,这只是第一步。就像一辆停在废墟里的汽车,松开刹车后,还需要清理路障、加满油、掌握方向才能重新上路。但至少现在,我们找到了启动这辆车的钥匙。
点击充电,成为大圆镜下一个视频选题!