
9 天前
治白血病的老药,成了激活肿瘤免疫的新钥匙
当医生给一位晚期肺癌患者用上PD-1抗体时,所有人都在等奇迹——但肿瘤纹丝不动。这不是个例:超过70%的患者对这类当下最火的免疫疗法没反应,核心原因是他们的肿瘤是「冷的」——免疫细胞根本找不到肿瘤在哪,更别说发起攻击。
安徽农业大学的研究团队,最近在一堆临床老药里翻出了破局的可能:一款原本治白血病的巴非替尼,居然能精准撬开肿瘤的免疫「锁芯」。它不是直接杀癌细胞,而是激活免疫细胞里的一个关键开关,让沉睡的免疫系统突然醒过来,浩浩荡荡冲进肿瘤里。
那个被忽略的免疫开关
你可以把NLRP3炎症小体想象成免疫细胞里的「警报器」——平时安安静静待在角落,一旦感知到危险信号,就会触发一连串反应:释放炎症因子、召唤免疫援军,甚至直接启动细胞的「自爆程序」清理病原体。
但真实的机制比这更精确:这个警报器的启动需要一个关键前提——细胞内的钾离子必须快速流出。就像警报器需要拔掉保险栓,钾离子外流就是那个「拔栓」动作。而巴非替尼,刚好瞄准了控制钾离子外流的「阀门」——钾离子通道TWIK2。
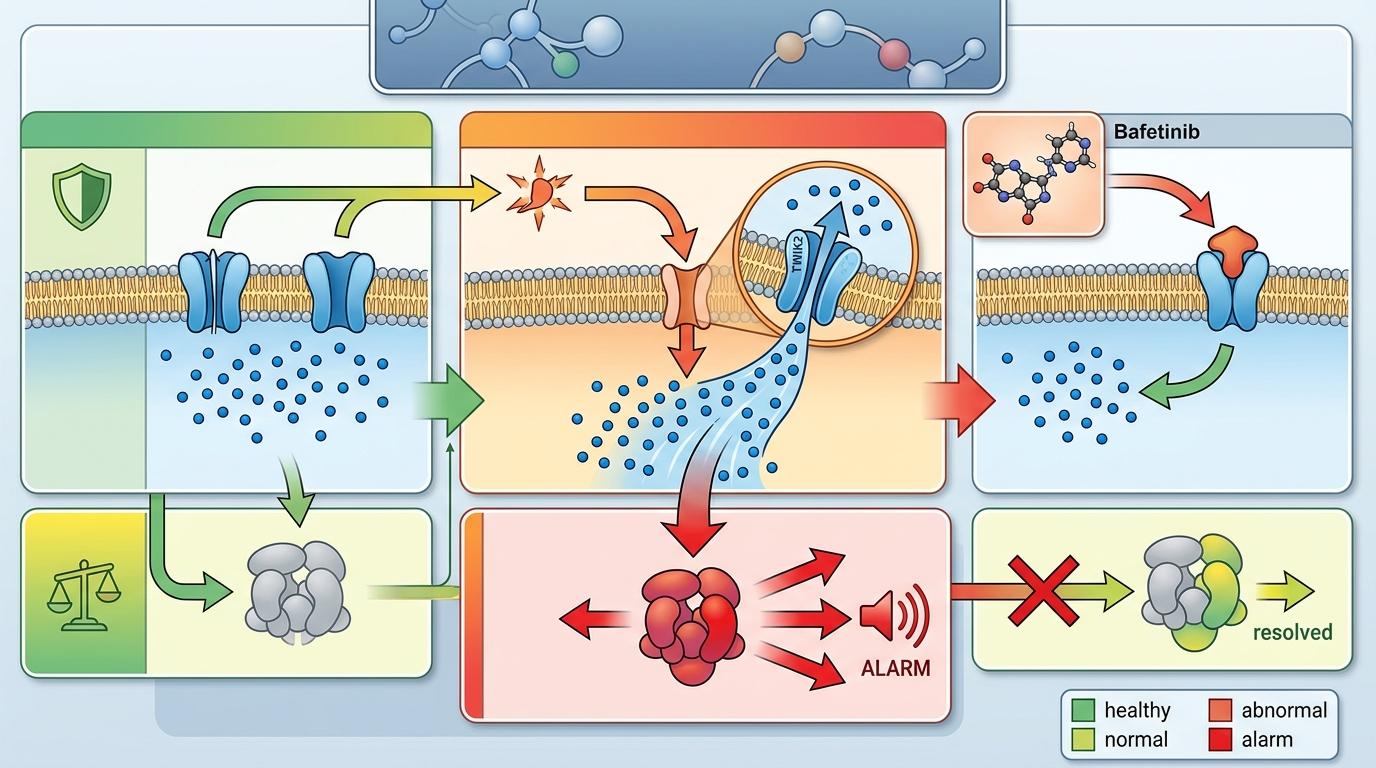
它不是直接拧开阀门,而是挡住了细胞回收这个阀门的「垃圾处理通道」,让更多TWIK2留在细胞膜上。阀门多了,钾离子自然大量外流,NLRP3警报器也就被精准触发了。
更重要的是,这个过程完全独立于巴非替尼原本治白血病的靶点——相当于一款老药,意外解锁了全新的技能树。
给老药装个「肿瘤导航」
就算巴非替尼能激活免疫警报,直接吃药还是会有麻烦:药物会跑到全身各处,可能触发不必要的炎症反应。研究团队给它配了个「肿瘤专属导航」——缺氧响应型纳米颗粒。
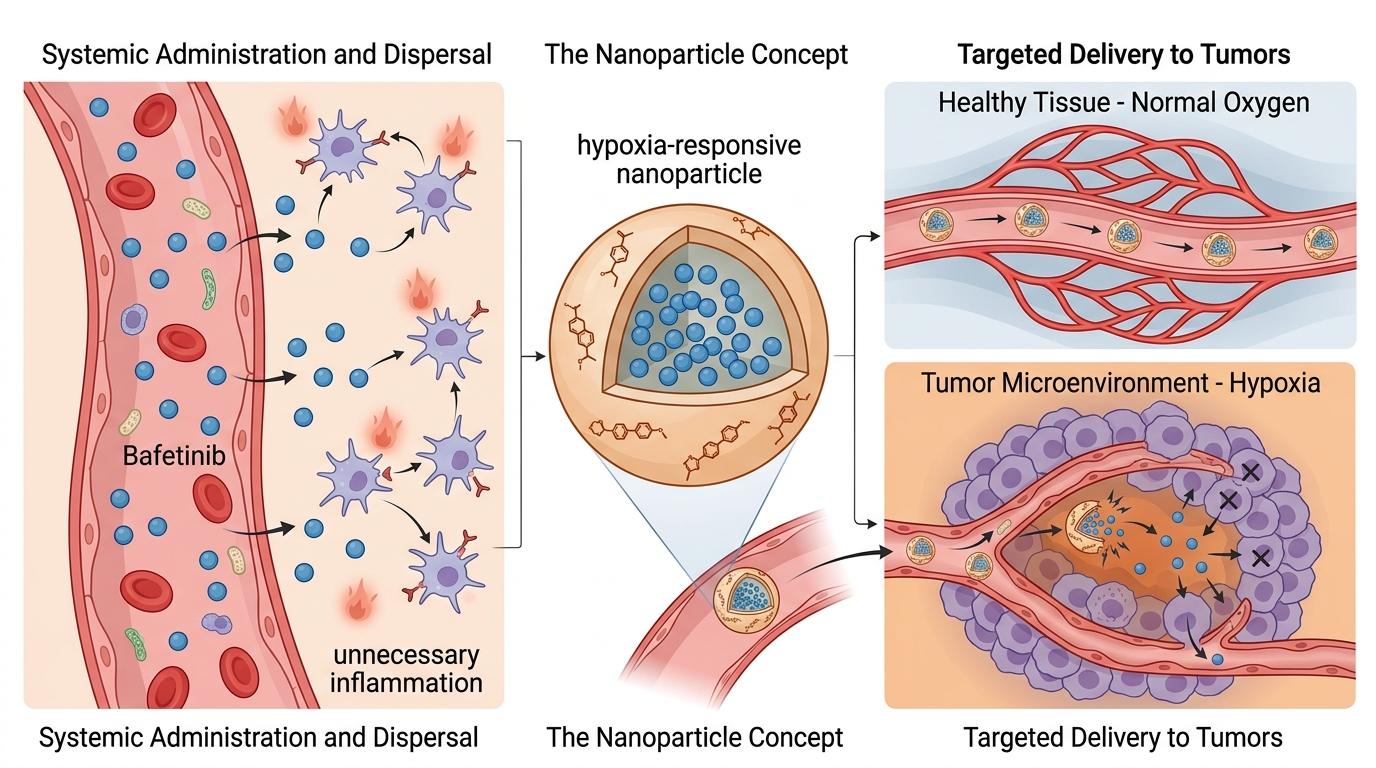
肿瘤因为长得太快,内部往往缺氧,就像一个没装通风系统的拥挤房间。这种纳米颗粒一进入缺氧环境,外壳就会自动溶解,把巴非替尼精准释放到肿瘤里。
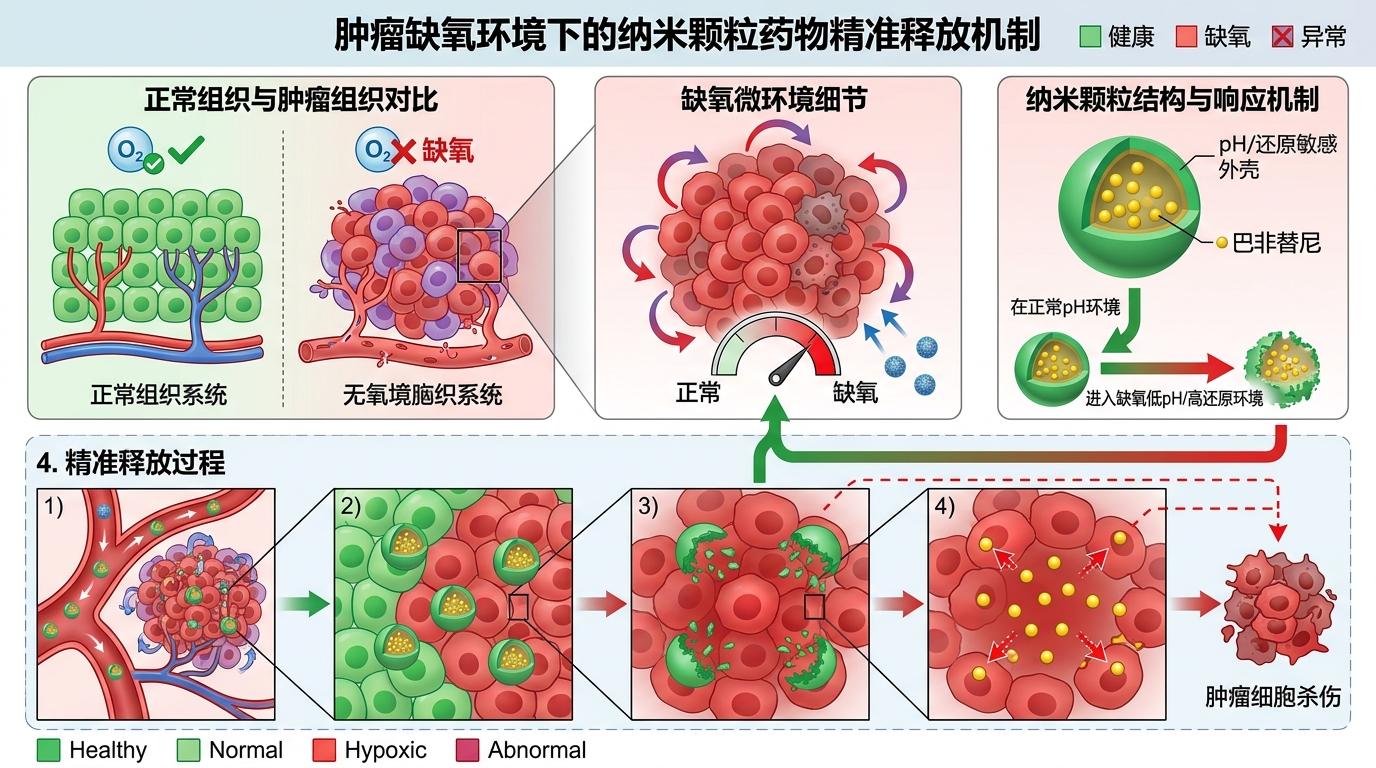
在小鼠实验里,装了导航的巴非替尼表现出了惊人的效果:它先激活肿瘤里的巨噬细胞,让这些原本「中立」的免疫细胞瞬间变成「战斗模式」,释放的信号招来了大量CD8+T细胞——就是那种能直接咬死癌细胞的「免疫特种兵」。单独使用时,它能显著抑制肿瘤生长;和PD-1抗体联用时,更是把治疗效果又翻了一倍。
有意思的是,在没有免疫系统的裸鼠身上,这款药几乎没效果——它的所有威力,都来自于唤醒沉睡的免疫系统。
希望背后的三道关卡
当然,这个发现离真正走进病房,还有几道必须跨过的关卡。
首先是「度」的问题:NLRP3炎症小体就像一把双刃剑,激活不够没用,激活过度可能引发全身炎症风暴,反而伤了患者。巴非替尼的激活强度刚好卡在「有效又安全」的区间吗?还需要更多临床数据验证。
其次是纳米颗粒的产业化:实验室里做出几克样品不难,但要大规模生产出质量稳定、批次一致的纳米药物,还要通过监管部门的层层审核,又是一场硬仗。
最后是肿瘤的「个性化」:不同患者的肿瘤缺氧程度不一样,免疫状态也千差万别,这款药不可能包治所有癌症。未来还得找到能精准筛选适合患者的生物标志物,才能真正实现精准治疗。
当我们把目光从「直接杀癌细胞」转向「唤醒免疫系统」,肿瘤治疗的边界正在被重新拓宽。巴非替尼的故事,本质上是科学家在旧药堆里挖出新宝藏的过程——它提醒我们,很多时候,破解难题的钥匙,可能早就摆在我们面前,只是换了个场景就认不出来了。
老药新用,是对抗癌症最务实的破局思路。毕竟,比起从零开始研发一款新药,给经过临床验证的老药找个新用途,不仅成本更低,也能让患者更快用上有效的治疗方案。在和癌症的持久战里,每一个这样的小突破,都是在为最终的胜利铺路。
点击充电,成为大圆镜下一个视频选题!