14 小时前

14 小时前
当结核分枝杆菌悄悄钻进肺部,人体会迅速拉起一道“围墙”——结核肉芽肿。这层由巨噬细胞、淋巴细胞紧密堆叠的防御工事,本该把病菌牢牢锁死,却成了慢性感染的“温床”:全球每年仍有160万人因结核病死亡,传统的增强免疫疗法甚至会加重病情。
2026年4月,中科院微生物所等团队在《自然·微生物学》上的研究,戳破了这层矛盾的窗户纸:肉芽肿里的免疫细胞不是“不卖力”,是被过量的胆固醇绊住了脚。这道本该御敌的防线,为何会变成病菌的避难所?
你可以把巨噬细胞想象成肺部的“巡逻保安”,它的本职是抓住病菌、拆解抗原,再通过表面的MHC II类分子——相当于“通缉令”——把病菌特征传递给CD4+ T细胞,召唤后者来精准杀菌。但结核分枝杆菌很狡猾,它会篡改巨噬细胞的代谢指令:一方面诱导巨噬细胞疯狂摄取和合成胆固醇,另一方面堵住胆固醇外排的通道,让大量胆固醇淤积在溶酶体里。
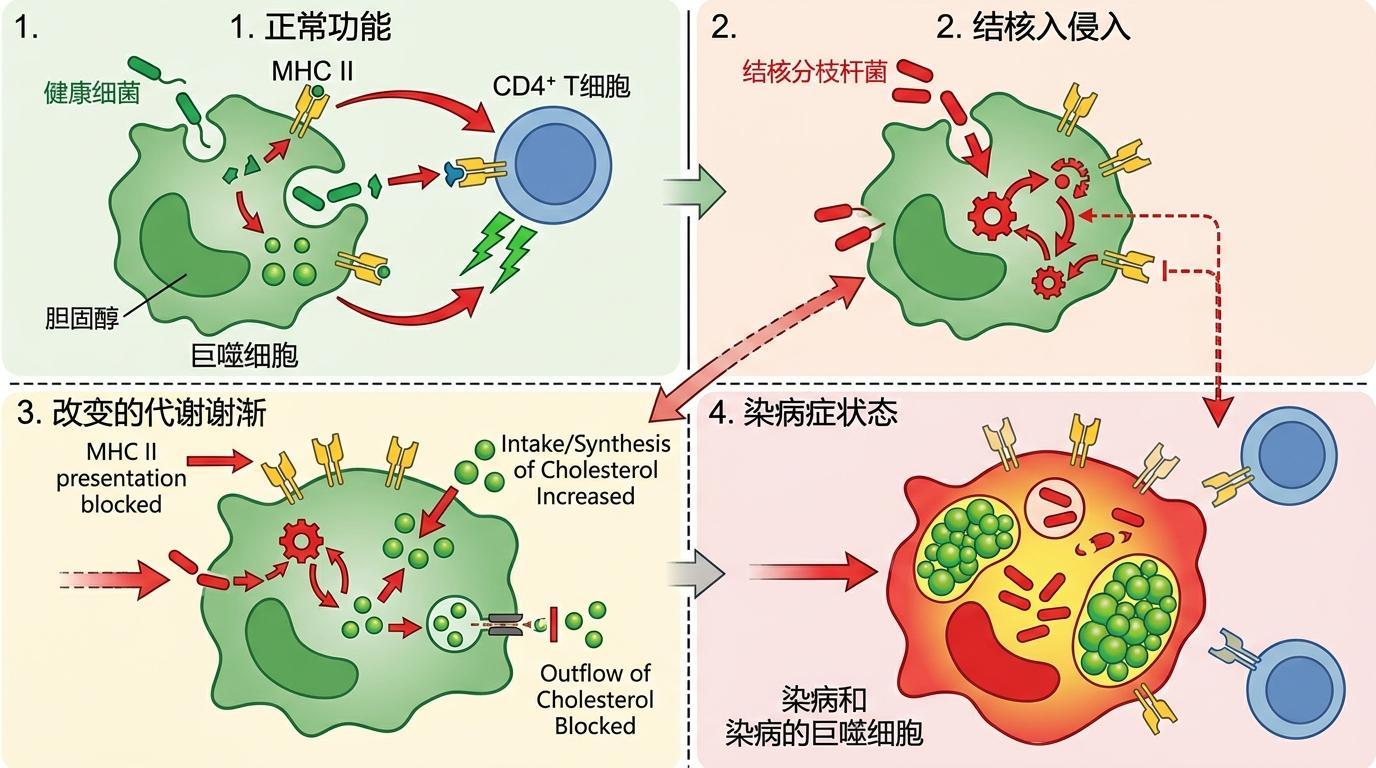
这就像保安的办公室被堆满了无用文件,连整理通缉令的桌子都没有了。溶酶体里的胆固醇会直接“绑架”MHC II类分子,要么让它无法结合病菌抗原,要么把它困在细胞里送不出表面。空间转录组学的图像显示,在坏死性肉芽肿中,巨噬细胞表面的MHC II类分子数量比正常状态下降了近60%,周围的CD4+ T细胞也大多处于“休眠”状态——它们根本接不到开战的信号。
更糟的是,过量胆固醇会让巨噬细胞变成“泡沫细胞”:细胞内充满脂滴,既失去了吞噬病菌的能力,还会释放抗炎信号,给肉芽肿内部营造出一种“和平假象”。而结核分枝杆菌就靠吞噬这些脂滴里的胆固醇存活,甚至能在泡沫细胞里进入休眠状态,躲过药物和免疫细胞的追杀。
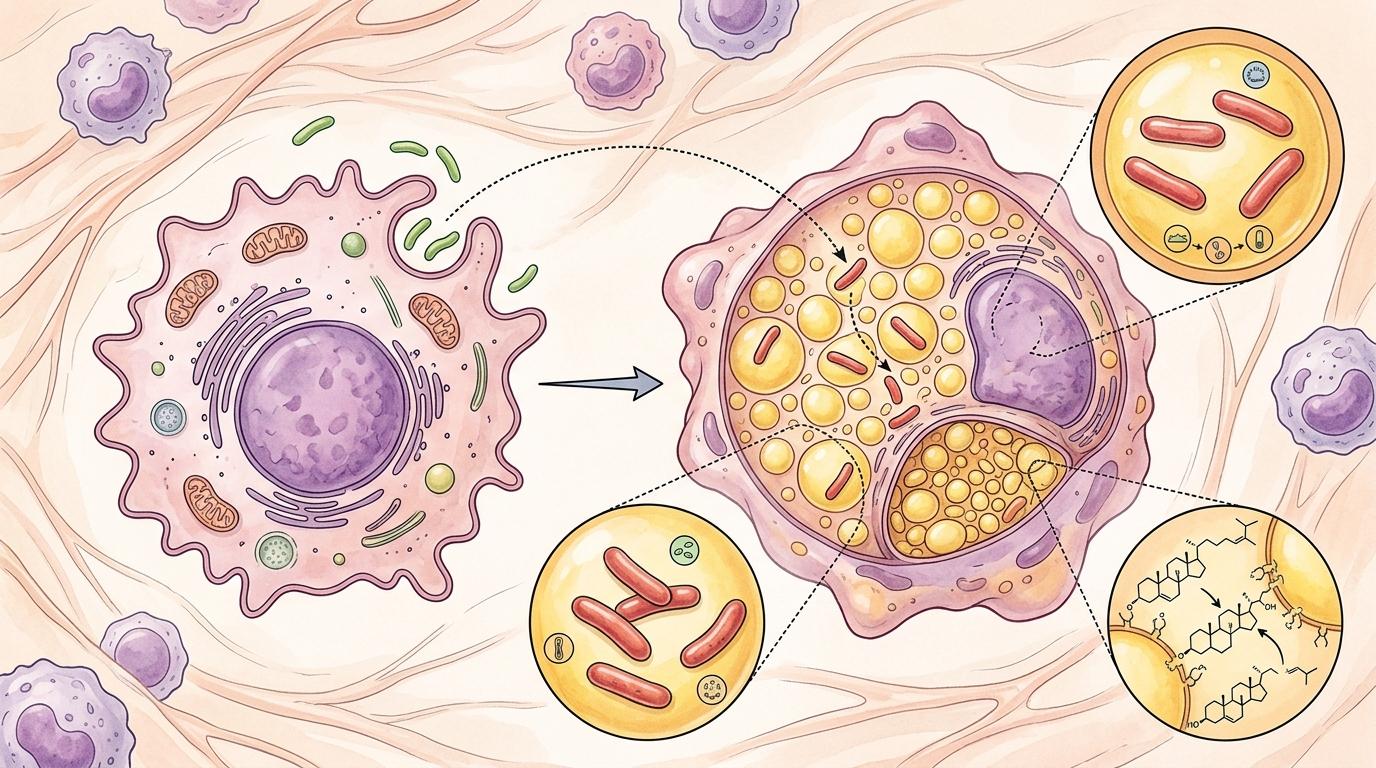
过去十年,科学家们尝试过用肿瘤免疫的思路治疗结核:激活CD4+ T细胞、阻断免疫检查点,但结果都事与愿违——过度激活的免疫细胞会在肺部引发强烈炎症,反而加速肉芽肿坏死,让病菌扩散得更快。这次的研究让人们意识到:问题不在免疫细胞不够强,而在局部免疫环境的“通讯线路”被胆固醇堵死了。
研究团队在小鼠模型里做了一个实验:用药物恢复巨噬细胞的胆固醇代谢,让多余的胆固醇能正常外排。仅仅两周后,肉芽肿里巨噬细胞的MHC II类分子表达量恢复了70%,CD4+ T细胞的激活比例从12%提升到47%,小鼠肺部的病菌载量下降了近90%。更关键的是,这种治疗没有引发过度炎症,因为它只是“疏通”了免疫细胞的协作通道,而不是强行“刺激”免疫反应。
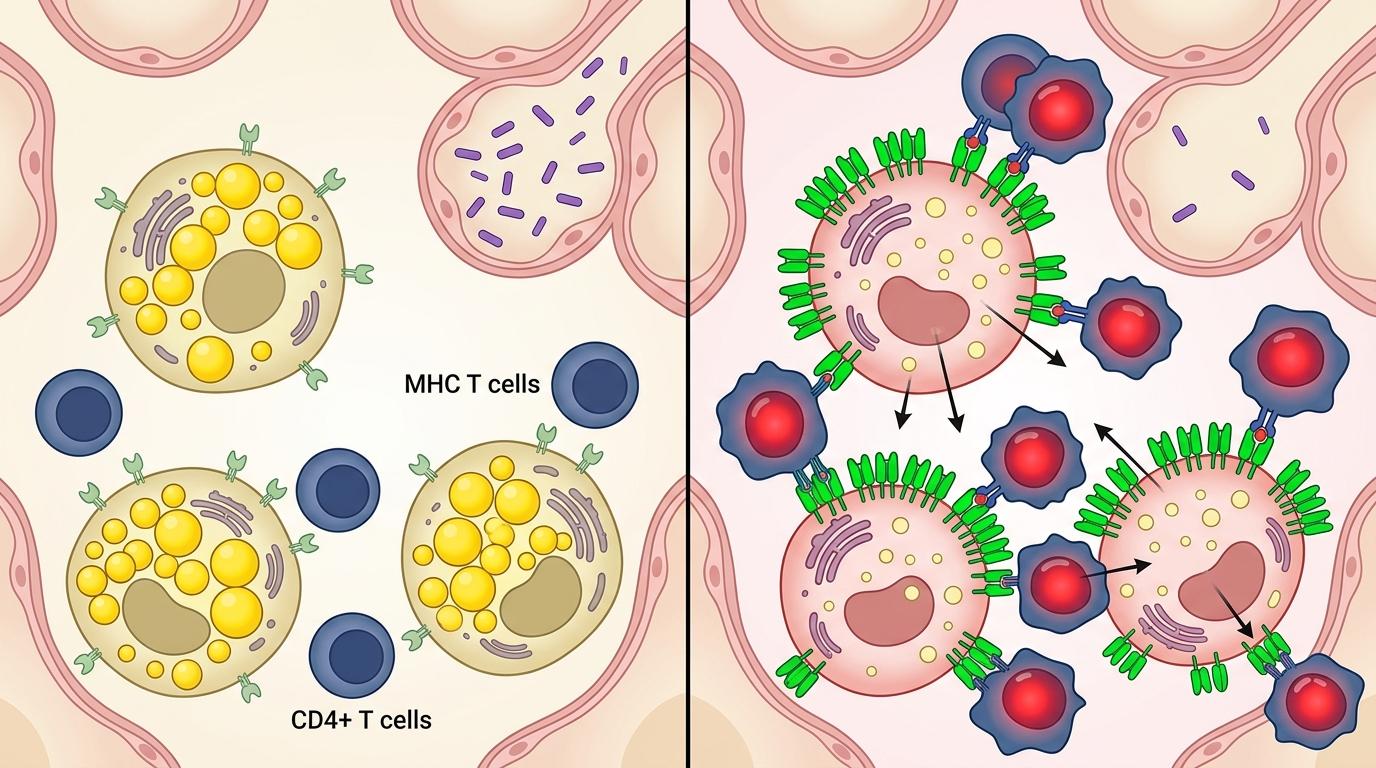
这也解释了为什么他汀类药物——一种常用的降胆固醇药——在临床观察中能辅助治疗结核:它不仅能降低血液里的胆固醇,还能直接作用于肺部巨噬细胞,抑制胆固醇的合成,减少泡沫细胞的形成。不过研究团队也指出,直接使用现有他汀类药物的效果有限,因为它们无法精准靶向肉芽肿里的巨噬细胞,未来需要开发能穿透肉芽肿的靶向药物。
更值得关注的是,这次的研究还揪出了一个关键的调控蛋白——胆固醇25-羟化酶(CH25H)。结核分枝杆菌感染后,巨噬细胞里的CH25H会过度表达,它会把胆固醇转化为25-羟基胆固醇,这种物质会进一步抑制胆固醇外排,同时削弱MHC II类分子的抗原呈递功能。
研究团队用基因编辑技术敲除小鼠巨噬细胞的CH25H基因后,即使感染了结核分枝杆菌,巨噬细胞也不会形成泡沫细胞,肉芽肿里的免疫协同信号能正常传递。这意味着CH25H可以作为一个精准的治疗靶点:只要抑制它的活性,就能从源头阻止胆固醇在巨噬细胞里堆积,恢复免疫细胞的协作能力。
不过这种疗法也有挑战:CH25H是干扰素诱导的蛋白,正常情况下有抗病毒的作用,过度抑制可能会影响人体对其他病毒的抵抗力。如何在结核治疗和维持正常免疫之间找到平衡,是未来需要解决的问题。
当我们谈论结核病时,总把目光放在病菌的抗药性上,却忽略了人体自身的免疫防线可能“卡了壳”。这次的研究让我们看到,慢性感染的核心或许不是免疫细胞不够强,而是免疫微环境的代谢平衡被打破了——就像一个运转不畅的工厂,再多的工人也无法正常生产。
“免疫的本质,是代谢的平衡。”这句话或许能概括这次研究的核心启示。未来的抗结核治疗,可能不再是给免疫细胞“打鸡血”,而是给它们“松绑”:疏通被胆固醇堵住的协作通道,让巨噬细胞和T细胞重新并肩作战。毕竟,最好的防线,从来不是堆起高墙,而是让每一个战士都能顺畅地传递信号、协同御敌。
点击催更,成为大圆镜下一个视频选题!