对抗知识焦虑,从看懂这条开始
App 下载
祖辈饥饿竟能让子孙更长寿?Science揭开跨代遗传新篇章
秀丽隐杆线虫|细胞器|跨代遗传|王萌教授|贝勒医学院|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
秀丽隐杆线虫|细胞器|跨代遗传|王萌教授|贝勒医学院|分子细胞生物学|生命科学
我们从父母那里继承了眼睛的颜色、头发的曲直,这些都清晰地写在DNA的蓝图上。但我们是否想过,祖辈们经历的饥饿、感受过的环境压力,能否也化作一种无形的印记,悄悄传递给下一代?这听起来像是科幻小说,一种超越基因的记忆。然而,科学的边界总是在被不断拓展。一个长期以来被认为是细胞“垃圾回收站”的微小细胞器,正揭示着一个惊人的秘密:我们祖辈的生活经历,或许真的能跨越代际,影响我们的寿命。
2025年9月25日,贝勒医学院的王萌教授团队在顶尖期刊《Science》上发表了一项颠覆性的研究,为这个看似天方夜谭的设想提供了确凿的分子证据。他们的研究主角是一种体长仅1毫米的微小生物——秀丽隐杆线虫。
故事始于一个意外的发现。研究人员通过激活线虫肠道细胞内一种名为LIPL-4的溶酶体脂肪酶,成功使其寿命延长了超过50%。这本身就是一个了不起的成就。但更让团队惊讶的是,当这些长寿线虫与普通线虫繁殖后,它们的子孙——即便体内已不携带任何经过改造的基因——也表现出了明显的长寿特征。这种“长寿福利”甚至可以延续到第四代,第三代后代的寿命依然比普通线虫长18%。

这无疑指向了一种非孟德尔遗传模式。某种“长寿记忆”在没有改变DNA序列的情况下,从亲代传递给了子代。这个神秘的信使究竟是谁?它又是如何完成这场跨越身体与代际的“信息接力”的?
答案隐藏在细胞的表观遗传机制中。如果说DNA是生命的“硬件”,那么表观遗传就是调控硬件如何运行的“软件”。它通过在DNA或其包装蛋白上添加化学“标签”,来决定哪些基因开启,哪些基因关闭。
王萌团队发现,这场跨代遗传大戏的核心,是一种特殊的组蛋白变体——H3.3(在秀丽隐杆线虫中由his-71基因编码)。
整个过程如同一场精心策划的接力赛:
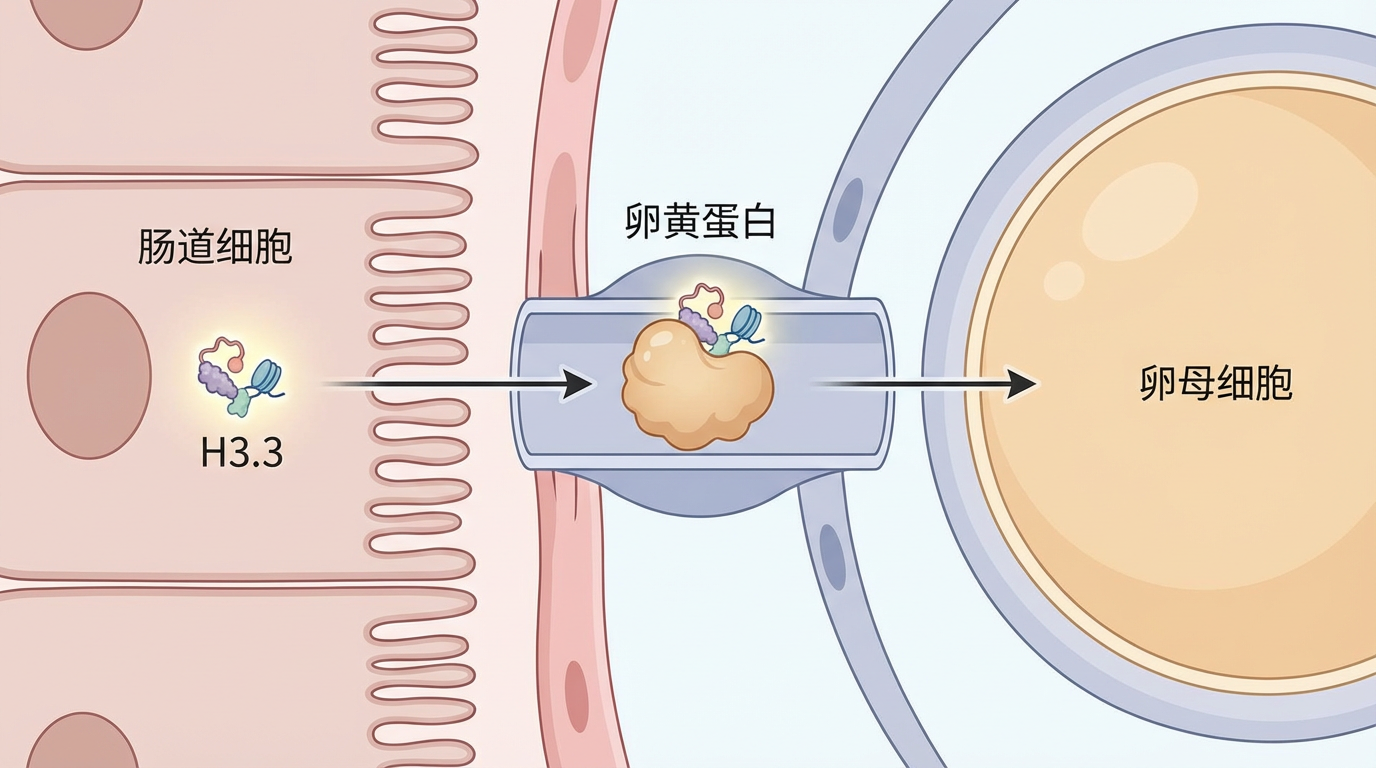
信号触发:当线虫经历饥饿,或其肠道内的溶酶体脂质信号被激活时,肠道细胞会收到“指令”,大量生产H3.3蛋白。此时,H3.3就像一位肩负特殊使命的信使,诞生于身体的一个普通角落(体细胞)。
跨界之旅:这位“信使”面临着一项艰巨的任务——必须从肠道细胞穿越到生殖细胞(卵母细胞)中,才能将信息传递给下一代。研究发现,H3.3巧妙地“搭上”了卵黄蛋白的“顺风车”,通过其特有的运输系统,成功完成了这次从体细胞到生殖细胞的“跨界旅行”。这是对传统细胞生物学边界的一次重大挑战,证明了身体的经验可以物理性地传递给遗传蓝图的守护者。
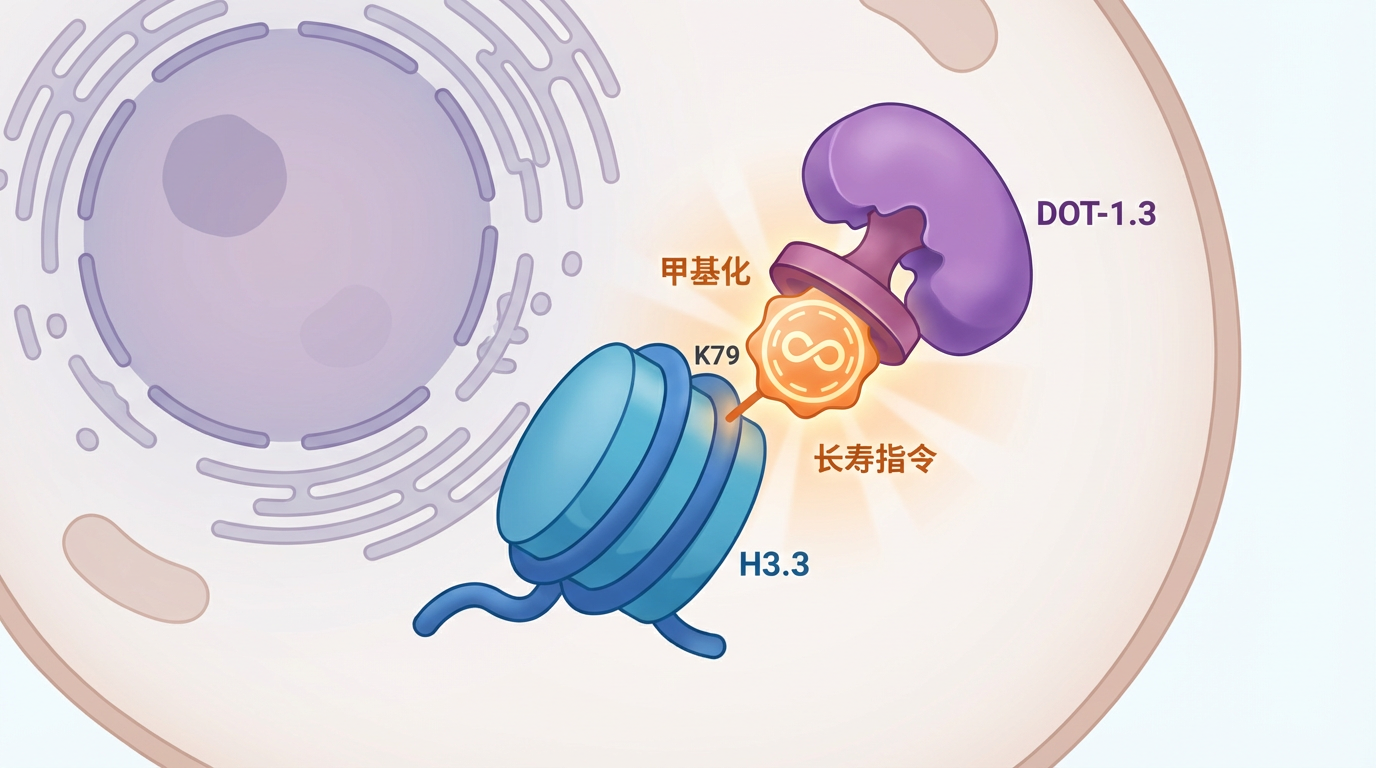
这项研究的意义远不止于解释线虫为何能跨代长寿。它将一个长期被低估的细胞器——溶酶体,从一个被动的“废物处理厂”提升到了一个能够感知环境、并指导跨代遗传的**“代谢信号中枢”**的高度。
无论是饥饿、抑制促进细胞生长的mTOR信号,还是激活感知能量状态的AMPK信号,这些经典的延寿途径,最终都汇入了上述的H3.3表观遗传通路。这表明,生物体进化出了一套精密的系统,能将环境中的生存信息(如食物的丰寡)编码为表观遗传信号,作为一种快速适应策略传递给后代。
这一发现为“获得性遗传”这一古老而充满争议的观点提供了现代分子生物学证据。它完美诠释了环境(Nurture)与遗传(Nature)之间并非割裂,而是通过像H3.3这样的分子信使紧密相连。
当然,从线虫到人类,还有很长的路要走。但考虑到溶酶体、组蛋白H3.3以及相关的信号通路在进化上高度保守,这项发现在人类健康和衰老研究领域激起了巨大的涟漪。
然而,我们仍面临诸多未解之谜:这种表观遗传记忆的稳定性如何?它能持续多少代?在哺乳动物中,由于存在更彻底的表观遗传重编程,这一机制是否依然存在?
王萌团队的研究,如同一束光,照亮了生命遗传中一个幽深而迷人的角落。它告诉我们,生命远比DNA序列所能编码的更为丰富和深刻。我们的细胞里,不仅流淌着祖先的血液,也可能铭刻着他们经历风霜雨雪后留下的无声叮咛。
我们不再仅仅是基因的载体,更是祖辈与环境互动的鲜活记录。每一个生命,都是一个跨越时空的故事,而这个故事的最新篇章,正由我们自己,以及我们所处的这个世界,共同书写。