对抗知识焦虑,从看懂这条开始
App 下载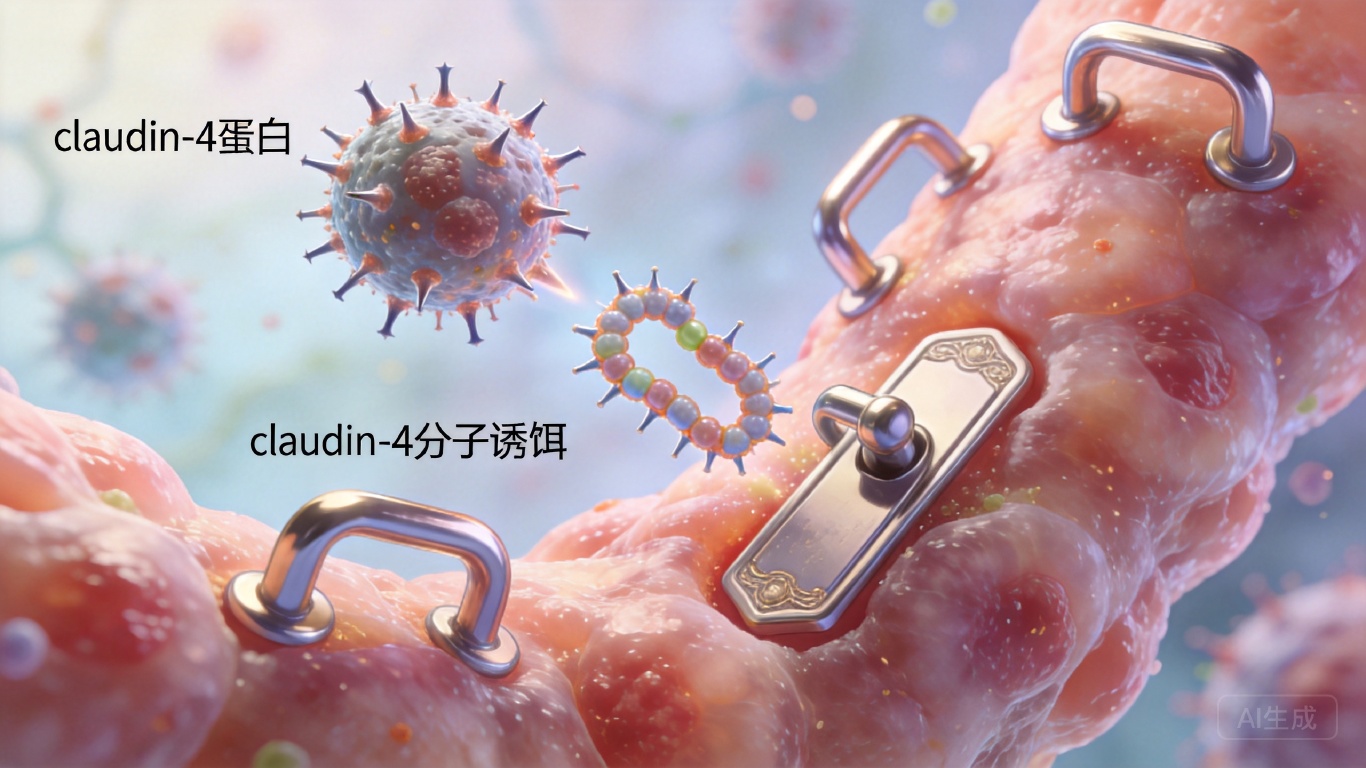
揪出肠癌幕后帮凶的钥匙,还做成了解毒诱饵
约翰霍普金斯大学|分子诱饵|claudin-4|BFT毒素|产毒脆弱拟杆菌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
约翰霍普金斯大学|分子诱饵|claudin-4|BFT毒素|产毒脆弱拟杆菌|肿瘤学|医学健康
全球每年有190万人被确诊结直肠癌,其中近半数会因此离世。这种癌症的背后,藏着一个潜伏在20%健康人肠道里的“隐形杀手”——产毒脆弱拟杆菌。它分泌的BFT毒素能撬开结肠细胞的防线,引发炎症、驱动癌变,可过去17年里,没人知道它到底是怎么“破门而入”的。直到最近,约翰霍普金斯大学的团队在《自然》杂志上公布了答案:毒素要先抓住细胞表面一个叫claudin-4的“门把手”,才能动手破坏。更关键的是,他们顺着这个发现,造出了能“骗走”毒素的分子诱饵,在小鼠身上成功挡住了攻击。
BFT本质是一种金属蛋白酶,它的终极目标是E-钙黏蛋白——这种像“胶水”一样的分子,把结肠上皮细胞牢牢粘在一起,维持着肠道屏障的完整。一旦E-钙黏蛋白被切断,细胞间的连接就会松动,细菌和毒素趁机侵入,炎症反复发生,细胞开始不受控地增殖,癌变的种子就此埋下。
但反常的是,BFT并不直接攻击E-钙黏蛋白。这意味着中间一定有个“接头”,把毒素精准带到目标位置。过去17年里,科学家们猜测过各种信号蛋白,却始终没找到正确答案。直到研究团队用上了全基因组CRISPR筛选:把结肠上皮细胞的基因挨个敲除,看哪个基因缺失后,BFT就失效了。
结果让所有人意外。
不是什么复杂的信号受体,而是claudin-4——一种负责“封死”细胞间缝隙的紧密连接蛋白,过去只被认为是肠道屏障的“砖瓦”,没人想到它会是毒素的“帮凶”。当claudin-4被敲除,BFT完全无法结合细胞,E-钙黏蛋白毫发无损。后续的生物物理实验更直接证明,BFT和claudin-4会形成1:1的紧密复合物,这是二者绑定的首个物理证据。
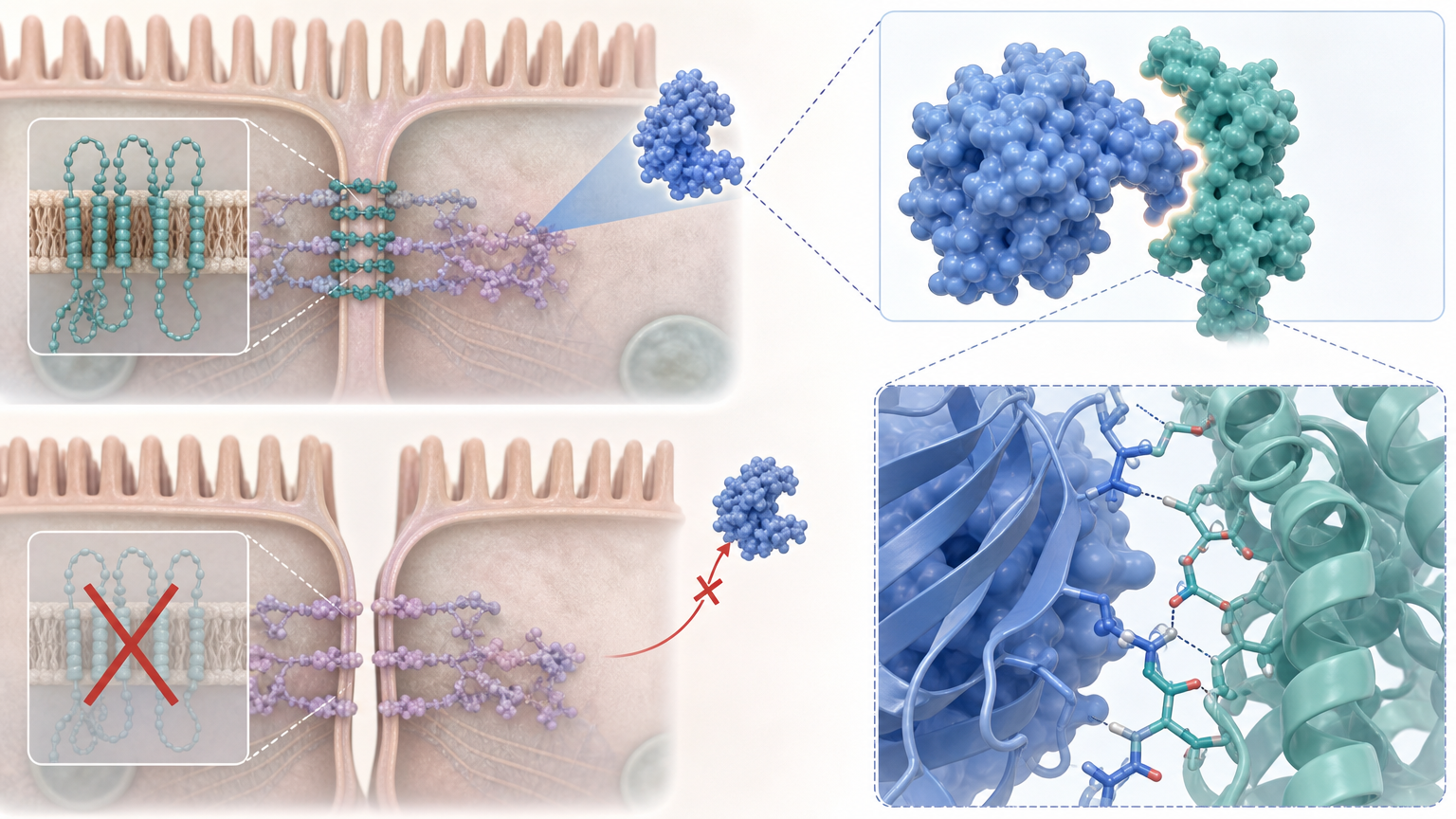
既然claudin-4是毒素进门的唯一“把手”,那只要提前把这个“把手”的复制品扔到肠道里,是不是就能骗走毒素?
研究团队正是这么做的。他们设计了一种可溶性的claudin-4“分子诱饵”——它和细胞表面的真claudin-4有着一模一样的BFT结合位点,却不附着在细胞上,而是游离在肠道里。当BFT毒素被分泌出来,会优先和这些“假把手”结合,自然就碰不到真正的结肠细胞了。
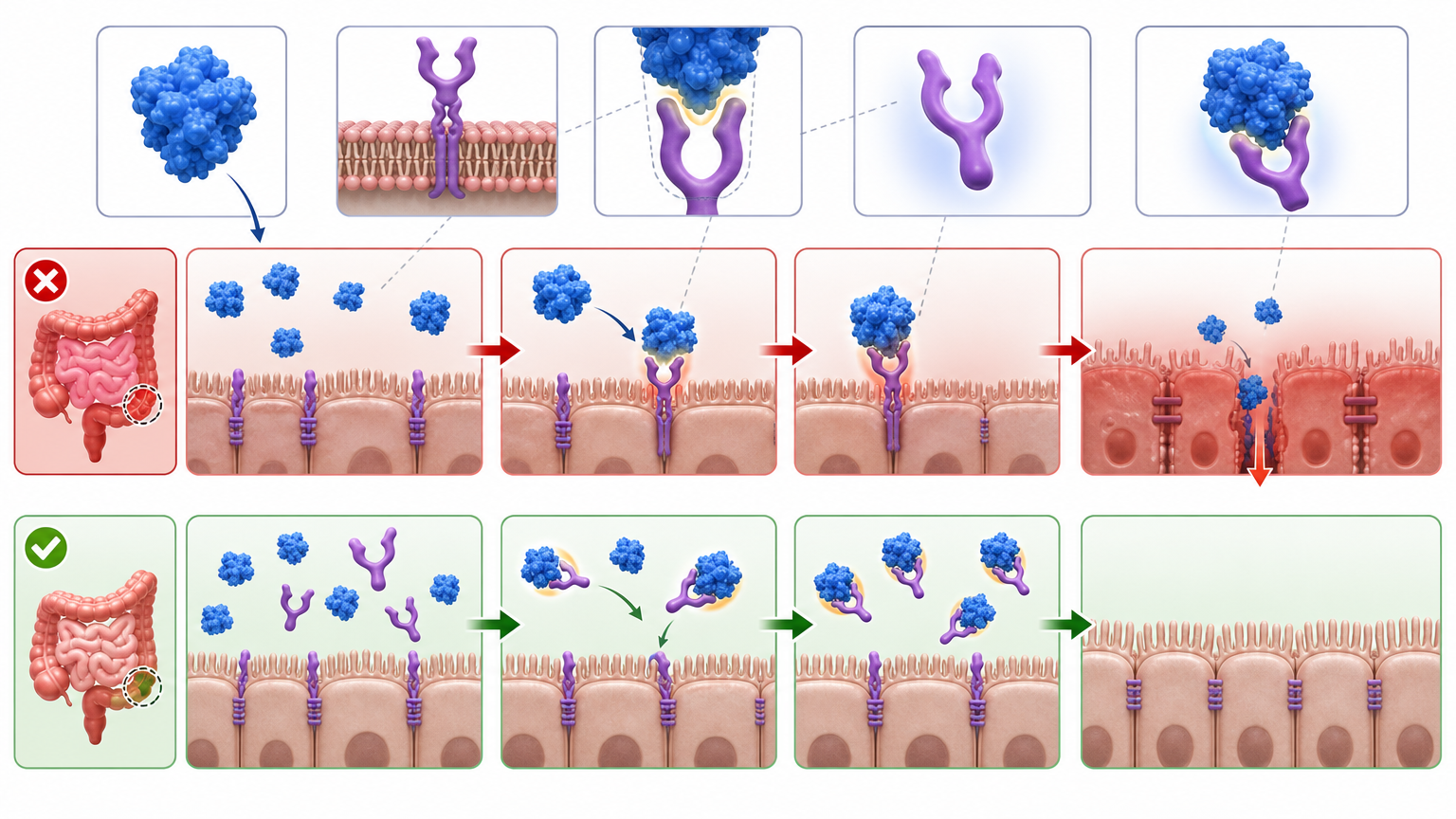
在小鼠实验里,这个策略效果显著:注射了BFT的小鼠,结肠上皮会出现明显的细胞脱落和水肿,而同时注射分子诱饵的小鼠,肠道屏障几乎完好无损,E-钙黏蛋白也没被切割。
这个思路的妙处在于,它不直接杀灭细菌,只是切断了毒素的“作案路径”——既避免了抗生素可能带来的耐药性问题,又精准针对致癌的关键环节。研究人员已经提出,可以把这个分子诱饵优化成小分子药物或者生物制剂,提升它在体内的稳定性和作用时间,为临床转化铺路。
不过这项研究还留下了不少待解的谜题。
首先,BFT和claudin-4结合的精确三维结构还没被解析出来。虽然AlphaFold等AI工具尝试预测,但这种膜蛋白复合物的结合细节太过复杂,目前的模型还无法完全还原。只有拿到高分辨率的结构,才能设计出更精准的阻断分子。
其次,claudin-4的“备胎”claudin-3也能部分结合BFT,只是效率更低。如果长期使用针对claudin-4的诱饵,会不会让毒素逐渐适应,转而更多依赖claudin-3?这需要进一步的实验验证。
最后,BFT是怎么穿越肠道表面的黏液层,精准找到结肠上皮细胞的?毕竟肠道里充满了各种微生物和食物残渣,毒素要找到“门把手”,本身就需要一套特殊的导航机制。
从2009年发现BFT的致癌作用,到2026年找到它的“门把手”,这17年的等待不仅填补了认知空白,更给结直肠癌的防治打开了新的窗口。过去我们对付肠道致病菌,要么用抗生素“通杀”,要么直接中和毒素,但这次的思路更巧妙:从毒素的“作案逻辑”入手,精准打断它的攻击链条。
这也让我们意识到,肠道菌群和癌症的关系,远比想象中复杂——那些看似无害的共生菌,可能藏着精密的致病机制;那些被当成“结构件”的蛋白,可能是打开疾病大门的钥匙。
找到钥匙,就能做出锁。 未来,这种“分子诱饵”的思路或许不仅能用于结直肠癌,还能拓展到更多由细菌毒素介导的疾病中,为精准医疗提供新的方向。