对抗知识焦虑,从看懂这条开始
App 下载
T细胞耗竭真相:不是累瘫,是细胞垃圾堵死了
Goldrath团队|蛋白酶体|E3泛素连接酶|T细胞耗竭|CD8+T细胞|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
Goldrath团队|蛋白酶体|E3泛素连接酶|T细胞耗竭|CD8+T细胞|肿瘤学|医学健康
当我们的身体对抗癌症时,最精锐的免疫战士CD8+T细胞会悄悄“罢工”——它们明明还活着,却失去了杀敌的力气,这就是让免疫疗法屡屡折戟的“T细胞耗竭”。过去十年,科学家们一直以为是表观遗传或代谢紊乱拖垮了这些战士,直到加州大学圣地亚哥分校的Goldrath团队,在2026年4月的《Cell》杂志上捅破了一层窗户纸:耗竭的T细胞,其实是被自己产生的“垃圾”埋了。
你可以把T细胞想象成一间高速运转的工厂,每天要合成大量杀敌用的蛋白武器。正常情况下,工厂里有一群“质检员”——E3泛素连接酶,它们会给错误折叠、损坏的蛋白贴上“销毁”标签,再由蛋白酶体这个“垃圾处理厂”清理干净。
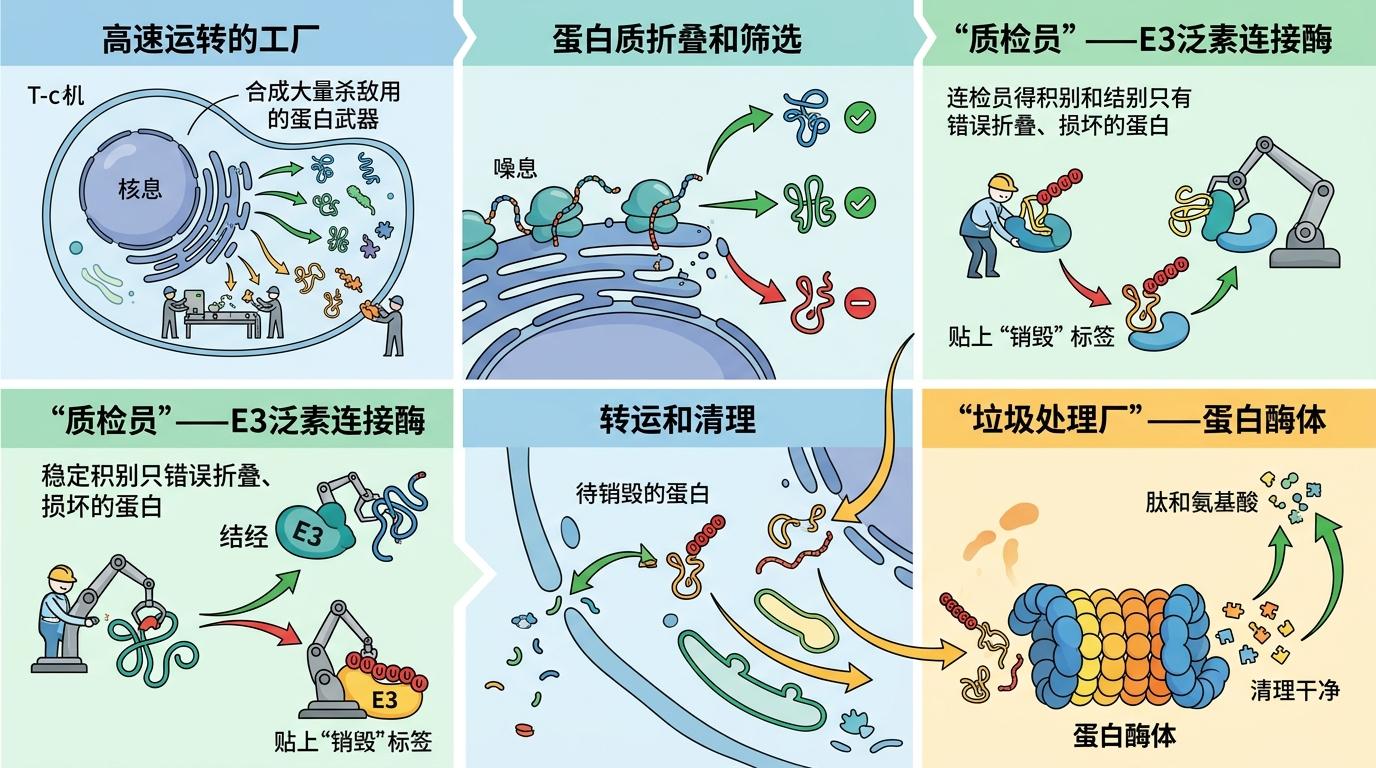
但Goldrath团队通过高精度蛋白质组学分析发现,耗竭的T细胞里,NEURL3、RNF149和WSB1这三种关键“质检员”的数量骤降了。更要命的是,T细胞的蛋白合成速度反而在加快——一边是次品没人标记,一边是新货疯狂生产,细胞内很快堆满了未折叠的错误蛋白,像工厂车间里堆成山的不合格零件。
这些“细胞垃圾”会引发内质网应激,干扰线粒体的能量供应,最终让T细胞失去增殖和分泌细胞因子的能力,彻底沦为“躺平”的废兵。
为了证实“质检员缺失”是耗竭的核心原因,团队做了两组对照实验:
在肿瘤浸润的耗竭T细胞中,通过基因工程过表达NEURL3、RNF149或WSB1,结果发现细胞内的错误蛋白被快速清除,T细胞重新恢复了干细胞样特性——能自我更新,能分泌更多干扰素-γ,在小鼠肿瘤模型中,甚至能显著抑制肿瘤生长。
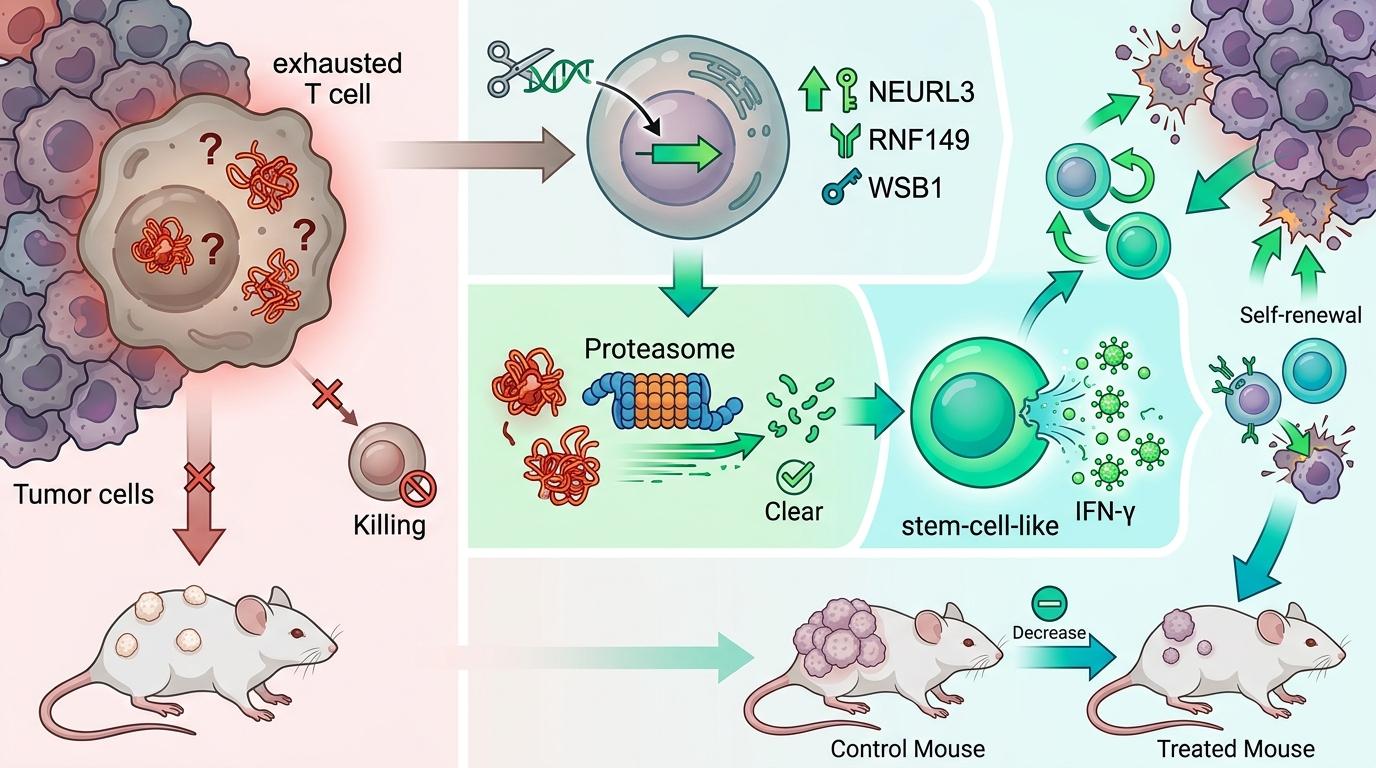
反过来,敲除正常T细胞中的这三种E3连接酶,这些原本骁勇的战士会迅速陷入耗竭,对抗肿瘤和急性感染的能力大幅下降。
更让人兴奋的是联合疗法的效果:给过表达E3连接酶的T细胞配上PD-1抑制剂,小鼠体内的肿瘤被抑制的程度,远超过单一疗法。这意味着,修复蛋白质质量管理系统,能让免疫疗法的效果翻倍。
过去,研究T细胞耗竭的重点一直放在表观遗传修饰、代谢重编程和免疫检查点上,蛋白质稳态这个基础机制被长期忽略。但Goldrath的研究让人们意识到,细胞最基础的“家务事”,恰恰是决定免疫战士生死的关键。
有意思的是,这种“蛋白垃圾堆积”的机制,和阿尔茨海默病、帕金森病等神经退行性疾病的病理高度相似——都是因为错误蛋白无法被及时清除,最终导致细胞功能崩溃。这也意味着,免疫学家和神经科学家或许能从彼此的研究中找到新的突破口。
不过,这项研究也有局限:目前的实验都在小鼠模型中完成,人类肿瘤中的T细胞是否存在完全相同的机制,还需要进一步验证。而且,如何精准调控E3连接酶的表达,避免过度激活引发自身免疫,也是未来临床转化要解决的难题。
当我们谈论癌症免疫疗法时,总在追求更强大的“杀敌武器”,却常常忘了,让战士们保持“内务整洁”同样重要。Goldrath团队的研究,就像给免疫疗法打开了一扇新的窗户——原来不用给T细胞装更锋利的武器,只要帮它们把车间里的垃圾清干净,就能让这些战士重新焕发生机。
细胞的战斗力,始于对自身的精准管理。 未来,或许我们能开发出专门调控蛋白质稳态的药物,让每一个T细胞都能在肿瘤微环境里,保持高效、清洁的运转状态,成为真正打不垮的抗癌战士。