对抗知识焦虑,从看懂这条开始
App 下载
清除脑内斑块十年,疗效不及多记半个词
考科蓝报告|脑水肿|认知测试|抗淀粉样蛋白单抗|阿尔茨海默病|神经退行性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
考科蓝报告|脑水肿|认知测试|抗淀粉样蛋白单抗|阿尔茨海默病|神经退行性疾病|医学健康
当一位阿尔茨海默病患者的家属,在半年里陪着老人完成8次静脉输液、4次脑部MRI后,他们最想听到的是“他的记忆力好多了”。但考科蓝2026年的最新报告,给这个期待浇了一盆冷水:过去十年投入数百亿美元研发的抗淀粉样蛋白单抗药物,18个月里能给患者带来的认知改善,平均只有0.85分——在满分70分的认知测试里,这还不到多记住半个词的程度。更让人揪心的是,每10个接受治疗的患者里,就有1个会出现脑水肿,还有3%可能伴随头痛、意识模糊甚至癫痫。这场瞄准“大脑垃圾”的豪赌,到底输在了哪里?
1984年,科学家首次在阿尔茨海默病患者脑内发现淀粉样蛋白斑块,一条看似无懈可击的逻辑链就此形成:斑块堆积→神经元死亡→记忆丧失。就像疏通下水道能解决堵塞,只要把这些“脑内垃圾”清走,大脑就能恢复正常。
制药公司顺着这条思路,培育出了精准靶向淀粉样蛋白的单克隆抗体——你可以把它理解成只认一种锁的钥匙,注射进体内后,会穿过血脑屏障,死死咬住淀粉样蛋白,再召唤免疫细胞把它吞噬分解。PET扫描的结果曾让所有人兴奋:治疗前患者脑内斑块密布,治疗后影像图几乎干干净净。
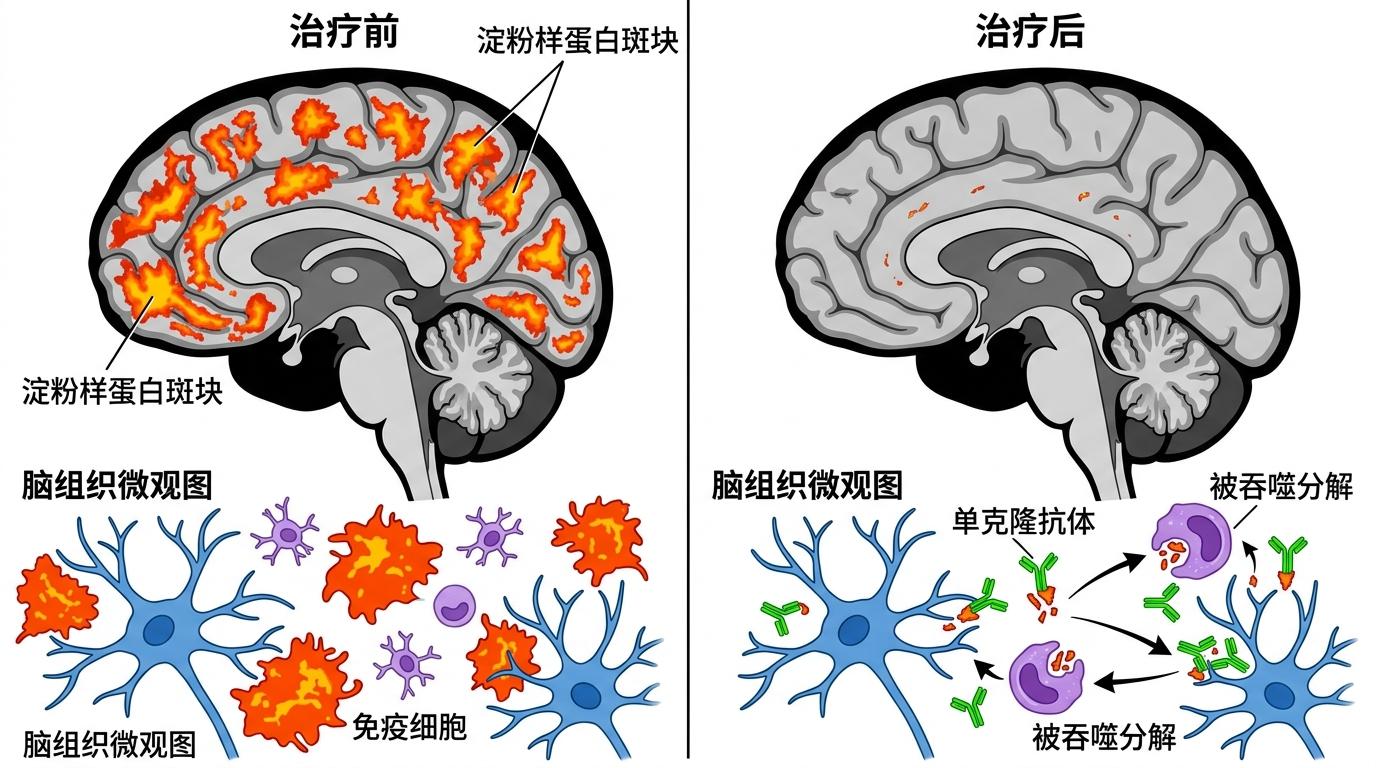
但现实给了理论一记响亮的耳光。考科蓝的报告整合了17项临床试验、2万多名患者的数据后发现,这些能高效清除斑块的抗体,对认知功能的改善连“临床可感知”的门槛都没摸到。轻度认知障碍患者的认知测试,至少要改善2到3分才能让家属察觉变化,而0.85分的提升,连这个门槛的一半都达不到。
更耐人寻味的是,这0.85分的“疗效”,可能还掺着水分。这类药物的副作用太过明显——只要做MRI发现脑水肿,患者和家属立刻就会知道打的是真药而非安慰剂,这种“功能性破盲”会悄悄影响评估:当家属知道亲人在用“最前沿的新药”,会不自觉把老人偶尔的状态波动当成疗效,比如“他今天好像认出我了”,这些主观判断最终会被编码成数据里的“改善”。有学者推测,真实的疗效可能比报告里的数字还要小,甚至趋近于零。
而副作用的风险却真实得刺眼。淀粉样蛋白不仅会形成斑块,还会像水垢一样附着在脑血管壁上。当抗体把这些“水垢”剥离时,血管壁可能会被撕出裂口,导致脑水肿或微出血。数据显示,用药组出现脑水肿的概率是安慰剂组的10倍,出现有症状脑水肿的风险更是飙升52倍。
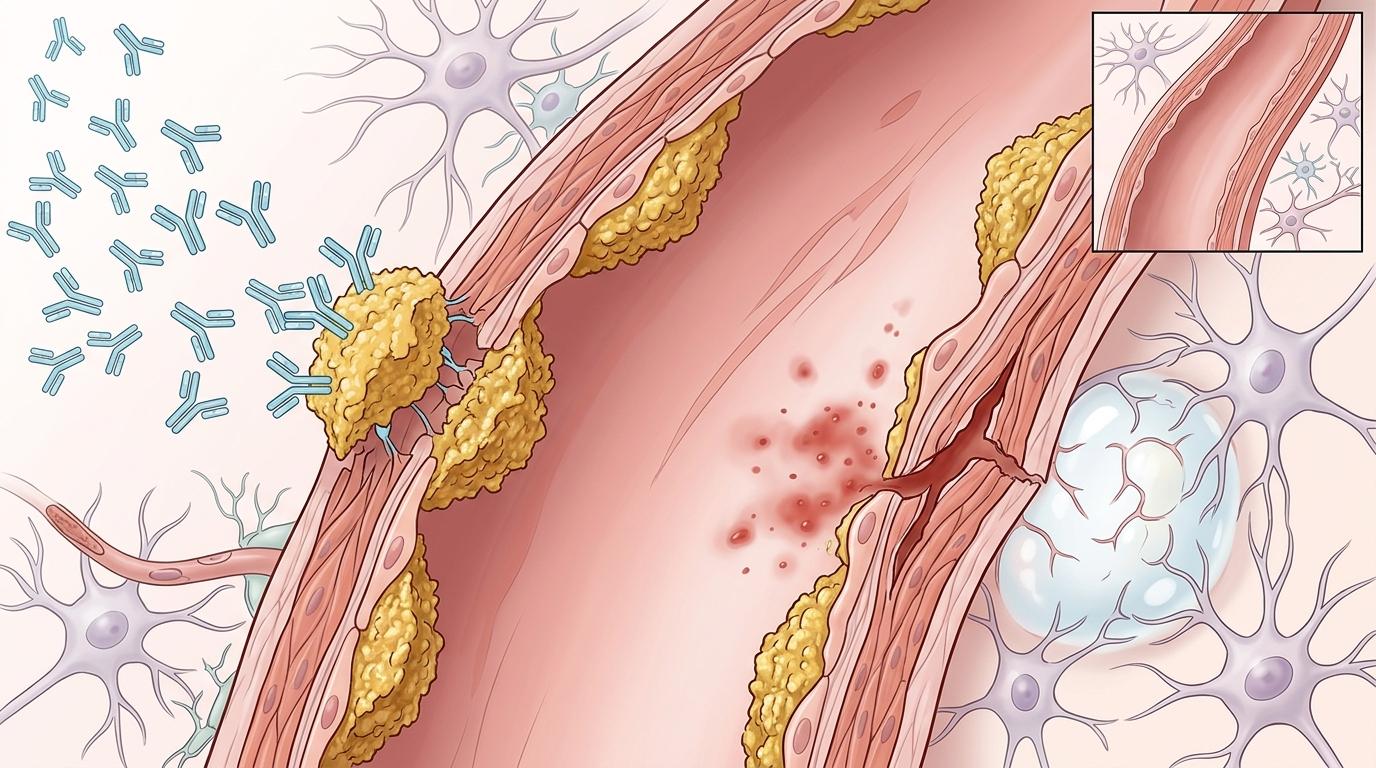
就算抛开副作用不谈,这类药物的性价比也低得惊人。以已获批的药物为例,年治疗费用超过2.6万美元,还不算频繁输液和MRI监测的成本。英国国家卫生与临床优化研究所直接拒绝将其纳入公费医疗,理由很直白:“疗效不足以证明成本的合理性。”
考科蓝的报告发布后,也有学者提出质疑:把不同机制的新旧药物混在一起分析,会稀释新药的效果。比如二代药物lecanemab和donanemab,确实能让认知衰退减缓27%到35%,但这种“减缓”依然是统计学上的意义,患者和家属很难在生活中切实感受到。
更关键的是,这场围绕淀粉样蛋白的三十年探索,可能从一开始就找错了核心。越来越多的研究显示,淀粉样蛋白斑块可能不是病因,而是结果——它或许是大脑应对神经炎症、代谢紊乱等问题时产生的“副产品”。就像火灾后的灰烬,扫掉灰烬并不能扑灭真正的火源。
现在,科学界开始把目光转向更复杂的病理机制:tau蛋白的异常磷酸化、神经炎症的恶性循环、脑内的胰岛素抵抗……甚至有学者提出,阿尔茨海默病更像一种“脑部代谢病”,需要从调控能量代谢、修复神经突触等多个角度入手。一些多靶点联合治疗的临床试验已经启动,比如同时靶向淀粉样蛋白和tau蛋白,或者结合抗炎药物,试图打破单一靶点的局限。
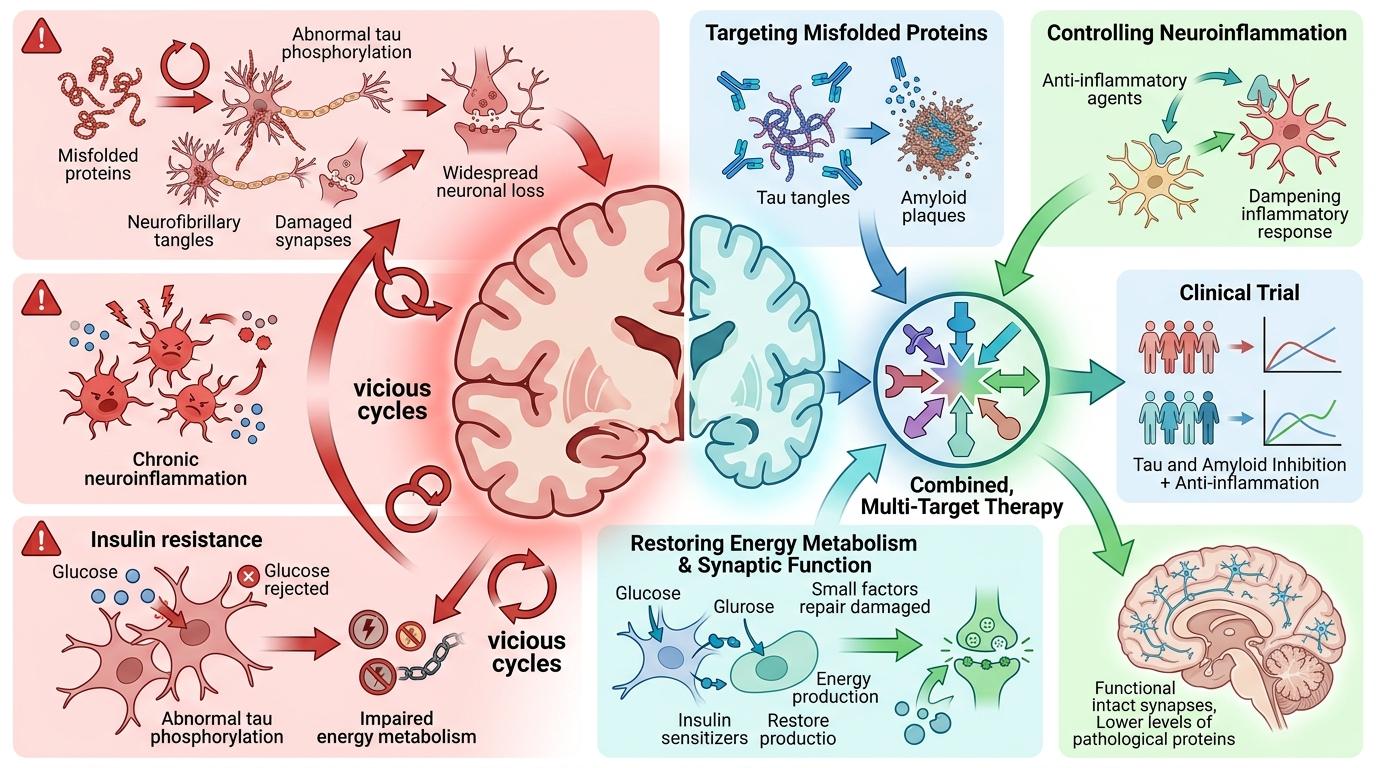
对于那些正在照顾阿尔茨海默病患者的家庭来说,这份报告不会改变他们明天的日常:帮老人穿好衣服,提醒他吃早饭,在他第三千次问“今天星期几”时耐心回答。但它给科学界敲响了警钟——阿尔茨海默病不是一个简单的“垃圾清理”问题,而是一场涉及神经、免疫、代谢的复杂战役。
靶点单一的时代,该结束了。 未来的治疗或许不会有“神药”,但会有更精准的策略:通过生物标志物早筛,在患者出现症状前就干预;根据不同的病理亚型,定制个性化的联合治疗方案;甚至通过生活方式干预,从源头降低发病风险。这场和遗忘的战争,才刚刚开始。