
9 天前

9 天前
想象一下:一款治疗肺纤维化的新药,从靶点发现到候选药物出炉,只用了18个月——而传统路径需要3到6年。这不是科幻,是AI制药公司Insilico Medicine已经完成的现实。就在2026年春天,千亿市值的制药巨头BMS宣布了今年第三笔AI合作,目标直指新药研发里最顽固的痛点:动辄十年的周期、26亿美元的成本,以及不足10%的成功率。为什么这些手握海量资源的制药大厂,突然集体扑向AI?答案藏在那些被数据重新定义的研发流程里。
你可以把传统药物研发比作蒙着眼睛找钥匙:在数百万个化合物里逐个试错,靠反复实验碰运气找到能和疾病靶点结合的分子。而AI做的,是给你一张精准的地图——通过分析基因组、蛋白质组、临床数据等海量信息,直接定位最有潜力的靶点,甚至从零生成符合要求的分子结构。
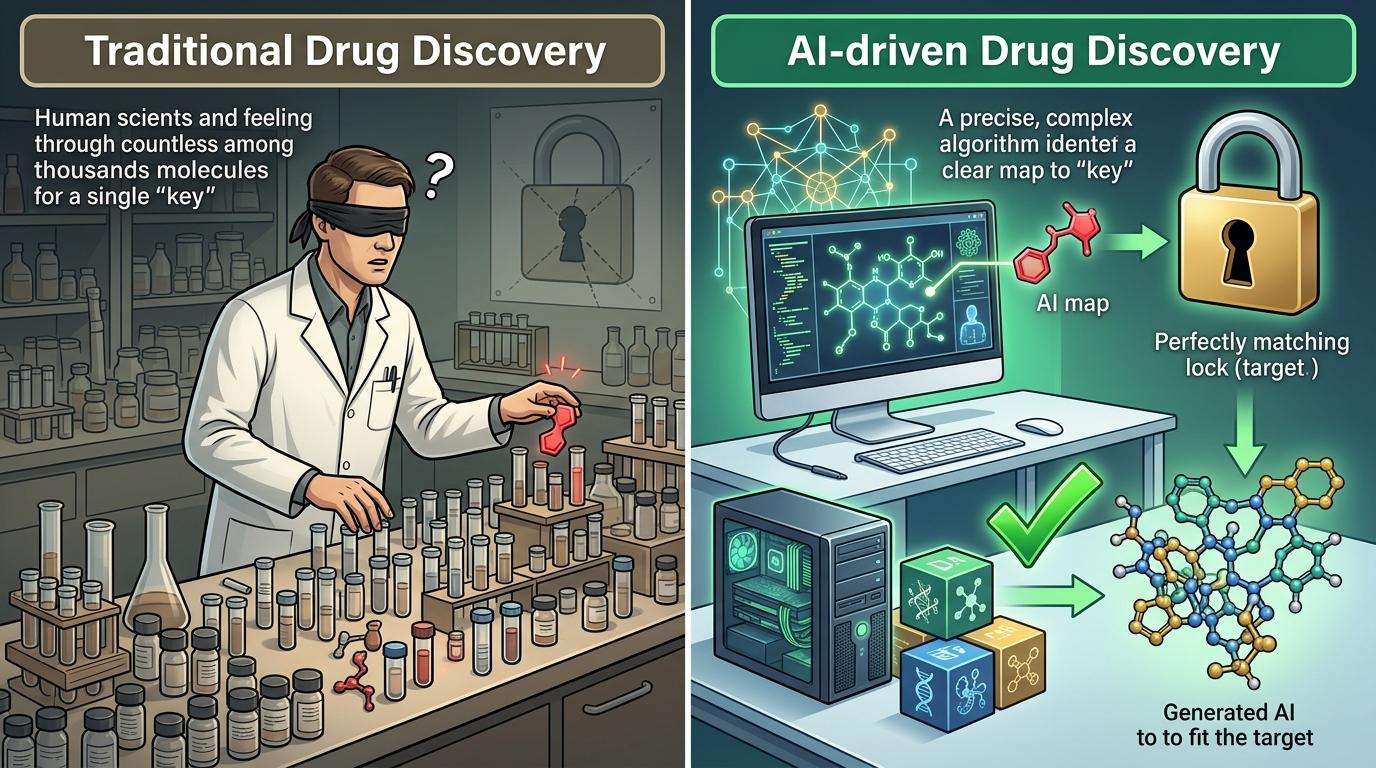
AlphaFold系列模型就是最好的例子。它能精准预测蛋白质三维结构,破解了大量曾被认为「不可药物化」的蛋白难题,让靶点筛选的效率提升了一个数量级。Insilico Medicine的肺纤维化新药就是明证:AI从多组学数据里揪出了全新靶点TNIK,再用生成模型设计出针对性分子,整个过程比传统方法快了一半还多。
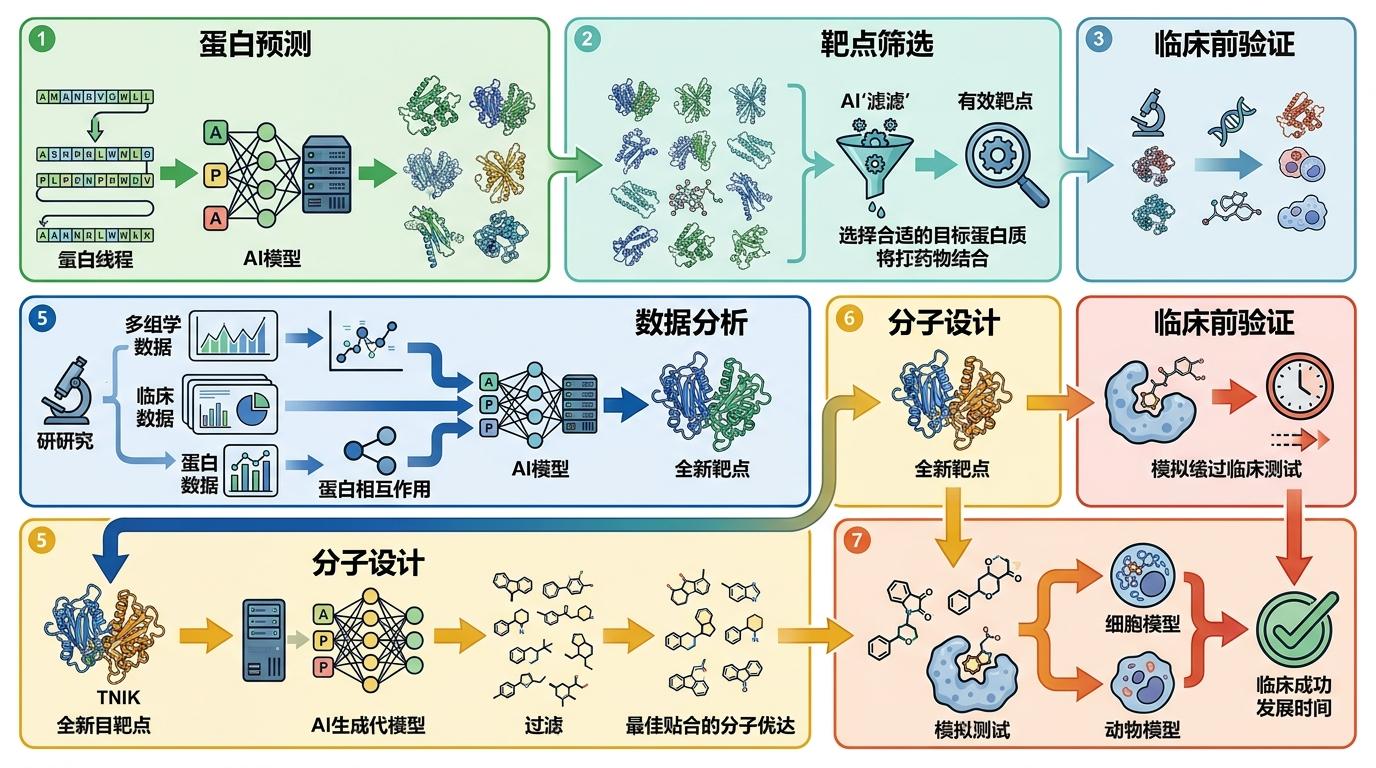
但真实的机制比这更精确:AI不仅能找靶点,还能提前预测药物的毒性、代谢路径,把那些可能在临床试验阶段失败的候选者提前筛掉。有数据显示,AI辅助的毒性预测准确率能达到95%,把临床阶段的失败率降低6倍。这相当于在研发的起跑线上就砍掉了大部分无用功。
如果说药物发现是「找钥匙」,那临床试验就是「开门」——这是新药研发中成本最高、耗时最长、失败率最高的环节,传统临床试验平均要花6到7年,成本占总研发费用的70%以上。AI在这里的角色,是一把能精准调整的「隐形手术刀」。
最直观的变化是患者招募。传统方式靠人工筛选电子病历,匹配一个合适的患者可能要几周;而AI用自然语言处理技术分析病历,能在几天内完成匹配,准确率超过90%,招募周期直接缩短65%。更关键的是临床试验设计的革新:AI能基于真实世界数据优化入组标准,比如针对非小细胞肺癌的试验,放宽某些实验室指标限制后,合格患者数量翻倍,却不影响试验的安全性和疗效。
还有更激进的尝试:数字孪生技术。它能给每个患者建一个虚拟模型,模拟他们对药物的反应,甚至生成「合成对照组」——不用再找大量健康人参与试验,靠虚拟数据就能完成对照分析。这不仅能降低伦理争议,还能把临床试验的成本降低40%,周期缩短30%到50%。
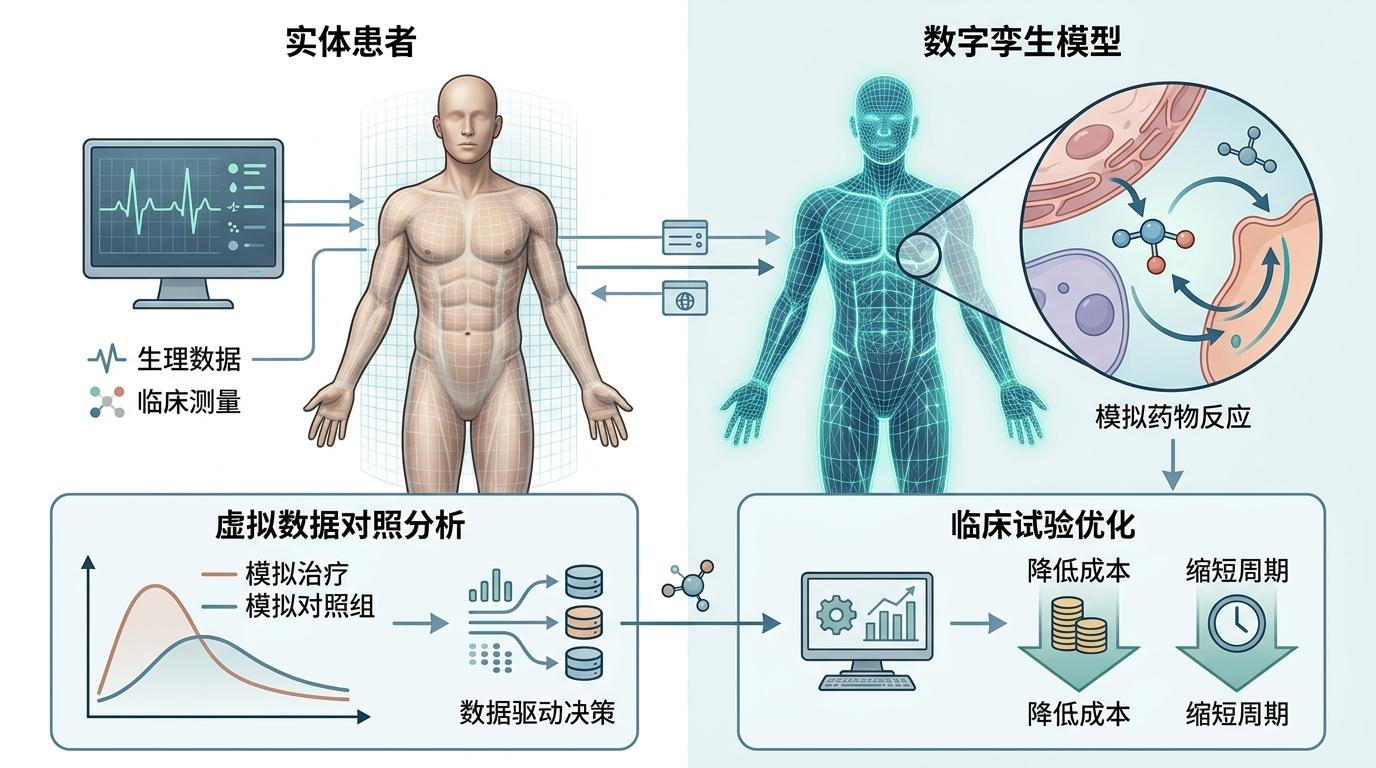
不过这些改变也有局限:AI模型高度依赖高质量数据,如果训练数据有偏差,比如缺乏少数族裔患者的数据,就可能导致试验结果不具代表性。而且目前AI在临床试验中的应用还集中在设计和招募阶段,对试验执行的优化效果还需要更多验证。
当我们为AI的效率欢呼时,不能忽视它眼前的几道坎。
首先是「黑箱」问题。复杂的深度学习模型能给出精准预测,但没人能说清它是怎么得出这个结论的——这让临床医生和监管机构很难信任它的决策。比如AI预测某个化合物有效,但无法解释它作用于哪个蛋白位点,医生就不敢贸然用于临床。监管机构也要求AI模型必须具备可解释性,否则难以通过审批。
其次是数据壁垒。AI需要海量高质量数据,但医疗数据分散在不同医院、药企和研究机构里,缺乏共享机制。很多关键数据被当作商业秘密锁起来,导致AI模型只能在局部数据上训练,泛化能力大打折扣。而且数据质量参差不齐,缺失、偏差的问题普遍存在,直接影响AI的准确性。
最后是人才缺口。AI制药需要既懂生物学、药理学,又懂AI算法的复合型人才,但目前这类人才极度匮乏。药企里的AI团队大多是计算机背景,对生物医学知识一知半解;而医学专家又不懂AI技术,两者之间的鸿沟很难跨越。
当BMS这样的巨头一年之内连签三笔AI合作时,我们看到的不只是商业布局,更是整个制药行业的转向——从依赖科学家的经验和运气,转向依赖数据和算法的精准。未来十年,AI或许不能完全解决新药研发的所有问题,但它一定会把「十年磨一药」的漫长等待,压缩到普通人能感知的时间里。
「效率的革命,最终是生命的革命。」这不是一句空话:当新药研发的周期从十年缩短到两年,那些在病床前等待的患者,就能多一分活下去的希望。而我们要做的,是在追求效率的同时,守住数据公平、模型透明的底线,让AI真正成为惠及所有人的工具。
点击充电,成为大圆镜下一个视频选题!