
1 个月前

1 个月前
你体内每个细胞里,都藏着数百万个首尾相连的“环形RNA”——一种比线性RNA稳定10倍以上的闭合分子。过去10年,科学家一直默认它们是“微RNA海绵”,靠吸附小RNA间接调控基因。但中科院生物物理所薛愿超团队的新研究,推翻了这个主流假设:他们找到11万7千多组环形RNA和靶标RNA的直接绑定关系,其中大部分环形RNA根本不需要微RNA帮忙,就能直接掐断蛋白合成。这到底是怎么做到的?
要理解这个反转,得先把细胞里的蛋白合成流程拆成日常场景:细胞核里的DNA转录出线性mRNA,像带着生产图纸的快递盒,要被送到细胞质里的“核糖体工厂”翻译成蛋白。过去认为环形RNA是“快递盒小偷”——靠吸附微RNA这种“门禁卡”,让快递盒进不了工厂。
但薛愿超团队用RIC-seq技术(一种能在活细胞里捕捉RNA空间互动的测序方法)画了张全基因组的环形RNA互动地图,才发现真相完全不同:83%的靶标mRNA会被多个环形RNA直接绑定,就像快递盒被好几只手拽住。以高丰度的CDR1as为例,它能和上百个mRNA的特定序列精准配对,像钥匙插进锁孔一样紧密。
更关键的是,他们在敲除了AGO2和DICER(微RNA调控的核心蛋白)的细胞里做实验,环形RNA的抑制效果丝毫没减弱。这就实锤了:环形RNA根本不需要“借刀杀人”,它自己就能完成对蛋白合成的阻断。
那环形RNA是怎么让mRNA没法翻译成蛋白的?答案藏在细胞质里的无膜颗粒——P-body里。你可以把P-body理解成细胞里的“待处理快递站”,这里堆满了暂时不被翻译的mRNA,要么被储存,要么被降解。
薛愿超团队开发的GRIC-seq技术(专门捕捉颗粒内RNA互动的升级版测序),终于拍到了实锤:环形RNA会通过碱基配对,把靶标mRNA“拖拽”进P-body这个小黑屋。一旦进去,mRNA就被物理隔离,再也碰不到核糖体工厂。
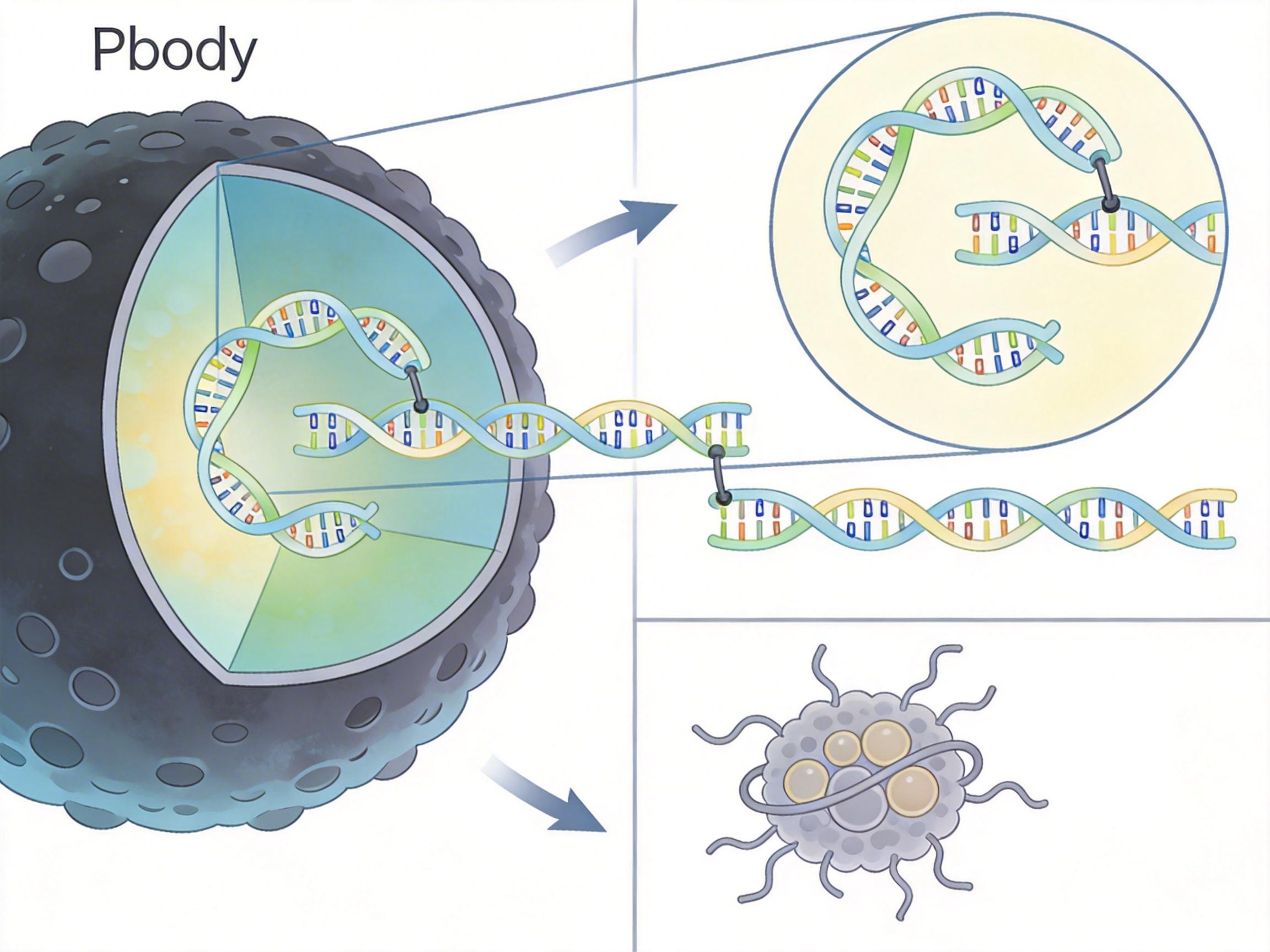
这个过程的精准度高得惊人:只要破坏环形RNA上的配对序列,或者把P-body的核心蛋白DDX6敲除,mRNA就能立刻从小黑屋里跑出来,蛋白合成效率直接回升1.6倍以上。而且只有完整的环形RNA能做到这点——线性的“残次品”连小黑屋的门都摸不到。
说句题外话,这就像你网购的快递被快递员直接送到了小区的暂存柜,还把柜门焊死了——不是快递丢了,就是不让你拿到。
这张11万条数据的互动地图,还藏着更重要的信息:环形RNA和mRNA的绑定位点附近,致病性变异的数量是随机区域的2.3倍。也就是说,这些绑定位点一旦出问题,很可能直接引发疾病。
比如在神经退行性疾病患者的脑组织里,CDR1as的结合位点常常出现突变,导致本该被隔离的GRIN2B mRNA(一种和突触功能相关的基因)大量翻译成蛋白,最终干扰神经元的正常信号传递。而在肿瘤细胞中,有些环形RNA的表达量异常升高,把抑制肿瘤的蛋白mRNA锁进P-body,相当于给癌细胞开了绿灯。
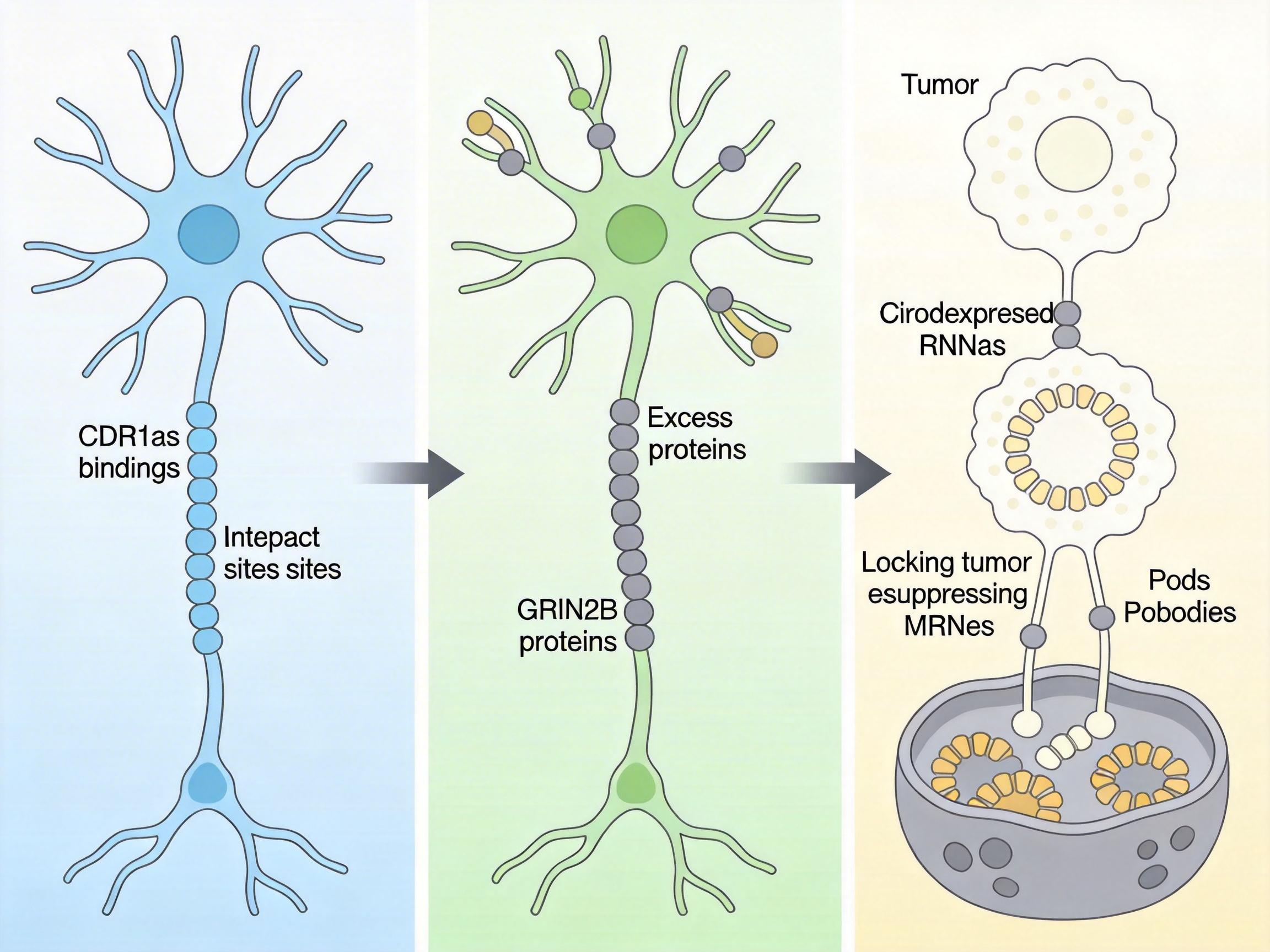
更值得关注的是,这个发现给药物研发指了条新路子:过去我们总盯着蛋白靶点,现在可以尝试设计能精准阻断环形RNA和mRNA配对的小核酸分子,把被锁在小黑屋里的“抑癌快递”放出来。
从被当作“转录垃圾”,到被认为是“微RNA海绵”,再到现在被发现是直接操控蛋白合成的“调控者”,环形RNA的身份用了20年才被慢慢看清。我们对细胞内的RNA调控网络的认知,就像在拼一幅永远缺块的拼图——每一个新发现,都在推翻之前的理所当然。
环形RNA的故事告诉我们:微小的分子,也能掌控生命的开关。 未来当我们再谈论基因调控时,或许不会只盯着DNA和蛋白,而是会想起那些在细胞质里悄悄拖拽mRNA的环形分子,想起那些藏在无膜颗粒里的、决定细胞命运的微小选择。
点击充电,成为大圆镜下一个视频选题!