
4 个月前

4 个月前
对于全球数百万乳腺癌患者而言,过去十年是一场希望与失落交织的赛跑。2015年以来,以CDK4/6抑制剂为代表的靶向药物,如同一道曙光,彻底改变了最常见的HR+/HER2-亚型乳腺癌的治疗格局。这些药物像精准的“刹车系统”,通过抑制细胞周期蛋白依赖性激酶CDK4和CDK6这两个关键“引擎”,有效阻止了癌细胞的失控性增殖,将患者的生存期显著延长。
然而,癌细胞的狡猾超乎想象。在这场漫长的拉锯战中,一个巨大的阴影逐渐笼罩临床——耐药性。就像经验丰富的游击队,癌细胞总能找到绕过封锁的秘密通道。当CDK4/6两条主路被堵死后,它们会激活一个名为CDK2的“备用引擎”,重新启动增殖机器,导致治疗失效,疾病卷土重来。这个“逃逸路线”一度成为横亘在医生和患者面前的巨大瓶颈,一个看似无解的僵局。
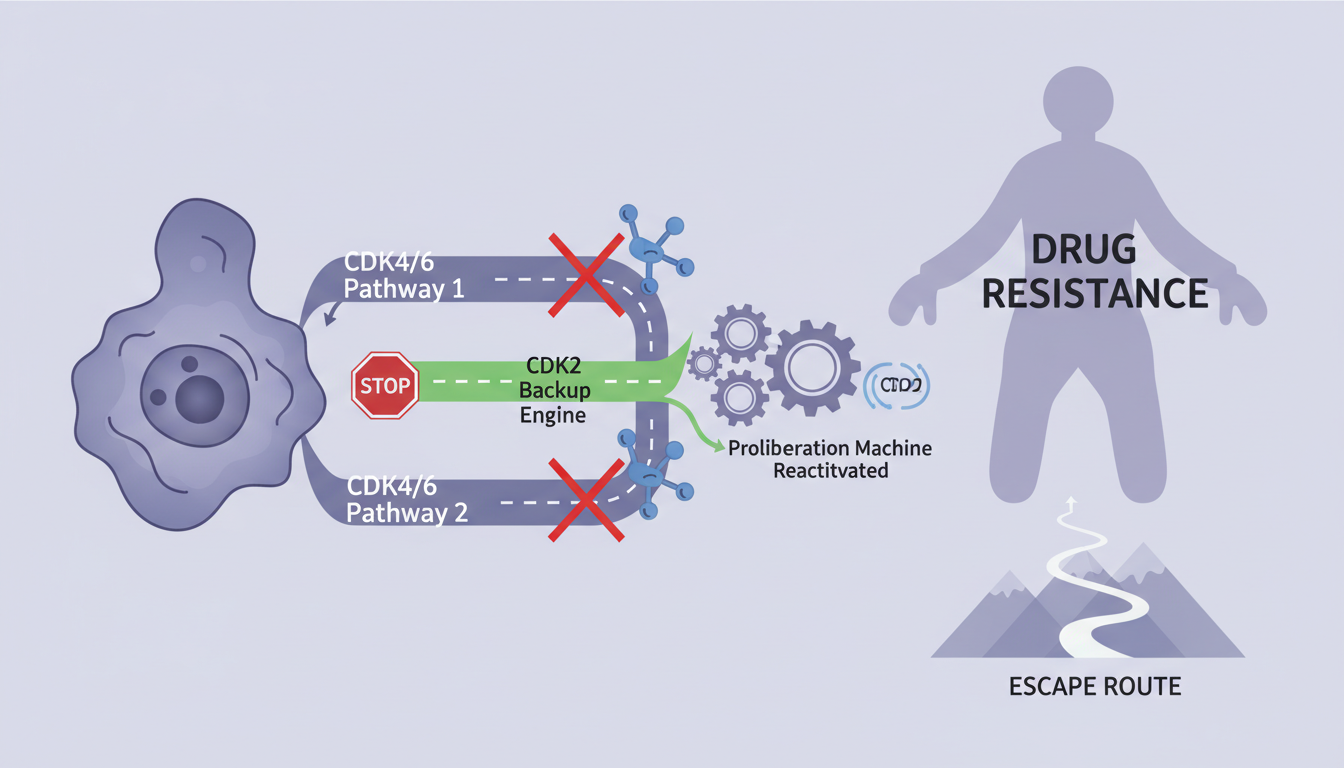
现在,这个僵局可能即将被打破。
近日,由解放军总医院第五医学中心的江泽飞教授与江苏省人民医院的殷咏梅教授领衔的一项3期临床研究,在国际顶尖期刊《信号转导与靶向治疗》上投下了一枚重磅炸弹。研究结果证实,一款名为culmerciclib(库莫西利)的新型多靶点抑制剂,联合内分泌治疗药物氟维司群,成功地将HR+/HER2-晚期乳腺癌患者的无进展生存期(PFS)从7.5个月戏剧性地延长至16.6个月——翻了一倍还多。
这组惊人的数据背后,是疾病进展或死亡风险降低了64%的巨大临床获益。更重要的是,这是全球首个在大型临床试验中被验证的、通过同时抑制CDK2、CDK4和CDK6三大靶点来有效克服耐药性的治疗策略。这项由中国科学家主导的研究,不仅为无数患者带来了新的希望,也标志着乳腺癌精准治疗正式迈入一个新阶段。
要理解culmerciclib的革命性,必须深入癌细胞的“作战指挥室”——细胞周期调控系统。癌细胞的疯狂增殖,依赖于CDK家族蛋白(特别是CDK2, 4, 6)作为“油门”,推动细胞分裂。传统的CDK4/6抑制剂,相当于同时踩住了两个油门踏板,效果显著,但癌细胞很快学会了猛踩第三个(CDK2),继续飞速前进。
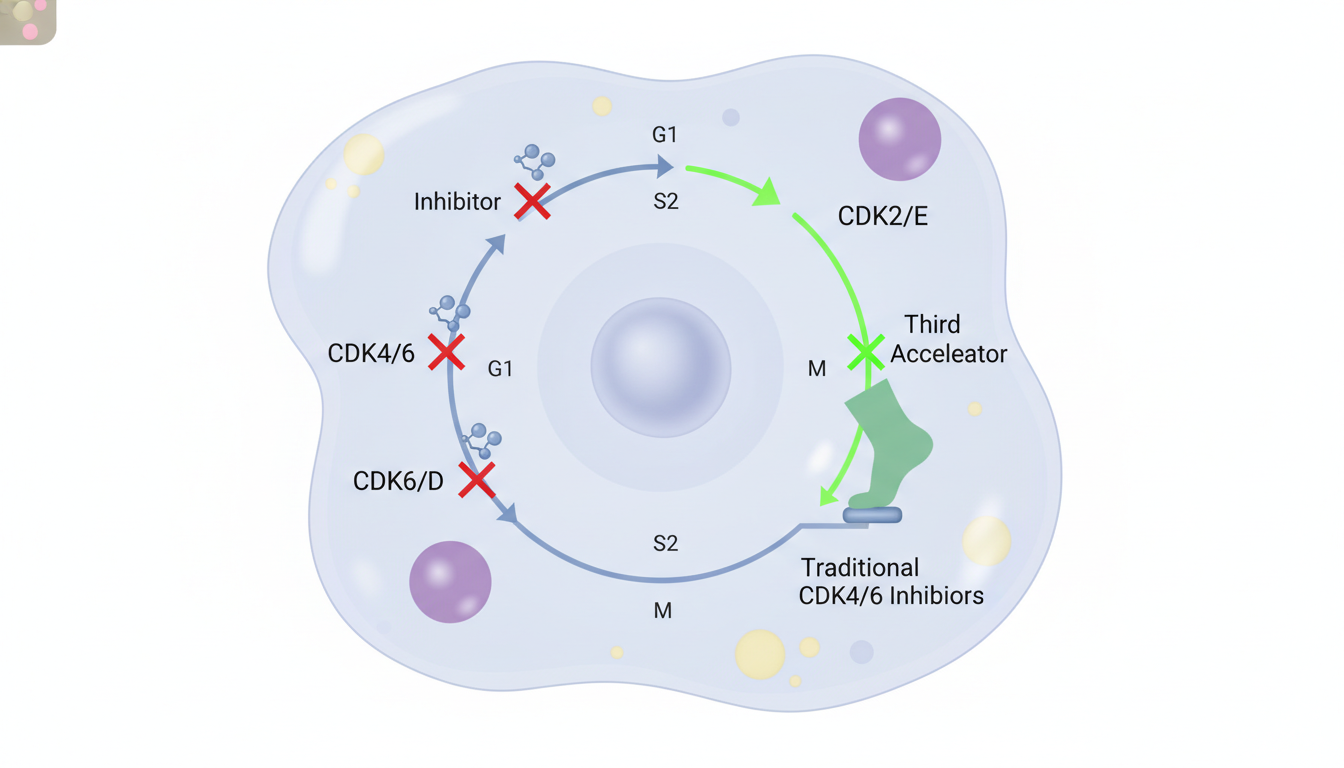
Culmerciclib的设计理念,正是要彻底终结这场“猫鼠游戏”。它不再是单点或双点打击,而是一种“三位一体”的全面封锁。通过独特的分子结构设计,它不仅能强效抑制CDK4,更重要的是,它对CDK2也表现出强大的抑制能力。这种多靶点抑制策略,相当于同时锁死了癌细胞增殖的所有关键引擎,使其无路可逃。
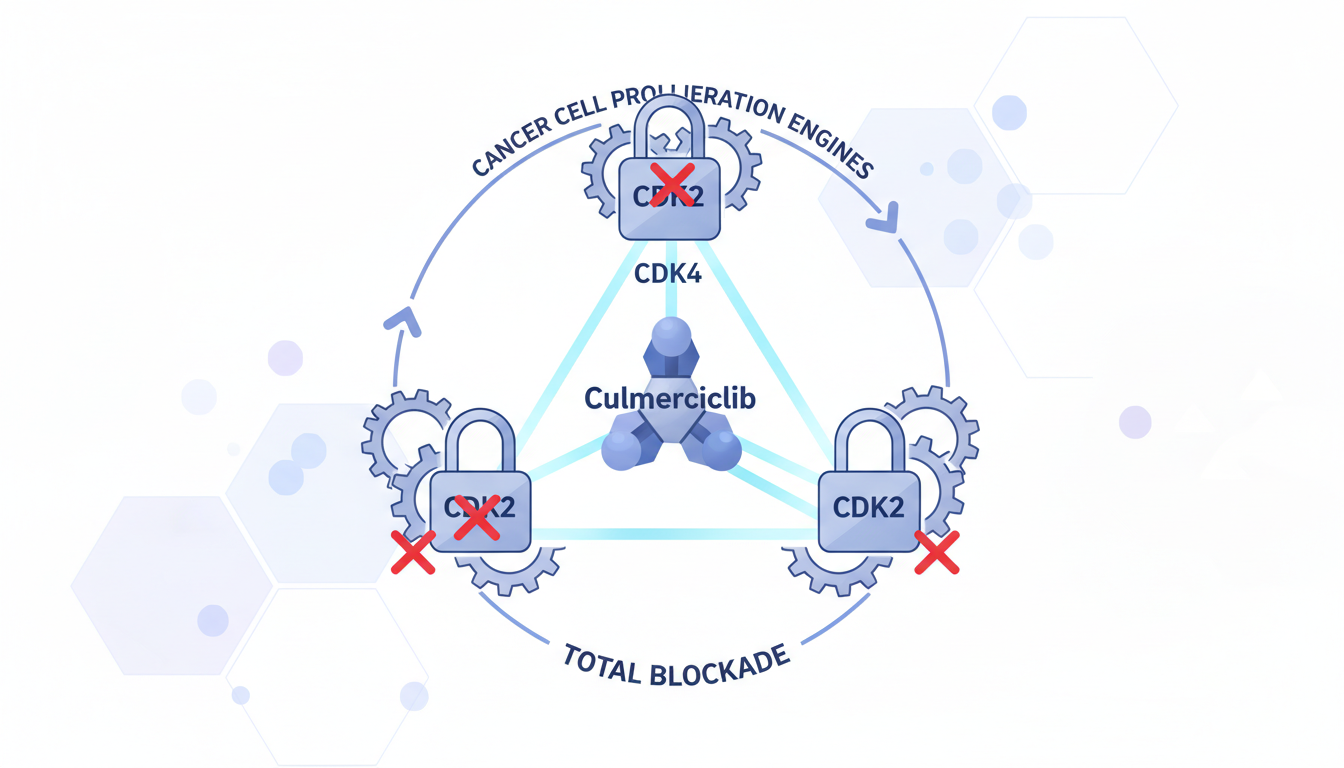
更有价值的是,culmerciclib对CDK6的抑制作用相对较弱。这一点至关重要,因为CDK6与造血功能密切相关,过度抑制是导致严重骨髓抑制(如中性粒细胞减少)副作用的主要原因。这种“有保有压”的精准设计,使得culmerciclib在强效抗癌的同时,展现出更好的安全性,为患者的长期治疗提供了保障。
此次公布的3期临床试验(CULMINATE-1)纳入了293名既往接受过治疗的患者,她们代表了临床上最棘手的群体。试验结果不仅PFS数据亮眼,其他指标同样令人振奋:
这些数据共同描绘了一幅清晰的图景:culmerciclib不仅“有效”,而且“安全”、“普适”,具备成为新一代标准疗法的巨大潜力。
CDK抑制剂的研发历程,是一部不断追求精准与安全的进化史。从第一代“广谱撒网”、毒副作用巨大的泛CDK抑制剂,到第三代高选择性、极大改变临床实践的CDK4/6抑制剂,科学家们用了近二十年。然而,耐药问题始终是悬顶之剑。
Culmerciclib的出现,可以被视为第四代CDK抑制剂的曙光。它所代表的CDK2/4/6多靶点抑制策略,正是为了解决前代药物的根本痛点而生。这一由中国本土药企(正大天晴)自主研发的创新药,从分子设计到完成关键性3期临床研究并获批上市,标志着中国在肿瘤新药研发领域,正实现从“跟跑”、“并跑”到部分领域“领跑”的历史性跨越。
Culmerciclib的成功,仅仅是乳腺癌精准治疗新篇章的序言。它证明了更深入地理解肿瘤耐药机制,并据此设计更智慧的药物,是未来抗癌战争的决胜关键。
未来的战场将更加精细化和个体化:
这场与癌症的战争远未结束,但每一次科学的突破,都如同在漫长的隧道尽头点亮一盏新的明灯。Culmerciclib的问世,正是这样一盏灯,它不仅照亮了克服耐药性的道路,也预示着一个依靠智慧和创新,为每一位患者量身定制治疗方案的个体化医疗新纪元,正加速到来。
点击充电,成为大圆镜下一个视频选题!