
10 天前

10 天前
当一条年产5000吨的生产线突然砍掉60%产能,你很难不注意到背后的市场暗涌。2026年4月,一家靠生物可降解塑料PHA(聚羟基脂肪酸酯)闻名的合成生物企业,宣布将3000吨PHA产能转向红法夫酵母、芽孢杆菌等绿色饲料添加剂——这不是一时的产能调剂,而是一场用技术重新定义增长逻辑的转身。
为什么曾被资本热捧的PHA会遇冷?为什么是农业赛道接住了这次转型?要回答这些问题,得先从合成生物技术到底是什么说起。
你可以把合成生物技术理解成给细胞写代码——它不是简单地改造某个基因,而是像搭乐高一样,把来自不同生物的基因元件拼接组合,让细胞按照人类的指令生产特定物质。比如PHA,就是通过改造微生物的代谢路径,让它们像“微型工厂”一样,把糖、秸秆甚至二氧化碳转化成可降解的生物塑料。
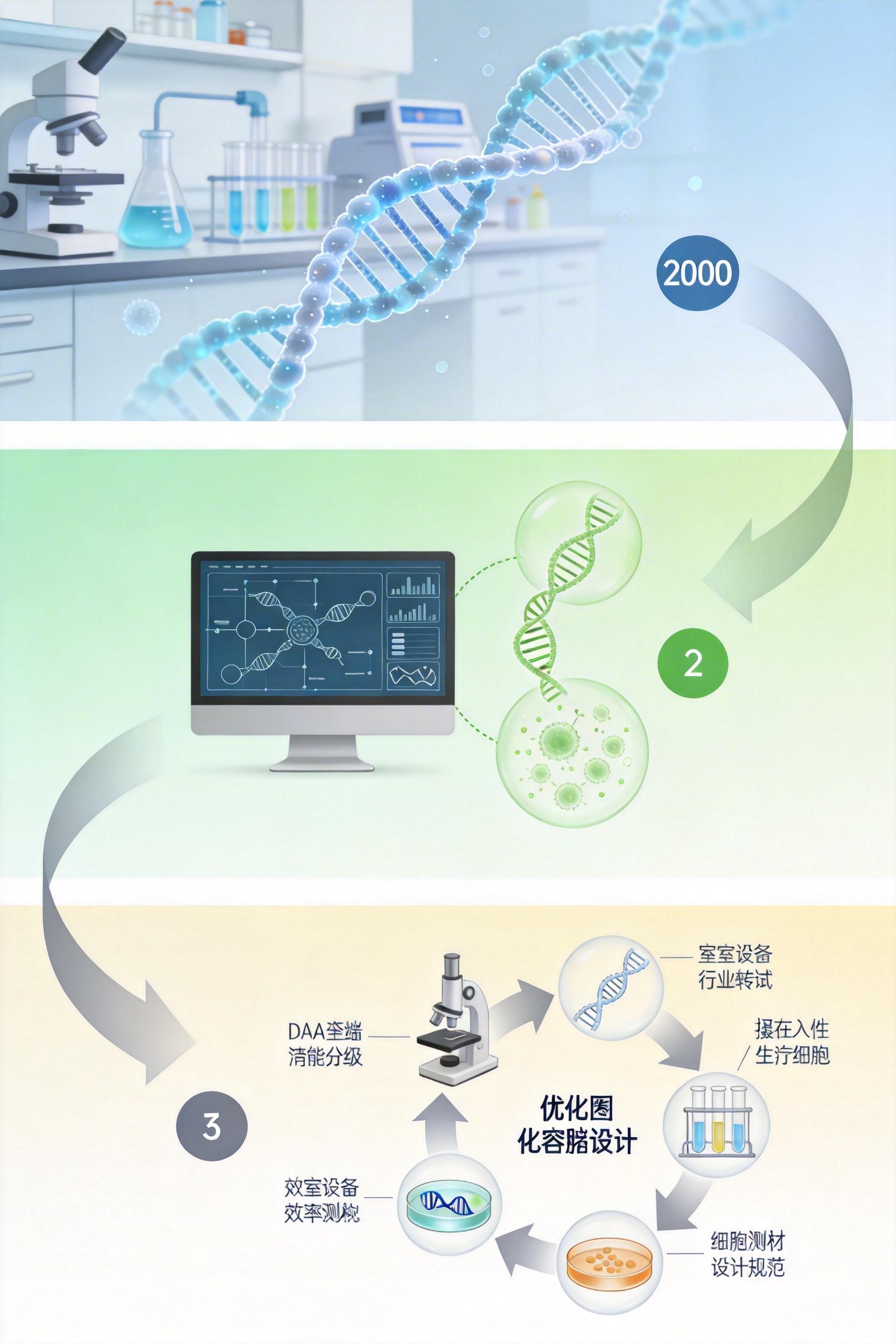
这项技术的起点可以追溯到2000年,麻省理工学院的团队首次构建出人工遗传开关,相当于给细胞装上了“开关按钮”。此后的20多年里,合成生物学从实验室走向产业,核心是一套叫“设计-构建-测试-学习”的循环机制:先在计算机上设计代谢路径,再合成对应的DNA片段导入细胞,测试生产效率,最后根据结果优化设计。这套循环让技术迭代速度呈指数级提升。
对于转型的企业来说,PHA的遇冷并非技术失败——这种塑料能在海洋、土壤甚至人体里完全降解,性能媲美传统塑料,但它的痛点卡在了成本和市场:生产1公斤PHA的成本是传统塑料的2-3倍,而全球可降解塑料的市场需求还在缓慢培育,导致5000吨的生产线只能开动40%。
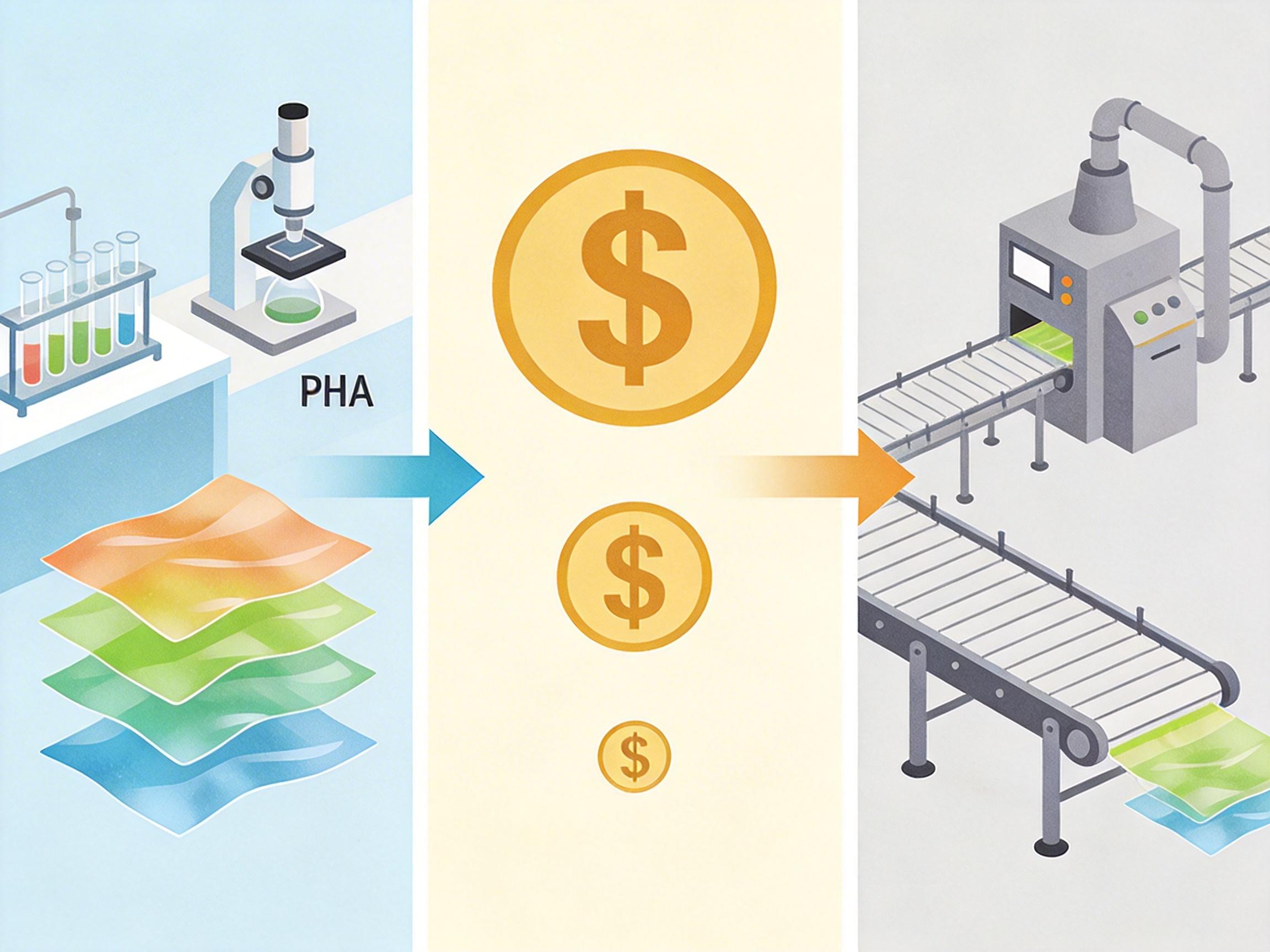
转向农业赛道,并非从零开始。这家企业多年积累的合成生物技术,刚好能平移到微生物饲料添加剂的生产上——本质都是改造微生物的代谢路径,只是把“生产塑料”的指令换成了“生产益生菌”。
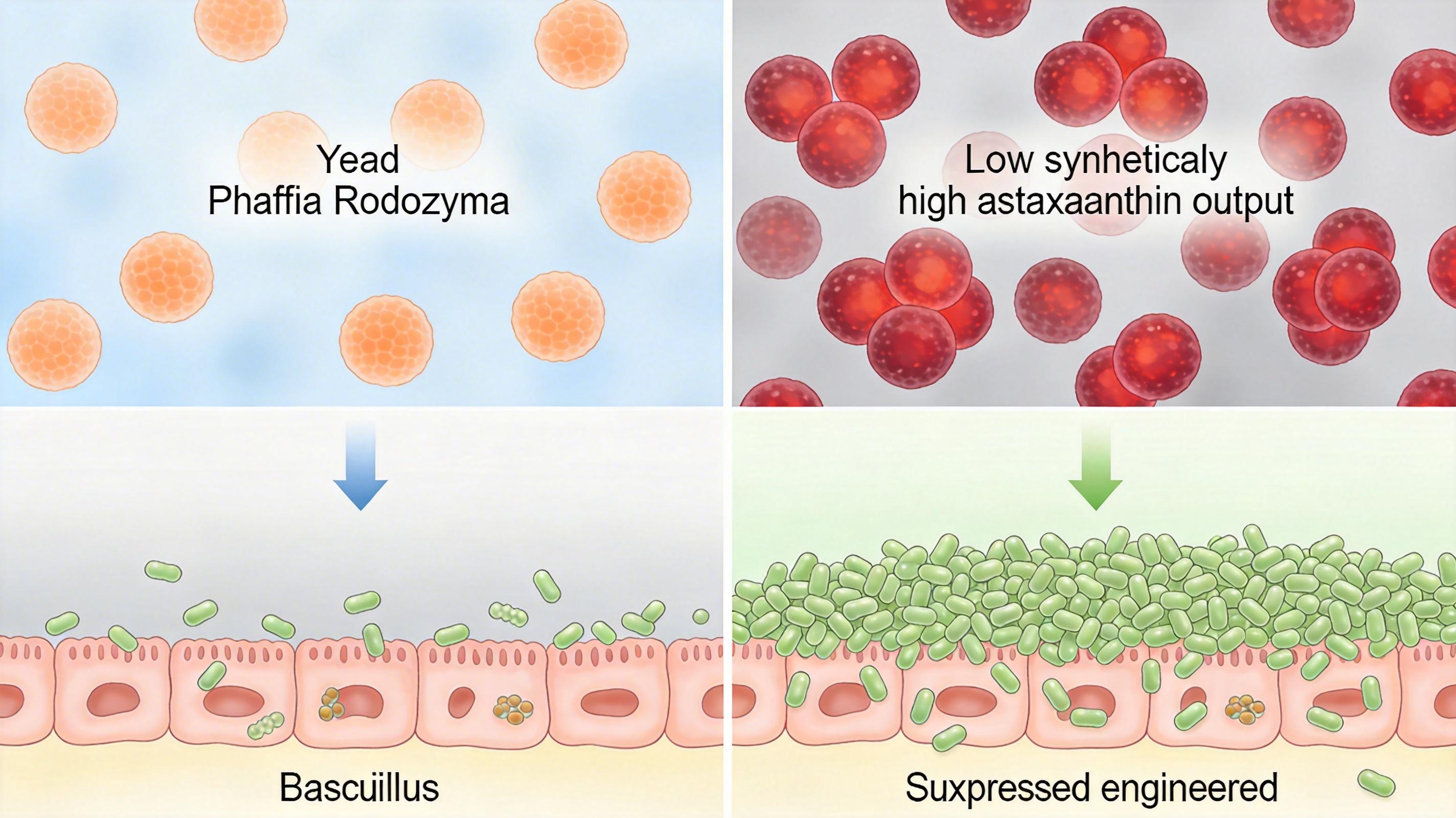
比如红法夫酵母,天然就能产生虾青素,这种物质能提升水产动物的免疫力和肉质颜色,是替代抗生素的理想饲料添加剂。但野生酵母的虾青素产量极低,通过合成生物技术,科学家可以敲除酵母体内无关的代谢路径,强化虾青素的合成线路,让产量提升数十倍。同样的逻辑也适用于芽孢杆菌:通过改造基因,让它能更稳定地在动物肠道定殖,抑制有害菌生长。
更关键的是,农业赛道的需求更迫切。中国自2020年全面禁止饲料添加抗生素后,微生物饲料添加剂的市场规模以每年15%的速度增长。相比PHA依赖海外市场的单一需求,农业领域的饲料添加剂、土壤改良剂、作物促生长剂等,构成了一个多层次的本土市场网络。这次转型后,企业不仅能把闲置的产能用起来,还能通过与农业巨头的合作,快速打通从实验室到田间的渠道。
这场转型的背后,藏着合成生物产业的一个核心矛盾:技术的可能性,永远走在市场需求的前面。
PHA的困境不是个例。很多合成生物产品在实验室里表现亮眼,但走到市场上,要么成本下不来,要么找不到足够大的应用场景。而农业赛道的优势在于,它是一个“刚需驱动”的市场——农民需要更高效的饲料,消费者需要更安全的农产品,政策需要更绿色的农业模式,这些需求都是明确且紧迫的。
但转型也并非没有挑战。农业领域的微生物产品,对稳定性和安全性的要求更高:饲料添加剂要能扛过饲料加工的高温,土壤改良剂要能适应不同的土壤环境。这意味着企业需要在技术上做更精细的调整——比如给微生物穿上一层“保护壳”,让它们能在恶劣环境下存活。此外,公众对生物技术在农业中的应用仍有疑虑,如何通过科普和实际效果建立信任,也是企业需要面对的长期课题。
当合成生物技术不再只盯着“高大上”的新材料,转而扎根泥土里的需求,它才真正找到了落地的土壤。这场从PHA到饲料添加剂的转型,本质上是技术向市场的回归——不是技术妥协于市场,而是技术在市场中找到更合适的生长空间。
技术的价值,从来不是造出多么复杂的东西,而是解决真实的问题。当微生物工厂的齿轮转向农业,我们看到的不只是一家企业的转型,更是合成生物技术真正融入产业的开始。
点击充电,成为大圆镜下一个视频选题!