对抗知识焦虑,从看懂这条开始
App 下载
三阴性乳腺癌耐药谜团,被中国团队解开了
肿瘤转移|复旦大学团队|PKD1突变|免疫治疗耐药|三阴性乳腺癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
肿瘤转移|复旦大学团队|PKD1突变|免疫治疗耐药|三阴性乳腺癌|肿瘤学|医学健康
58岁的张阿姨躺在病床上,手里攥着最新的检查报告——她的三阴性乳腺癌已经转移到了肺部。医生推荐的免疫治疗刚做了三次,肿瘤反而长大了。这不是个例:约15%的乳腺癌患者属于这种‘三阴性’亚型——既不依赖雌激素、孕激素,也没有HER2靶点,像个‘无孔不入’的幽灵,转移后中位生存期只有17到27个月。免疫治疗曾是她们的希望,但近一半患者会出现耐药,肿瘤在药物眼皮底下继续扩散。直到2026年3月,复旦大学的研究团队在这些耐药肿瘤里,找到了藏得最深的那个‘帮凶’。
三阴性乳腺癌的难缠,一半源于它的‘善变’。和其他乳腺癌亚型不同,它像一群没有统一指挥的叛军,能分化出基底样、免疫调节型等多个分支,每个分支对治疗的反应天差地别。而一旦发生转移,这些肿瘤细胞还会在新的器官里继续突变,长出和原发肿瘤完全不同的‘新面孔’——这也是很多药物失效的原因。
复旦大学的团队盯上了这个‘变脸’的过程。他们收集了296例中国转移性三阴性乳腺癌患者的转移灶样本,覆盖18个器官的796次转移事件,用484基因测序工具逐一排查。结果在转移灶里发现了一个异常活跃的基因:PKD1。约8%的转移样本里都有它的突变,这个比例远高于原发肿瘤,而且在105对原发和转移的配对样本里,这个差异被再次证实。
你可以把PKD1想象成肿瘤细胞的‘隐身斗篷开关’。正常情况下,它参与调控细胞的基本活动,但一旦突变,就会启动肿瘤的‘隐身模式’——这也解释了为什么免疫治疗会失效:免疫系统根本找不到这些藏起来的肿瘤细胞。
为了搞清楚PKD1到底是怎么帮肿瘤隐身的,团队做了一系列实验——从细胞培养到小鼠模型,再到真实的临床试验数据。他们发现,PKD1突变后,会指挥肿瘤细胞大量分泌一种叫CCL2的趋化因子。
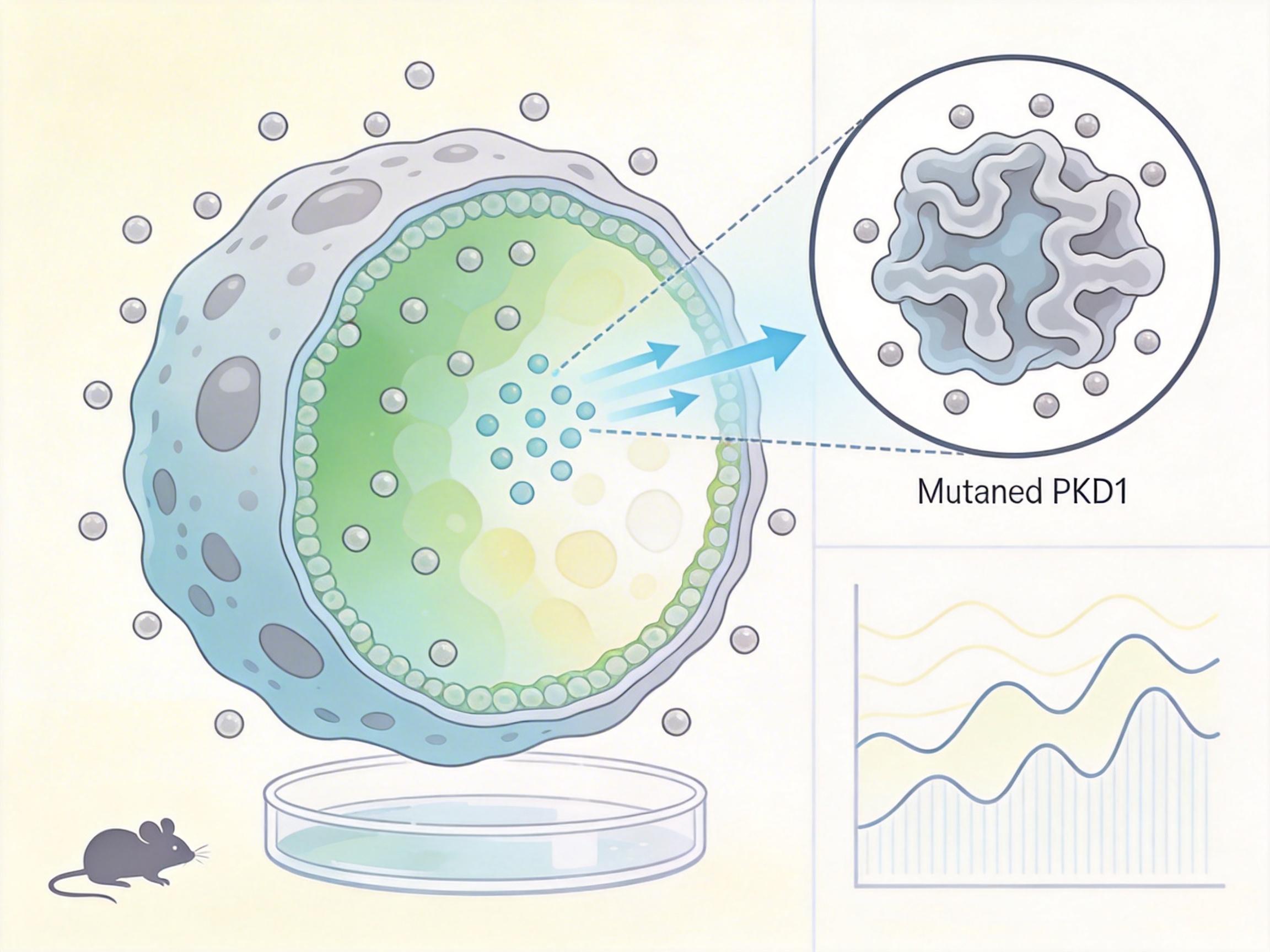
你可以把CCL2理解成肿瘤放出的‘劝退令’。它会像磁铁一样吸引来免疫抑制性的M2型巨噬细胞,同时把能杀伤肿瘤的M1型巨噬细胞和CD8+T细胞挡在门外。原本应该是免疫细胞‘战场’的肿瘤微环境,慢慢变成了寸草不生的‘荒漠’:没有免疫细胞能进来,进来了也会被‘策反’成帮凶。
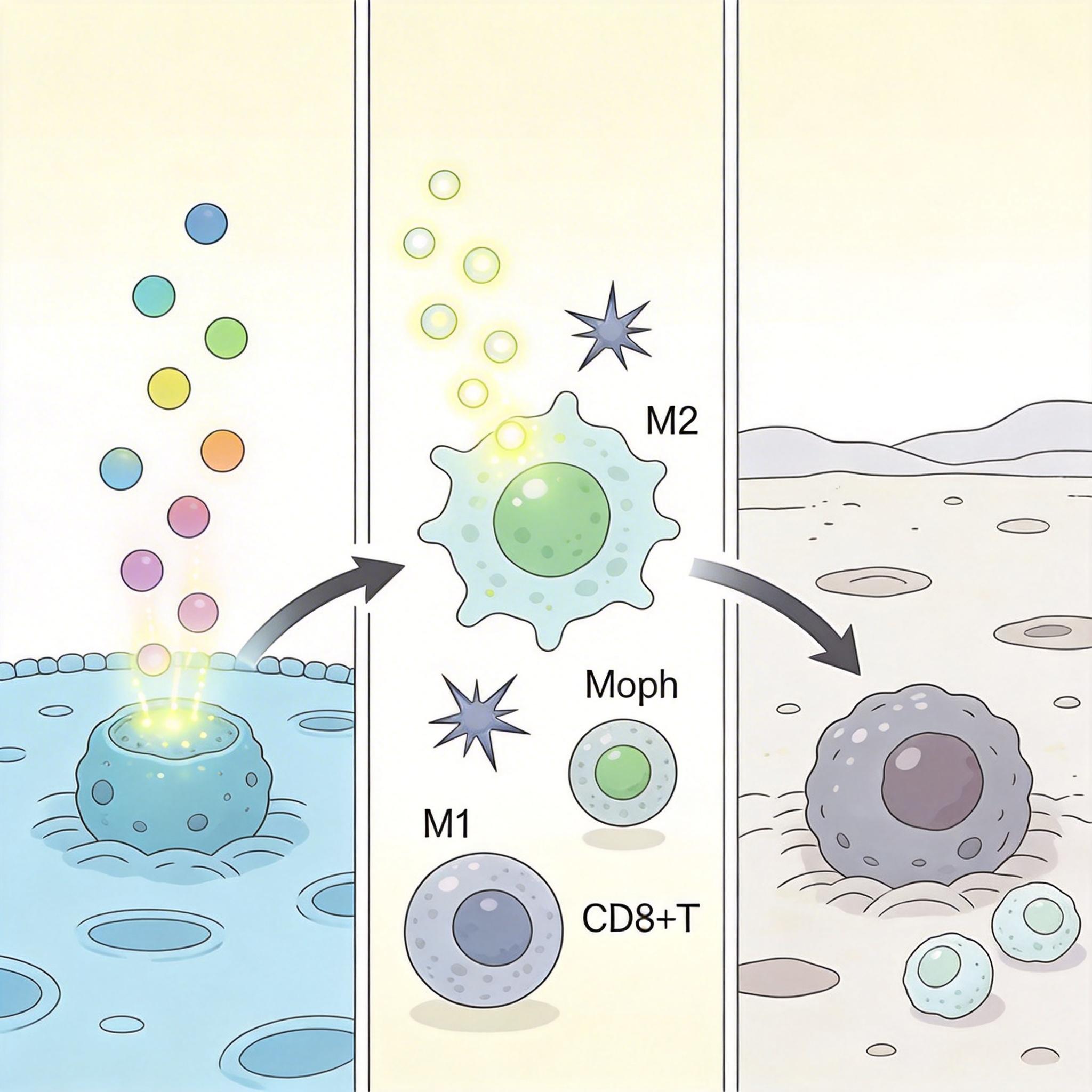
三项针对中国患者的临床试验数据验证了这个结论:携带PKD1突变的患者,对PD-1抑制剂的客观缓解率几乎为零,无进展生存期比没有突变的患者短了近一半。更关键的是,当研究人员用药物阻断CCL2后,小鼠模型里的免疫‘荒漠’重新长出了‘植被’——CD8+T细胞和M1型巨噬细胞回来了,肿瘤的生长速度明显变慢,甚至开始缩小。
这个发现给了耐药患者新的希望,但从实验室到病床,还有几道必须跨过去的坎。
首先是精准筛选患者。目前的检测还只能通过基因测序找到PKD1突变,但未来需要更便捷的生物标志物——比如血液里的CCL2浓度,或者肿瘤组织里的免疫细胞分型,让医生能快速判断谁适合这种联合治疗。
其次是平衡疗效和副作用。激活免疫系统就像打开了潘多拉的盒子,可能会引发免疫相关的不良反应,比如甲状腺炎、肺炎。如何精准调控免疫激活的程度,只攻击肿瘤而不伤害正常组织,是接下来要解决的核心问题。
更重要的是,中国患者的基因组特征和西方人群有差异——比如中国患者里PIK3CA突变率更高,TP53突变率更低。这意味着基于西方数据的治疗方案,不一定完全适合中国患者。这次的研究正是填补了这个空白,用中国患者的样本,找到了属于我们自己的耐药机制。
张阿姨的主治医生后来给她换了治疗方案——在PD-1抑制剂的基础上,加了一款针对CCL2的靶向药。三个月后,她肺部的肿瘤缩小了40%。
这不是一个奇迹,而是精准医疗的必然:当我们终于看清了肿瘤的‘隐身术’,就能找到破解它的钥匙。靶点藏在突变里,希望藏在细节中。未来的癌症治疗,不再是用同一种药对付所有患者,而是像侦探一样,根据每个肿瘤的‘指纹’,定制专属的抓捕方案。而中国患者的基因组数据,就是我们手里最珍贵的那本‘犯罪实录’。