
4 个月前

4 个月前
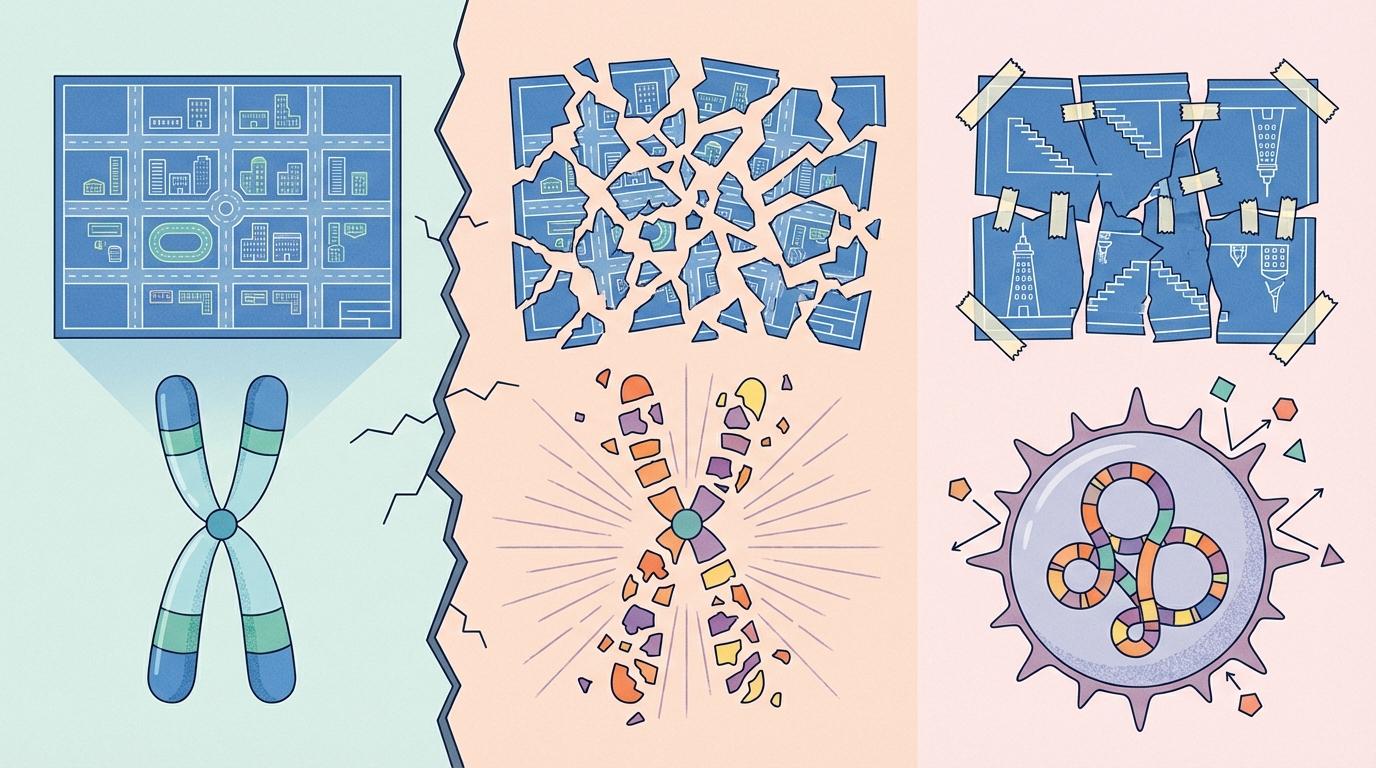
想象一下,一个城市的蓝图在一瞬间被撕成碎片,然后被胡乱地拼接在一起。这正是癌细胞内部正在上演的惊悚剧目——染色体碎裂(chromothripsis)。自2011年首次被发现以来,这一现象一直困扰着科学家。它不是温和的基因突变,而是一场灾难性的“基因组大地震”,一条或多条染色体在单次事件中崩解成数百个片段,再以随机、混乱的方式重新组合。这场混乱赋予了癌细胞一种可怕的能力:“超级进化”。通过这种方式,癌细胞可以迅速扩增癌基因、删除抑癌基因,从而轻松获得耐药性,让多种治疗手段失效。2020年的一项泛癌分析显示,这种现象在某些癌症中的发生率甚至超过50%。然而,十多年来,引发这场地震的“震源”究竟是什么,一直是个未解之谜。
近日,加州大学圣迭戈分校的Don W. Cleveland团队在顶级期刊《科学》上发表的重磅研究,终于将这场“基因犯罪”的头号嫌犯缉拿归案。这个嫌犯是一个名为N4BP2的核酸内切酶,一种潜伏在细胞质中的“分子剪刀”。
Cleveland团队的追捕过程如同一场精密的侦探工作。他们首先构建了一个特殊的肠癌细胞模型,在这个模型中,Y染色体会在细胞分裂时被错误地隔离进一个脆弱的临时监狱——微核(micronuclei)。当微核的“围墙”破裂时,Y染色体就会暴露在细胞质中,任人宰割。研究人员利用小干扰RNA技术,对细胞内204种已知的核酸酶(分子剪刀)进行了两轮地毯式排查。最终,所有线索都指向了此前功能尚不明确的N4BP2。
实验证据无可辩驳:
这一发现首次从分子层面揭示了染色体碎裂的直接推手。N4BP2并非导致微核形成的元凶,而是在微核破裂后,对暴露的染色体执行“死刑”的刽子手。
一个悬念随之而来:既然N4BP2是“行凶者”,那么是谁为它创造了机会,打破了微核这个“监狱”呢?巧合的是,就在去年,两项背靠背发表于《科学》的研究已经为我们揭示了“破门”的同伙。
研究发现,癌细胞中微核附近的线粒体——细胞的“能量工厂”——会释放出大量活性氧(ROS)。这些活性氧如同腐蚀性的酸液,一方面直接侵蚀微核的包膜,使其变得脆弱;另一方面,它们还会加速降解负责修复微核包膜的蛋白,双管齐下,最终导致微核彻底崩塌。
至此,癌细胞“超级进化”的犯罪链条被完整地拼接起来:
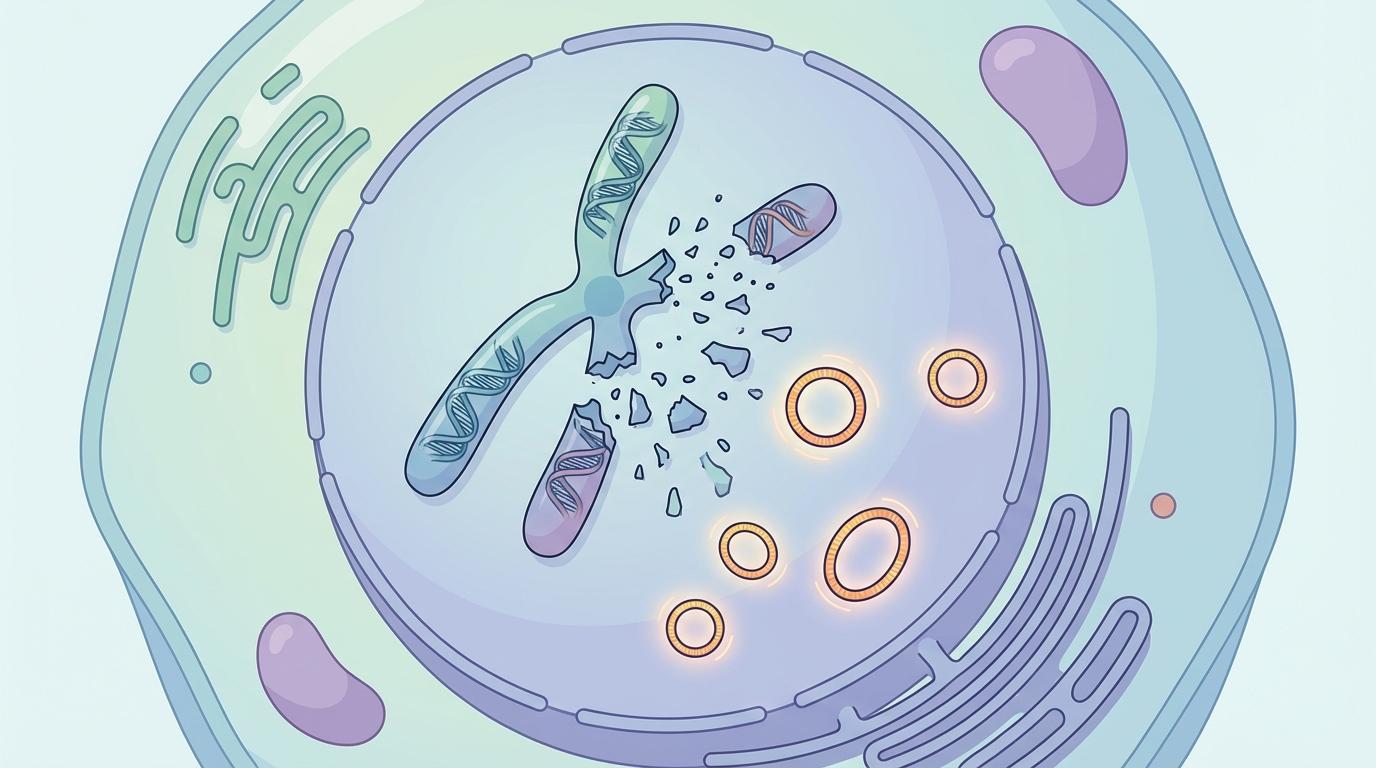
染色体碎裂后留下的残骸并非毫无用处。这些基因碎片会形成一种更危险的存在——染色体外DNA(ecDNA)。这些小型的环状DNA,是癌细胞最狡猾的“外挂程序”。
与庞大、受严格调控的染色体不同,ecDNA拥有几大“特权”:
N4BP2的发现,将染色体碎裂和ecDNA的形成紧密联系在一起,揭示了后者正是前者的直接下游产物。这也解释了为何N4BP2高表达的肿瘤,往往更具侵袭性,预后也更差——其关联性甚至强于著名的抑癌基因TP53。
揭开谜底的目的,是为了找到破解之法。N4BP2的发现,为癌症治疗提供了一个极具潜力的全新靶点。目前的许多疗法,如CHK1抑制剂,旨在干扰ecDNA的复制,但这属于“下游”干预。而靶向N4BP2,则相当于在“犯罪”的源头进行阻断,阻止ecDNA的产生,这无疑是更根本的策略。
更令人兴奋的是,靶向N4BP2可能带来“一石二鸟”的效果。当微核破裂,DNA碎片散落到细胞质中时,会激活细胞内的cGAS-STING天然免疫通路,这相当于向免疫系统发出了“警报”。通过调控N4BP2的活性,或许可以控制这一过程,将原本对免疫疗法不敏感的“冷肿瘤”转变为免疫系统可以识别和攻击的“热肿瘤”,从而增强免疫检查点抑制剂等疗法的效果。
当然,从基础研究的突破到临床应用的药物,还有很长的路要走。科学家们面临着新的挑战:
尽管挑战重重,但N4BP2的发现无疑为我们对抗癌症的武器库增添了一件极具潜力的新式武器。它让我们深刻地认识到,癌症的强大之处在于其混乱和演化能力。而通过揭示其制造混乱的底层逻辑,我们正一步步学会如何瓦解它的进化策略。这场围绕基因组的战争,正因这些基础科学的突破,而迎来新的转机。
点击充电,成为大圆镜下一个视频选题!