对抗知识焦虑,从看懂这条开始
App 下载
AI一次画出蛋白质,药物研发快了几十倍
碳水化合物结合蛋白|三维结构预测|氨基酸序列设计|蛋白质生成模型|新药研发|AIGC|医学健康|人工智能
对抗知识焦虑,从看懂这条开始
App 下载
碳水化合物结合蛋白|三维结构预测|氨基酸序列设计|蛋白质生成模型|新药研发|AIGC|医学健康|人工智能
想象一下:你要设计一把能精准插进锁孔的钥匙,不用先画图纸再打磨,也不用反复试错调整——只要说出锁的样子,钥匙的形状和金属纹路就能同时成型,插进锁里还能直接转动。这不是科幻,而是如今在生物实验室里发生的事:某团队开发的AI模型,能一步生成蛋白质的氨基酸序列和原子级三维结构,针对127个靶点的设计中,86个成功命中,单个靶点的最高命中率达63.5%,甚至做出了传统方法根本造不出来的、能结合碳水化合物的蛋白质。它是怎么跳过那些繁琐步骤,直接从需求跳到结果的?
你可以把蛋白质从头设计(de novo protein design)理解为“凭空造一把能开门的钥匙”——钥匙就是能绑定靶点的蛋白质,门就是对应的生物功能,比如阻断病毒入侵、激活细胞信号。过去的设计师有两种思路:要么拿着现成的钥匙模板改,改完就不能再调;要么完全凭空瞎想,从零开始慢慢试,不行再拆了重来。
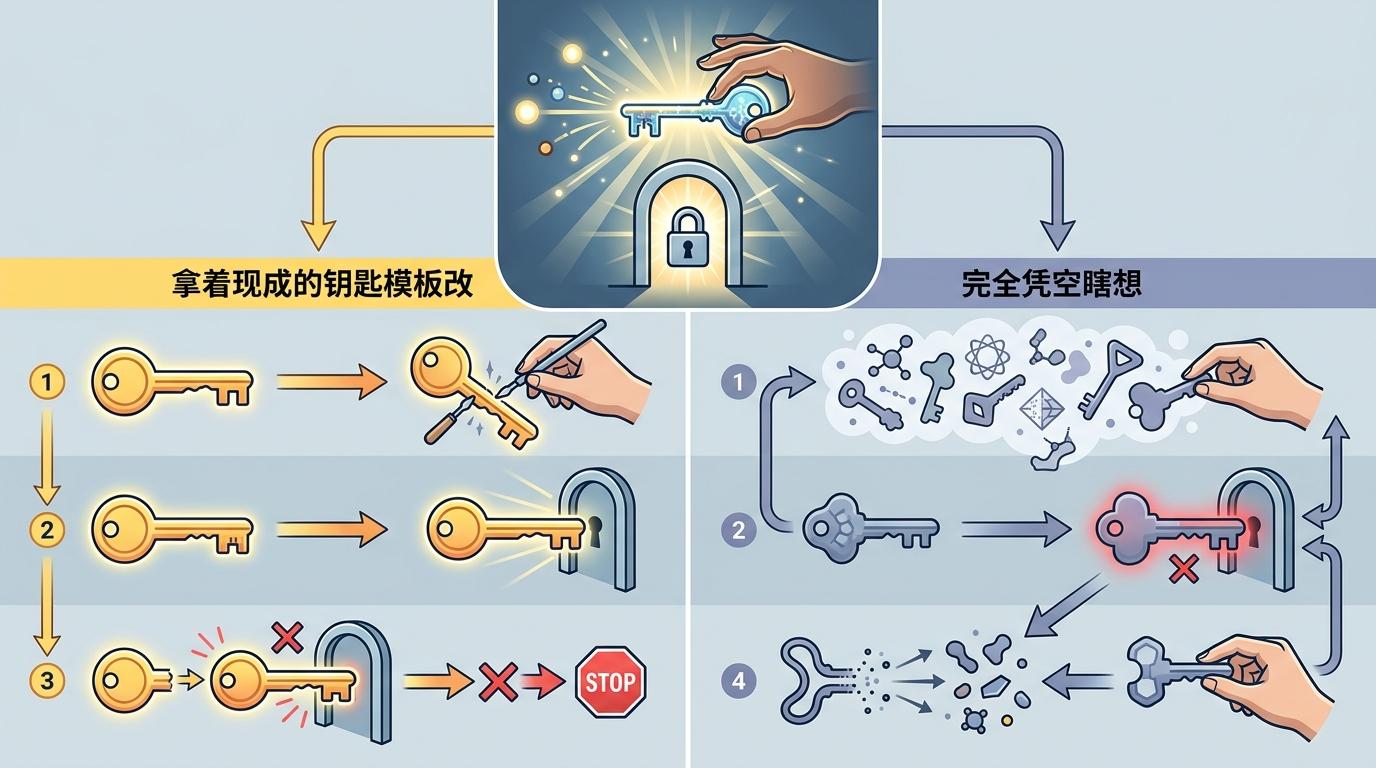
这两种方法都有绕不开的坑:模板法太死板,遇到没见过的锁就抓瞎;凭空法效率太低,往往要搭配好几个模型,先画钥匙轮廓,再打磨齿纹,最后还要验证能不能插进锁孔,不仅慢,还容易在步骤间出错。
新的AI模型打破了这种二元对立。它在一个连续的“潜在空间”里同时生成钥匙的形状和齿纹——也就是蛋白质的结构和序列,不用先画轮廓再补细节,也不用事后再调整。就像你在脑子里想好钥匙的样子,手里的3D打印机直接把完整的钥匙打印出来,不用任何后续加工。
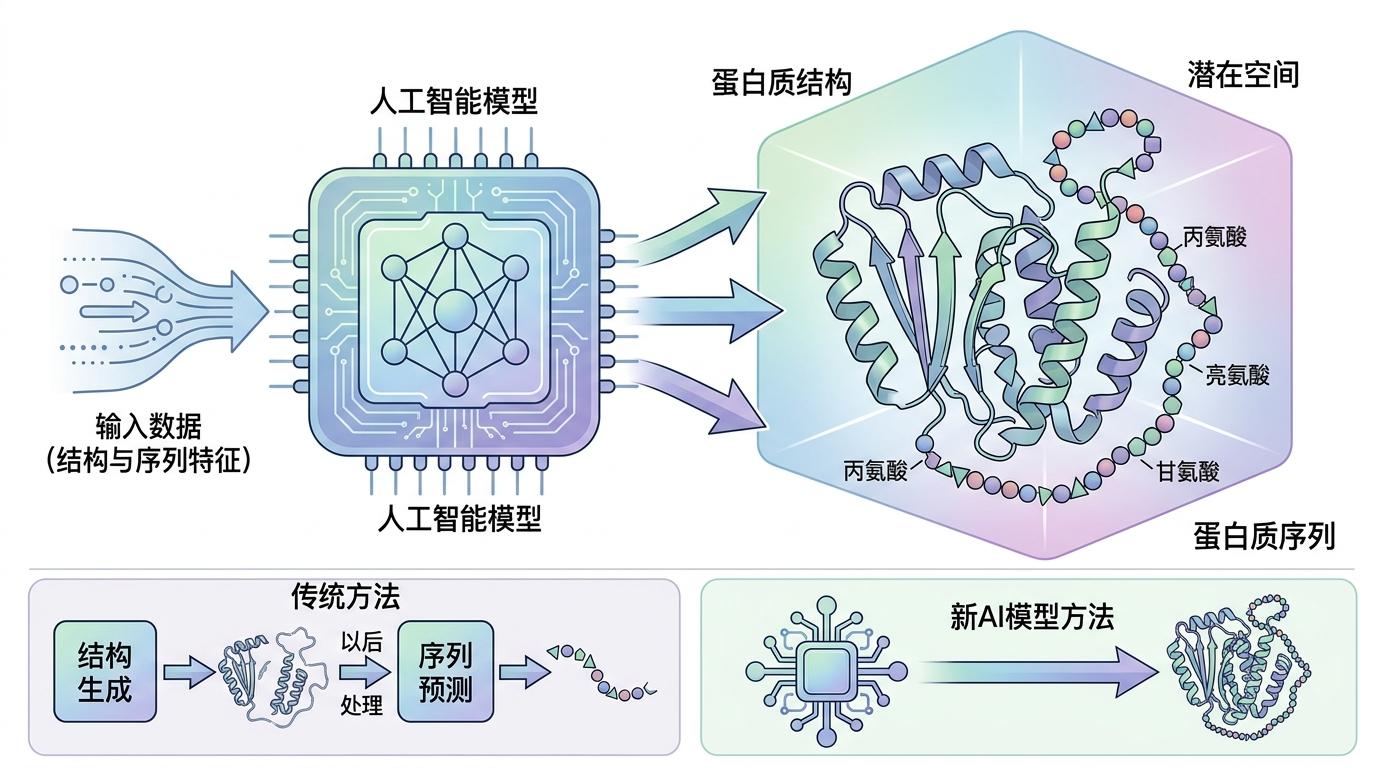
更关键的是,它解决了“没东西可学”的问题。过去研究蛋白质的实验数据太少,就像学开锁的人只见过10种锁。团队用AlphaFold预测的结构数据,拆分重组出了比现有公共数据库大10倍的合成数据集——相当于让AI学了100种锁的结构,自然能开出更多种门。
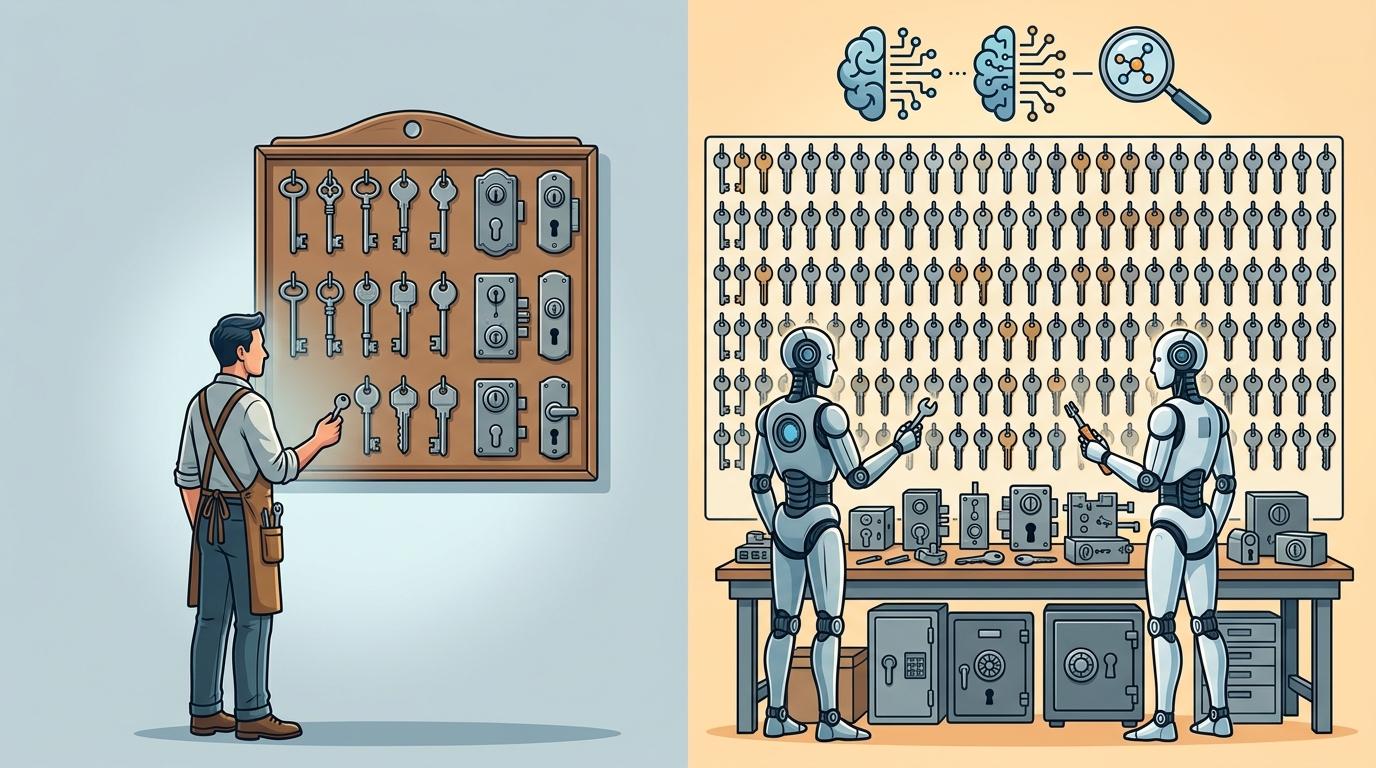
最直观的改变是速度。生成单个候选蛋白质,传统方法要70多秒,新模型只需要15.6秒——相同算力下,能多生成4倍多的候选样本,找到好钥匙的概率自然更高。
更重要的是“准”。在针对127个靶点的大规模实验中,它设计的蛋白质有91.2%能精准绑定目标靶点,不会误碰其他“锁孔”——这在药物研发里至关重要,意味着更低的副作用风险。针对PDGFR这个治疗癌症的关键靶点,它的命中率高达63.5%,最强的结合剂能以皮摩尔级的亲和力绑定靶点,这个强度已经达到了直接成药的标准。
最让人意外的是它突破了“不可能完成的任务”:传统方法根本做不出能结合游离碳水化合物的蛋白质,因为碳水化合物体积小、极性强,就像一个滑溜溜的球形锁,很难设计出能抓住它的钥匙。但这个AI模型做到了——针对血型B抗原的设计中,24个候选里有5个能让B型血红细胞凝集,最优候选的热稳定性超过95℃,已经具备了实际应用的潜力。
当然,它也不是万能的。目前它对多链蛋白质复合物的动态结构设计还不够精准,面对一些极端罕见的靶点,命中率依然会大幅下降。而且所有AI设计的结果,最终都还是要经过湿实验验证,不可能完全替代实验室里的试错。
这个模型的开源,意味着全球的科研人员和药企都能免费使用它的代码和数据集。已经有医药巨头用它来加速药物研发,还有团队在和它合作开发针对罕见病的治疗方案。
但这只是冰山一角。背后的团队还在推进更底层的基础设施:和其他机构合作扩充蛋白质结构数据库,让AI能学到更多“锁”的样子;开发高性能仿真工具,在计算机里就能模拟药物在人体内的作用,不用再反复在动物身上做实验。这些动作指向的是一个更宏大的目标:用AI重构整个生命科学的研究范式。
过去的生命科学研究,更像在黑暗里摸石头过河——先观察现象,再猜背后的机制,最后用实验验证。而AI的加入,让我们能直接从“需求”出发,反向推导“解决方案”:想要治疗某种病,就直接设计能阻断致病通路的蛋白质,再验证它的效果。这不是对传统研究的补充,而是从“发现”到“创造”的转向。
当AI能直接生成蛋白质的序列和结构,我们其实是在重新定义“生命设计”的边界。过去我们只能在自然给的蛋白质库里挑选、修改,现在我们能像搭乐高一样,根据需求凭空创造新的生物分子。
“从发现生命,到设计生命。” 这句话正在从科幻变成现实。当然,这条路还很长:我们还没完全搞懂蛋白质的所有规律,AI的设计也依然需要实验的验证,甚至还有伦理和安全的问题需要解决。但不可否认的是,当AI能一步画出蛋白质的完整画像,药物研发的速度、生命科学的想象力,都已经被推到了一个新的高度。