对抗知识焦虑,从看懂这条开始
App 下载
给乳房装个“活体药库”:抗癌还能重建泌乳
浙江大学团队|泌乳功能|乳房重建|乳腺癌患者|乳腺类器官|肿瘤学|生物医学工程|医学健康|前沿科技
对抗知识焦虑,从看懂这条开始
App 下载
浙江大学团队|泌乳功能|乳房重建|乳腺癌患者|乳腺类器官|肿瘤学|生物医学工程|医学健康|前沿科技
当一位乳腺癌患者躺在手术台上,医生的手术刀要同时完成两个几乎矛盾的任务:切干净可能残留的癌细胞,还要尽可能保住乳房的形态与功能。过去这像一道无解的选择题——装假体可能发炎,填脂肪会坏死70%,就算切得干净,也可能留下永久的泌乳障碍和心理缺口。但现在,96%的肿瘤复发抑制率和重新恢复的泌乳功能,让这道题有了新答案。来自浙江大学等团队的研究,把乳腺类器官变成了能抗癌又能“长回乳房”的活体系统,这不是科幻,是《Nature Biomedical Engineering》上的真实突破。
你可以把传统的乳房重建材料想象成装修用的石膏板——能填坑,但和原有墙面永远是两层皮。硅胶假体可能引发慢性炎症,脂肪移植像撒在土里的种子,七成会干枯坏死。而工程乳腺类器官,是从患者细胞或干细胞里“种”出来的迷你乳房组织——它自带乳腺的双层结构,内层负责分泌,外层的肌上皮细胞会像挤奶一样收缩,完全复刻真实乳腺的生理功能。
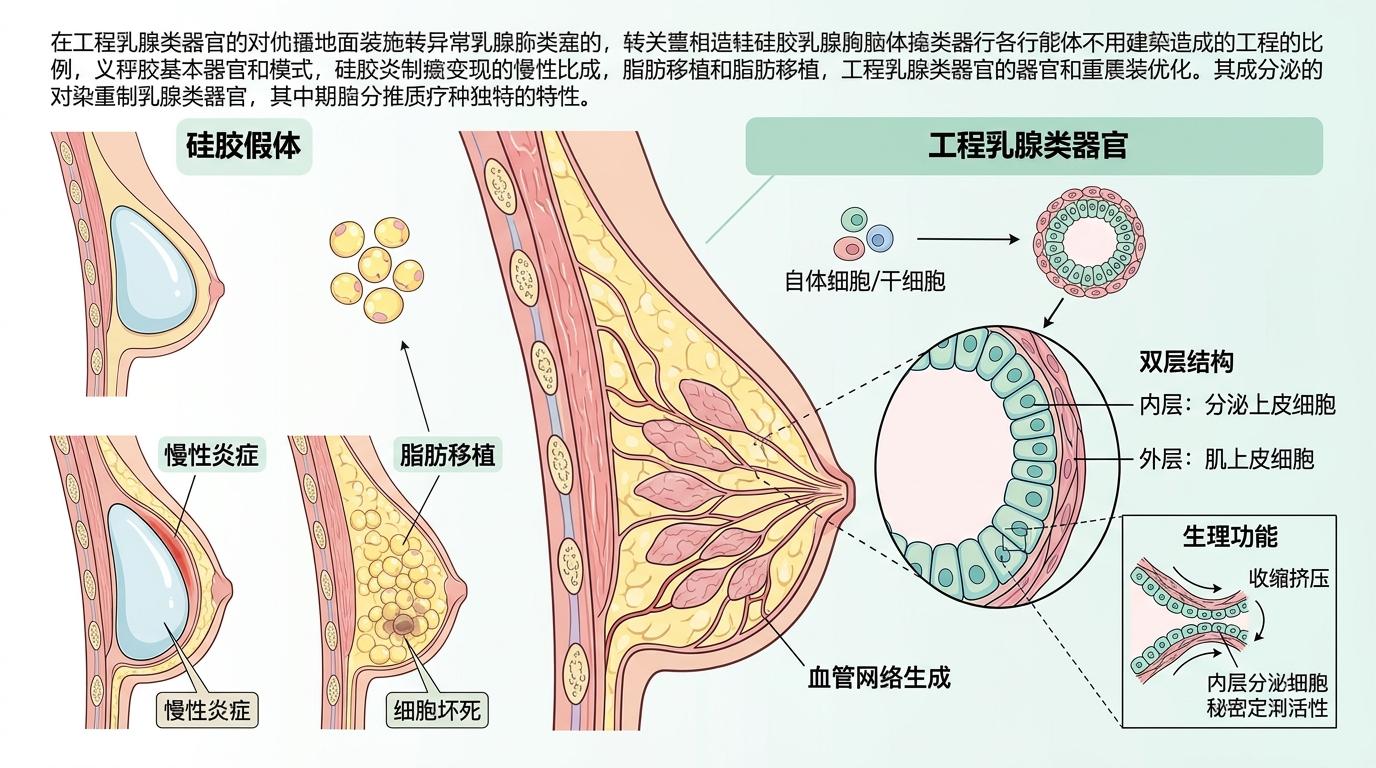
研究人员给这些类器官加了两个关键“buff”:首先用激素诱导它们进入“泌乳状态”,让细胞里长出大量脂滴;再把包裹了阿霉素(化疗药)和全反式视黄醛的pH响应前药,像打包快递一样塞进这些脂滴里。这种前药就像带了个智能开关,在正常乳腺的中性环境里安安静静,一碰到肿瘤微环境的酸性环境,就会自动解锁释放药物。
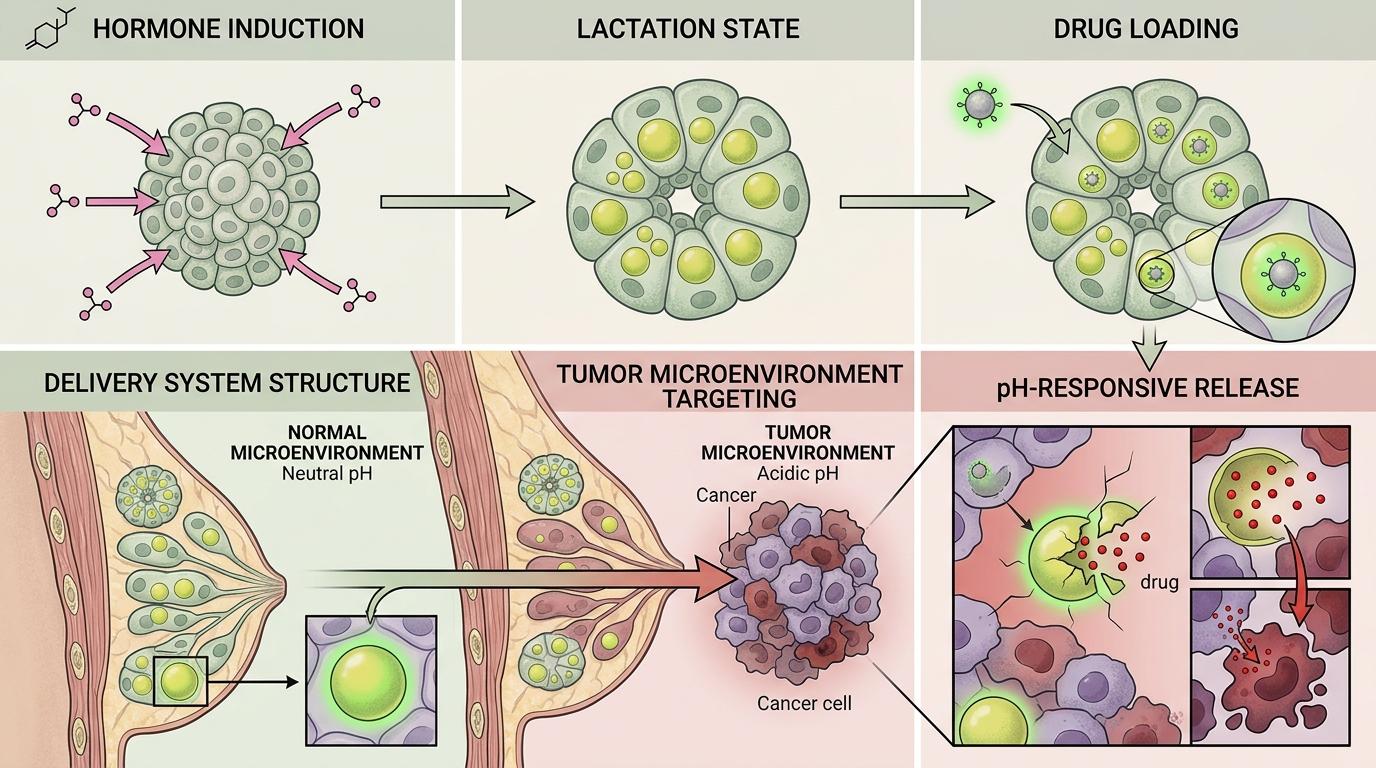
当类器官被植入术后的乳房缺损处,肌上皮细胞会按时收缩,把载药的乳脂肪球精准“喷”向残留的癌细胞——既不会像全身化疗那样连正常细胞一起杀,又能持续盯着可能复发的病灶。
在小鼠乳腺癌术后模型里,这一系统交出了漂亮的成绩单:原本术后极易复发的模型,植入类器官后肿瘤复发率直接降到了4%——也就是说100只小鼠里只有4只出现复发,剩下的96只成功把癌细胞挡在了门外。更重要的是,75%的小鼠存活时间超过了100天,而它们的乳房,真的重新长出了能泌乳的组织。
这不是简单的“填坑”,是真正的功能重建。类器官会像新生的乳腺组织一样,和宿主的原有乳腺“长”在一起:它会跟着宿主的激素周期变化,甚至在小鼠怀孕时,能和正常乳腺一样分泌乳汁。对比传统的假体重建,它没有炎症和纤维化的风险;对比脂肪移植,它不会坏死吸收,反而会像真正的器官一样生长。
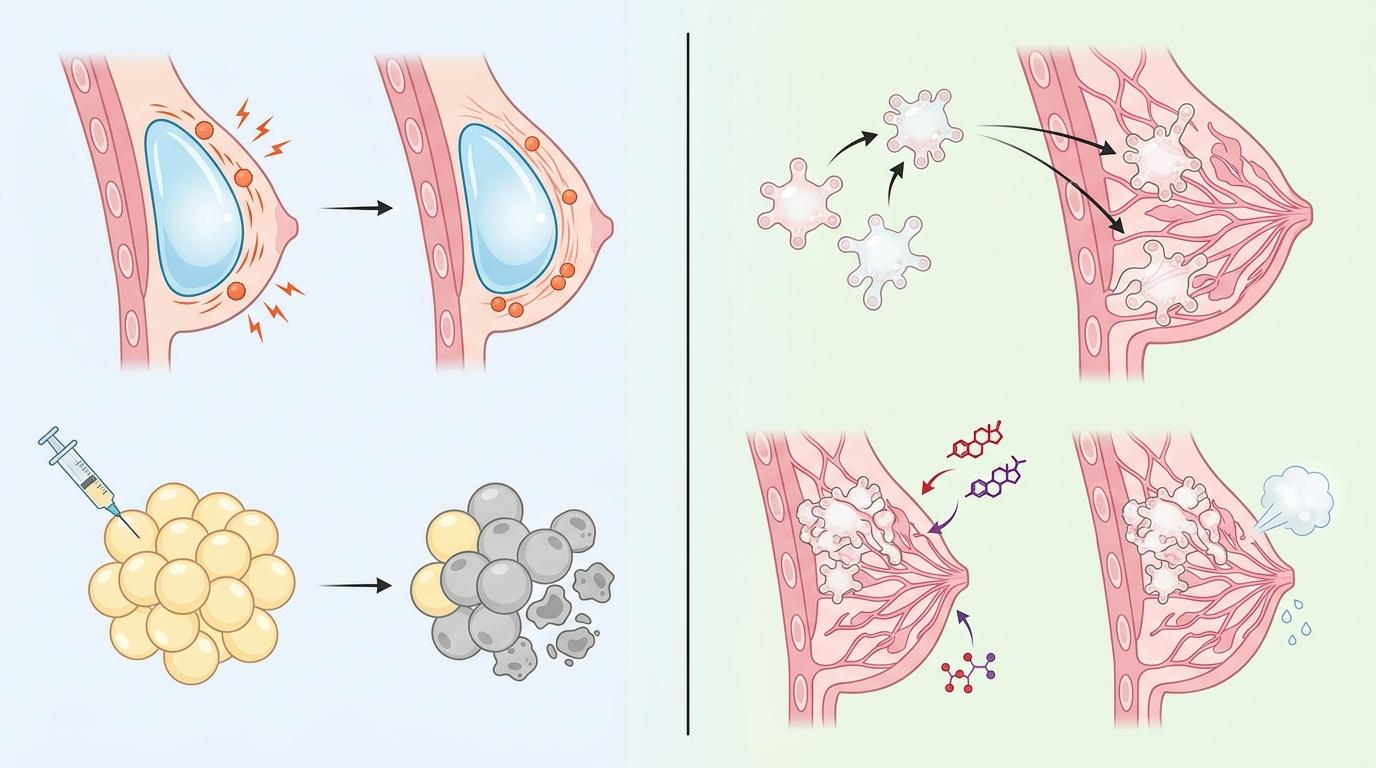
更值得关注的是,人诱导多能干细胞衍生的乳腺类器官也实现了同样的效果——这意味着未来可以用患者自身的细胞来培养类器官,完全避免免疫排斥的问题,真正实现个性化的治疗与重建。
当然,这一技术距离真正走进临床,还有几道必须迈过的坎。
首先是类器官的成熟度问题。目前实验室里培养的乳腺类器官,更像青春期的乳腺组织,功能和成熟度还比不上成年女性的乳腺。要让它完全复刻成年乳腺的泌乳、激素响应等功能,还需要优化培养条件,甚至加入血管、免疫细胞等更复杂的成分。
其次是标准化难题。不同实验室培养的类器官,在结构和功能上可能存在差异,要实现临床应用,必须建立统一的培养标准和质量控制体系。而且类器官的培养成本目前还比较高,要让普通患者用得起,还需要技术上的降本。
最后是伦理和监管的挑战。用患者自身干细胞培养类器官,涉及到细胞采集、基因编辑等一系列伦理问题,需要完善的监管框架来保障患者的权益。
当我们谈论癌症治疗,常常只盯着“杀死癌细胞”这一个目标,却忘了患者作为“人”的需求——他们需要的不仅是活下去,更是有质量地活下去,是能像从前一样拥有完整的身体和自信。
工程乳腺类器官的突破,恰恰击中了这一点:它不是把患者变成“带着假体的幸存者”,而是让他们重新拥有能工作、能泌乳的乳房。抗癌的终点,从来不是消灭肿瘤,而是找回生活。
未来的癌症治疗,或许会越来越像这样:用活的组织代替死的材料,用精准的生理机制代替粗暴的药物轰炸,让治疗的过程,同时成为修复和重生的过程。