
21 天前

21 天前
当一位多发性硬化症患者拿起杯子时,他的手可能会不受控制地颤抖——这不是因为肌肉无力,而是因为免疫系统错误攻击髓鞘后,大脑里的神经元正在悄悄死亡。过去30年,人类已经有十多种FDA批准的疗法能挡住免疫系统的进攻,却拦不住这场“免疫攻击后的余震”。直到约翰斯·霍普金斯大学的实验室里,一群研究人员在小鼠的脊髓切片里,发现了一条藏在神经元死亡背后的隐秘通路。为什么免疫炎症平息后,神经元还在持续死去?这个困扰了学界数十年的问题,终于有了新的答案。
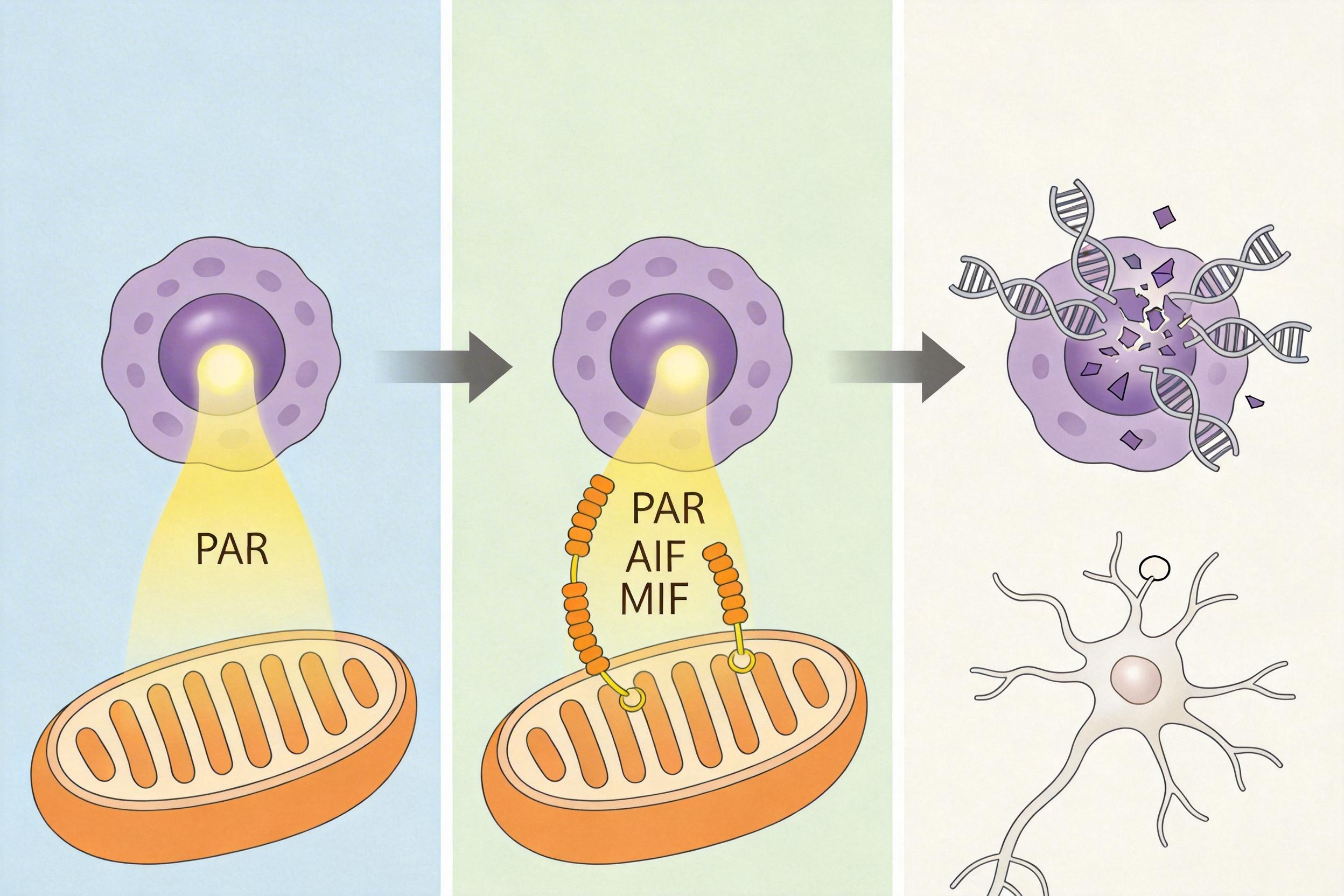
你可以把神经元想象成一座精密的信号站,DNA是它的核心指挥室。当免疫炎症引发的氧化应激像炸弹一样炸开,指挥室的墙壁(DNA)出现裂缝,这时一种叫PARP-1的酶会紧急启动——它本来是负责修补DNA的“维修工”,但当损伤过于严重,它会彻底失控,疯狂合成一种叫PAR的聚合物。
这不再是维修信号,而是自杀指令。
PAR会从细胞核逃到线粒体,拽着原本负责能量供应的AIF蛋白离开岗位,一起钻进细胞核。更关键的是,它们还会带上一个叫MIF的“刽子手”——这个原本调控免疫的蛋白,此刻会激活隐藏的核酸酶活性,像剪刀一样把DNA剪成大片段,最终让神经元彻底停止工作。这就是parthanatos,一种区别于凋亡、坏死的新型程序性死亡,它不是免疫系统的直接攻击,而是神经元在损伤后的“自我了断”。
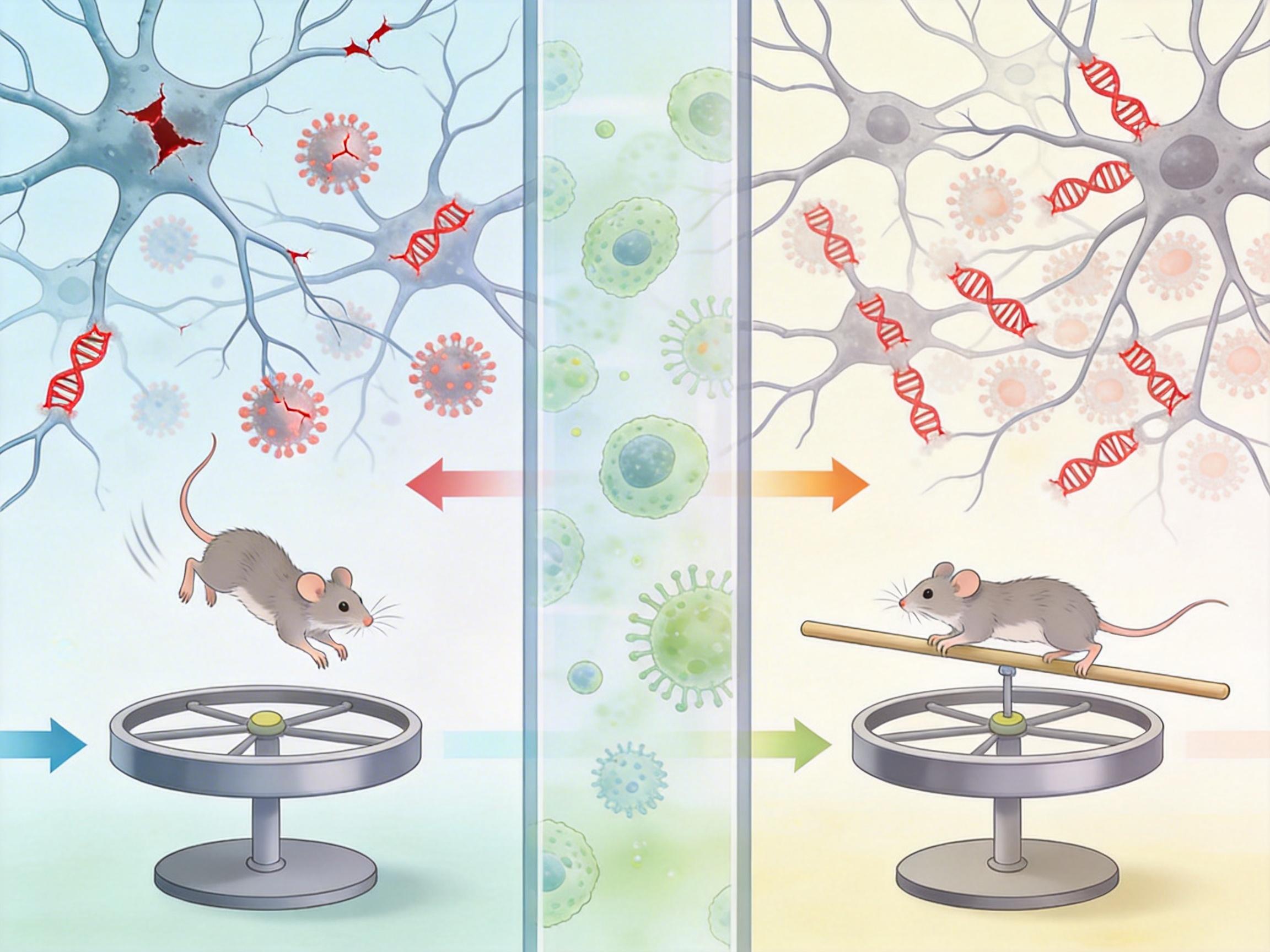
研究人员在实验性自身免疫性脑脊髓炎(EAE)小鼠模型中验证了这个猜想:他们给小鼠注射了能特异性阻断MIF核酸酶活性的小分子抑制剂PAANIB-1,结果令人惊讶——
神经元的DNA断裂标志物减少了60%,存活率提高了40%,小鼠在旋转杆测试中的运动时间延长了30%以上。更重要的是,这种抑制剂完全不影响免疫系统的正常功能,既不会削弱现有免疫疗法的效果,也不会让患者更容易感染。
这是一个关键的突破:过去的MS疗法都在“拦着免疫系统打人”,而现在我们可以直接“把被打晕的神经元救回来”。对比传统免疫疗法只能减少复发,这种下游干预能直接阻止神经元的退行性死亡——就像火灾扑灭后,不再只是防止复燃,而是抢救还没完全烧毁的建筑。
更值得关注的是,parthanatos通路不仅存在于MS中,在帕金森病、脑外伤、阿尔茨海默病等多种神经损伤疾病中都有激活,这意味着MIF抑制剂可能成为一种广谱的神经保护药物。
当然,这项研究还远不是终点。
首先,小鼠模型的成功不等于人类临床有效。虽然研究人员在MS患者的脑组织中检测到了PAR积累和MIF激活,但人体的神经炎症环境比小鼠复杂得多,抑制剂的血脑屏障穿透性、剂量安全性都需要进一步验证。
其次,MIF是个“多面手”,它同时调控免疫反应、细胞存活和细胞死亡,特异性阻断其核酸酶活性而不影响其他功能,需要更精准的药物设计——如果不小心关掉了它的免疫调控功能,反而可能引发新的问题。
最后,神经退行性损伤是一个多通路交织的过程,parthanatos可能只是其中之一。研究人员已经计划探索它和铁死亡的交叉作用,未来的治疗可能需要联合多种通路抑制剂,才能真正阻止神经元的死亡。
当我们把目光从免疫系统的“前线战场”转向神经元的“后方救援”,其实是在重新定义神经免疫疾病的治疗逻辑:我们不仅要阻止攻击,更要学会修复。30年的免疫研究让我们能挡住子弹,而parthanatos通路的发现,让我们第一次摸到了子弹击中后,拯救神经元的那扇门。
治疗的终点,从来不是战胜疾病,而是留住功能。 未来的某一天,当MS患者能稳稳拿起杯子时,我们或许会想起,这场跨越三十年的研究,最初只是为了回答一个简单的问题:为什么炎症平息后,神经元还在死去?
点击充电,成为大圆镜下一个视频选题!