内容由AI生成,思考得你完成
App 下载
内容由AI生成,思考得你完成
App 下载
在我们身体深处,蜿蜒的肠道被誉为“第二大脑”。这个拥有数亿神经元的复杂网络,不仅负责消化,还寄居着数万亿的微生物房客。长久以来,我们认为大脑是身体至高无上的指挥官,但如果,一场发生在大脑中的“风暴”——癫痫,其开关竟部分掌握在千里之外的肠道微生物手中,这听起来是否像天方夜谭?
对于全球数千万癫痫患者,尤其是那些占10%-30%的难治性癫痫患儿来说,常规药物的失效意味着一场漫长而无望的战斗。当大脑的电路陷入混乱,反复的异常放电夺走他们的童年与未来时,医学界一直在寻找新的突破口。现在,一束光似乎正从最意想不到的地方照来。
2026年1月16日,顶级期刊《Neuron》刊登的一项研究,为这场战斗带来了颠覆性的希望。由中国科学院深圳先进技术研究院的刘欣安、陈祖昕团队与深圳市儿童医院的操德智团队联合完成的研究,精准地揭示了一条前所未见的“肠-脑”秘密通路。
他们的核心发现是:一种名为**脆弱拟杆菌(Bacteroides fragilis)**的肠道细菌,能够通过一条特定的神经信号通路,有效抑制癫痫发作。这不仅是一个有趣的关联,研究人员更是完整地描绘出了这条信号通路的“地图”,从肠道中的一个特定细胞,经由一条关键的神经“高速公路”,直达大脑,从而平息神经元的异常活动。这一发现,实现了从临床观察到机制解析,再回到临床验证的完美闭环,为开发无副作用的微生物疗法奠定了坚实的科学基础。
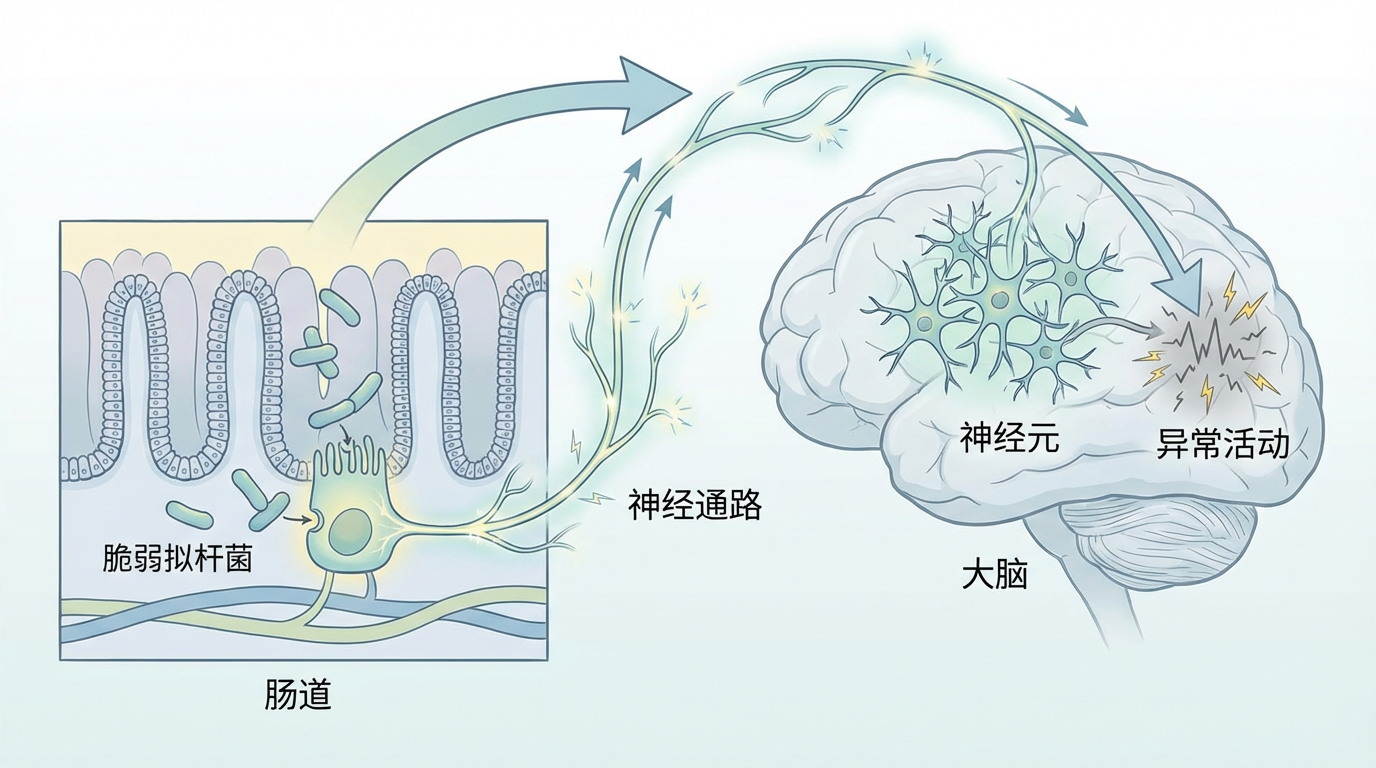
这项研究的精妙之处在于,它像一位密码破译专家,详细解读了脆弱拟杆菌是如何向大脑发送“停火”信号的。整个过程如同一部高效的情报传递系统:
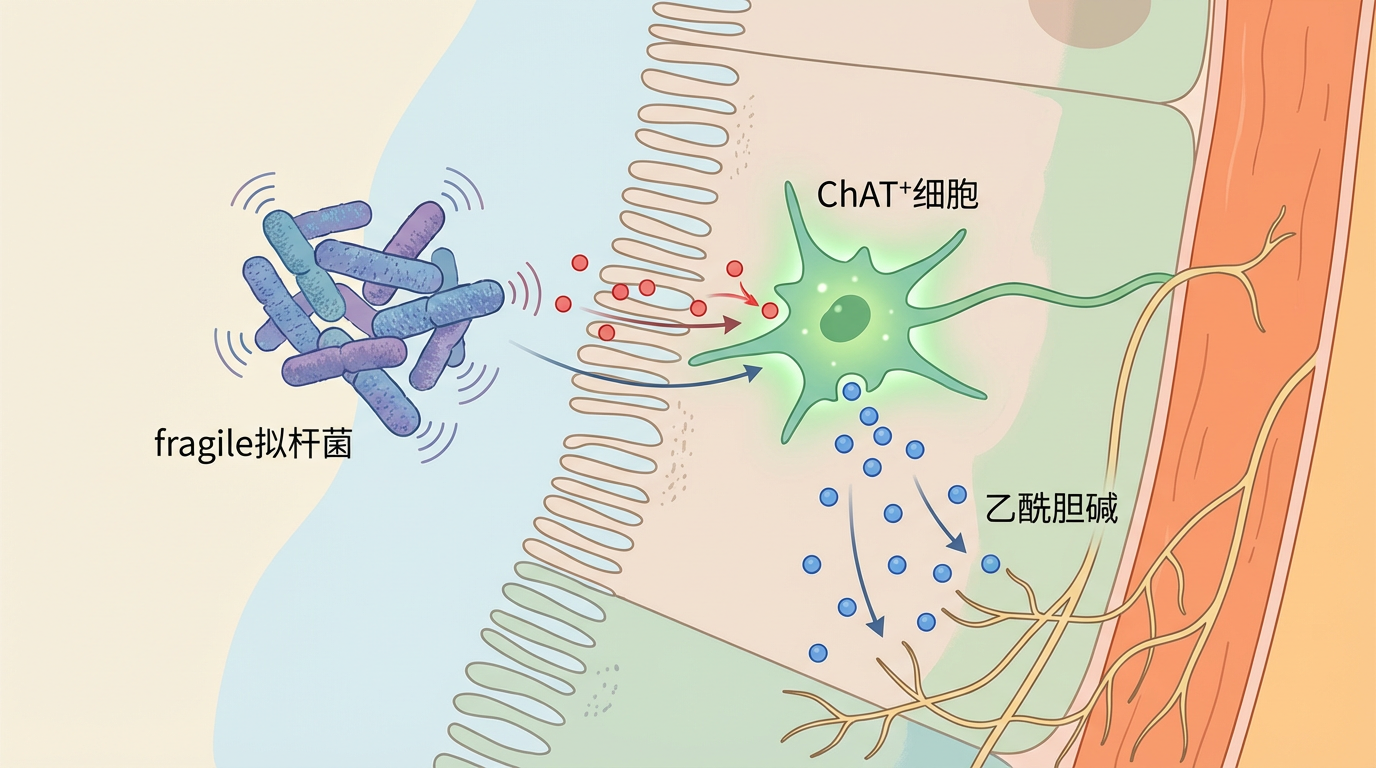
更有趣的是,脆弱拟杆菌并非孤军奋战。研究还发现,它的抗癫痫效果需要肠道内另一类益生菌——乳酸杆菌的协同配合。两者如同战友,共同创造了一个有利于信号产生的肠道微环境,放大了抗癫痫的效果。这一发现,在后续的临床试验中也得到了印证:那些对脆弱拟杆菌治疗反应良好的患儿,其肠道内乳酸杆菌的水平也更高。
这项发现并非仅仅停留在小鼠实验。研究团队进行了一项针对60名难治性癫痫患儿的随机双盲对照临床试验。结果令人振奋:
更早的一些临床研究也展示了相似的希望。例如,广州医科大学附属第二医院邓宇虹团队的研究曾发现,使用脆弱拟杆菌BF839辅助治疗难治性癫痫,有效率可达61%,并且能显著改善认知、情绪和睡眠等共患病。这些来自真实世界的数据,为肠道菌群干预从一个前沿概念,转变为一种可行的临床策略,提供了强有力的证据。
尽管前景光明,但通往标准化微生物疗法的道路并非一帆风顺。最大的挑战,源于我们每个人肠道微生态的巨大个体差异。
人类的基因组相似度高达99.9%,但肠道菌群的构成却千差万别,如同独一无二的“指纹”。饮食习惯、生活环境、遗传背景乃至用药史,都在塑造着这个微型生态系统。这意味着,同一种益生菌,在不同患者体内可能面临完全不同的“土壤环境”,其定植能力和功效也会大相径庭。
这就解释了为何益生菌疗法的效果时好时坏,难以预测。大多数机制研究仍依赖动物模型,而这些模型无法完全模拟人类肠道的复杂性和多样性。因此,如何为患者精准“匹配”最适合他们的益生菌或菌群组合,是横亘在科研人员面前的一道核心难题。我们需要的,不仅仅是“一种”益生菌,而是一套个性化的“生态处方”。
脆弱拟杆菌的故事,为癫痫乃至更广泛的神经系统疾病治疗打开了一扇全新的大门。它预示着一个新时代的到来——我们不再仅仅关注大脑本身,而是将身体视为一个相互关联的整体生态系统。
未来的研究将朝着更加精准和个性化的方向发展:
从遥远的肠道到精密的大脑,一条由微生物铺设的神经通路正被逐渐照亮。这不仅是对癫痫治疗的一次重大突破,更是对人类健康认知的一次深刻革命。它提醒我们,那些与我们共生的微小生命,或许正以我们难以想象的方式,深刻地影响着我们的心智与命运。