对抗知识焦虑,从看懂这条开始
App 下载
红细胞丢了生产线,竟靠“共享血红素”活命
Iqbal Hamza团队|线粒体丢失|血红蛋白合成|血红素转运|红细胞成熟|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
Iqbal Hamza团队|线粒体丢失|血红蛋白合成|血红素转运|红细胞成熟|分子细胞生物学|生命科学
想象一下:你正在赶制一批急需的订单,突然工厂的核心车间被拆走了——这就是红细胞成熟时面临的绝境。为了给装氧气的血红蛋白腾地方,红细胞前体必须扔掉线粒体,而线粒体恰恰是制造血红素的唯一工厂。血红素是血红蛋白的核心原料,没有它,红细胞就是个空壳。这个困扰学界几十年的悖论,直到马里兰大学Iqbal Hamza团队的新研究才终于有了答案:红细胞根本没打算自己硬扛,它会“借”血红素。
我们先把血红素的来龙去脉说清楚:它是个含铁的小分子,像个小磁铁,专门负责抓氧气。红细胞前体在成熟的最后一步,会把包括线粒体在内的所有细胞器全扔掉——就像为了装更多货物,把货车的驾驶室、发动机全拆了。但问题是,线粒体是合成血红素的唯一车间,没有车间,怎么造出组装血红蛋白需要的海量血红素?
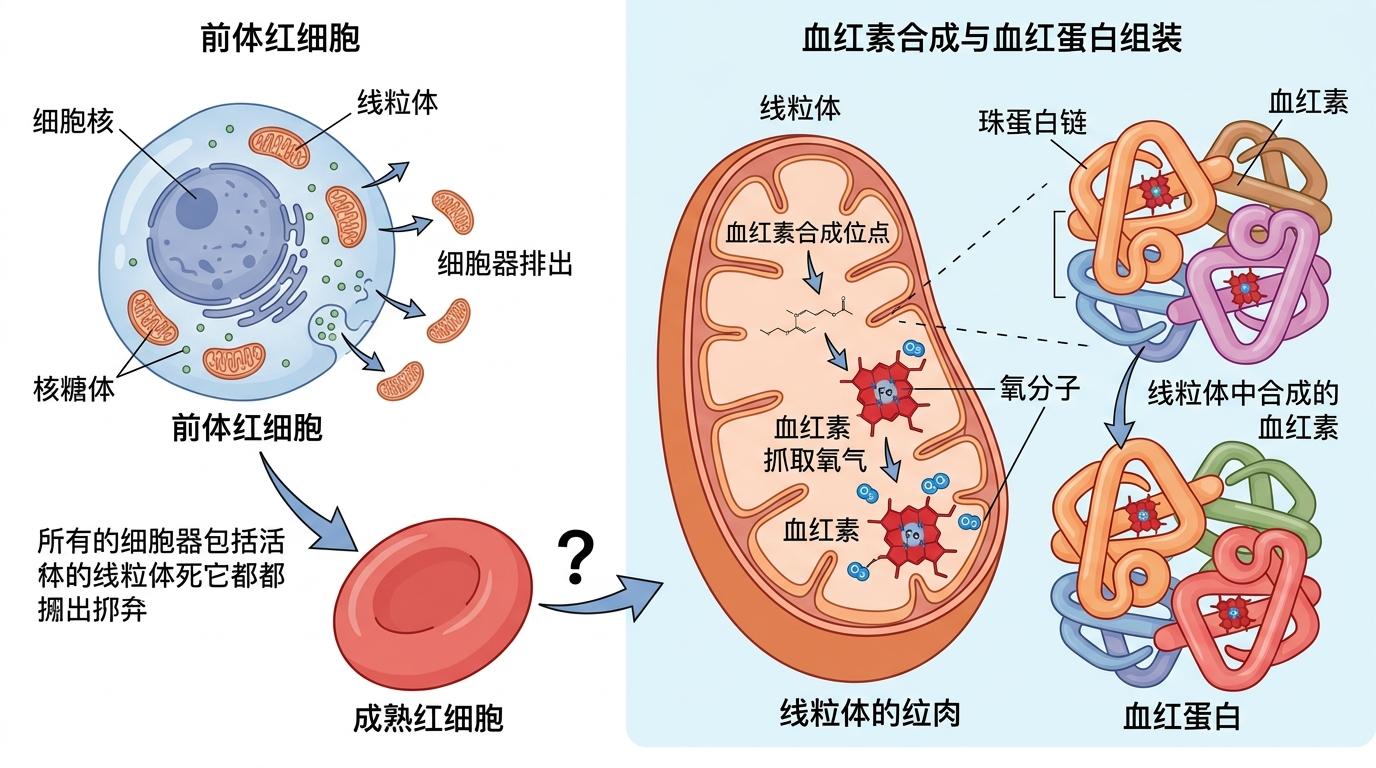
传统教科书说,每个细胞都得自己合成血红素。但红细胞的情况明显说不通:拆了车间的前体,在接下来的几天里,要把血红蛋白的产量翻几十倍,所需的血红素是平时的几百倍。Hamza团队用单细胞测序盯着这些“拆了车间”的前体,终于发现了关键线索:一种叫HRG1的蛋白,在应激状态下的红细胞前体里,表达量突然飙升了几十倍。
HRG1是什么?你可以把它看成细胞表面的“快递收件口”,专门负责把外面的血红素“运”进细胞里。
为了验证HRG1的作用,研究团队做了个基因敲除实验:把小鼠体内的HRG1基因去掉一部分,然后让这些小鼠经历急性失血——这是最典型的“应激造血”场景,身体需要在几天内造出大量新红细胞。
结果很明确:缺失HRG1的小鼠,在失血后根本造不出足够的成熟红细胞,血红蛋白含量直接跌到了正常水平的一半,出现了严重贫血。而正常小鼠的红细胞前体,会通过HRG1从周围细胞“借”血红素——这些血红素一部分来自巨噬细胞吞噬衰老红细胞后回收的“二手货”,一部分来自其他仍保留线粒体的细胞合成的“新品”。
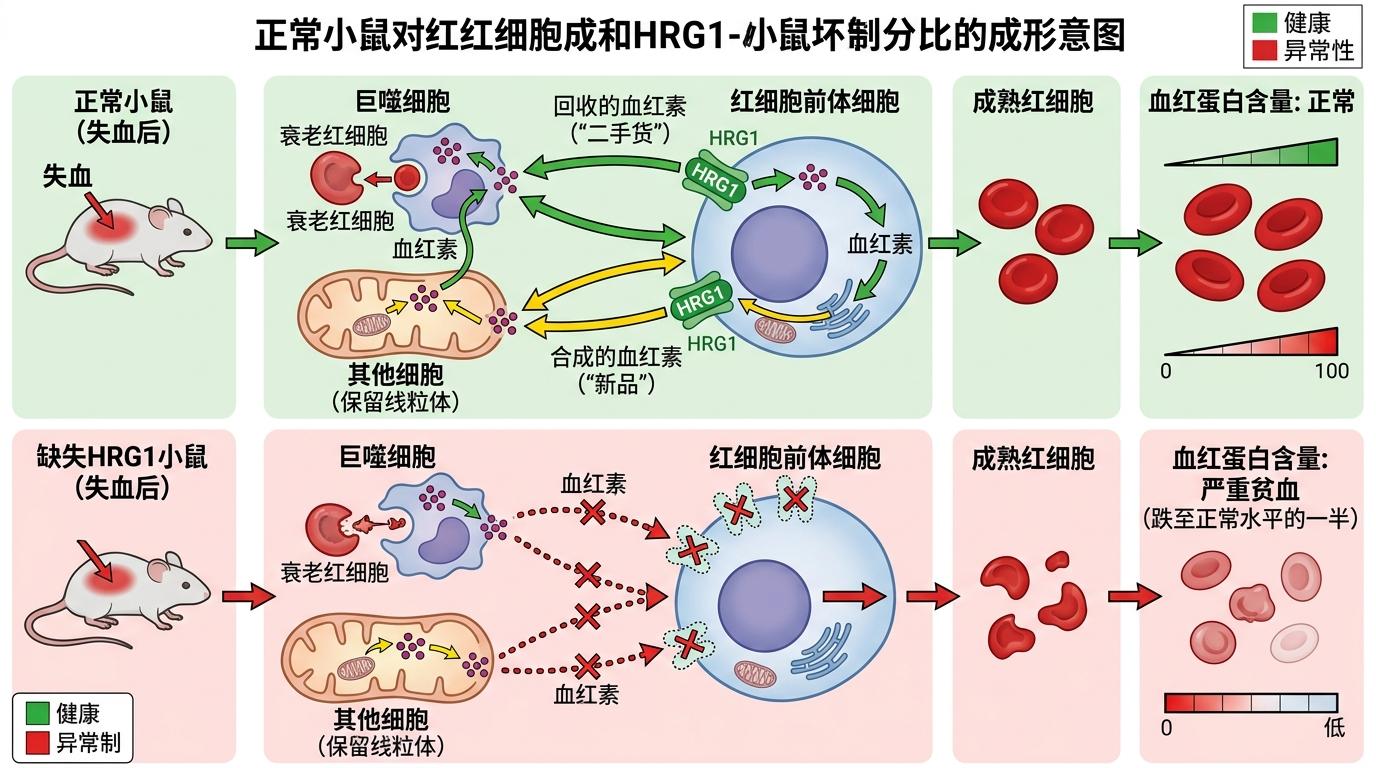
这就像一个应急供应链:平时每个工厂自己生产,一旦遇到紧急订单,附近有产能的工厂就会共享原料,保证最急需的生产线不停工。红细胞前体就是那个急需原料的生产线,HRG1就是它的原料进口通道。
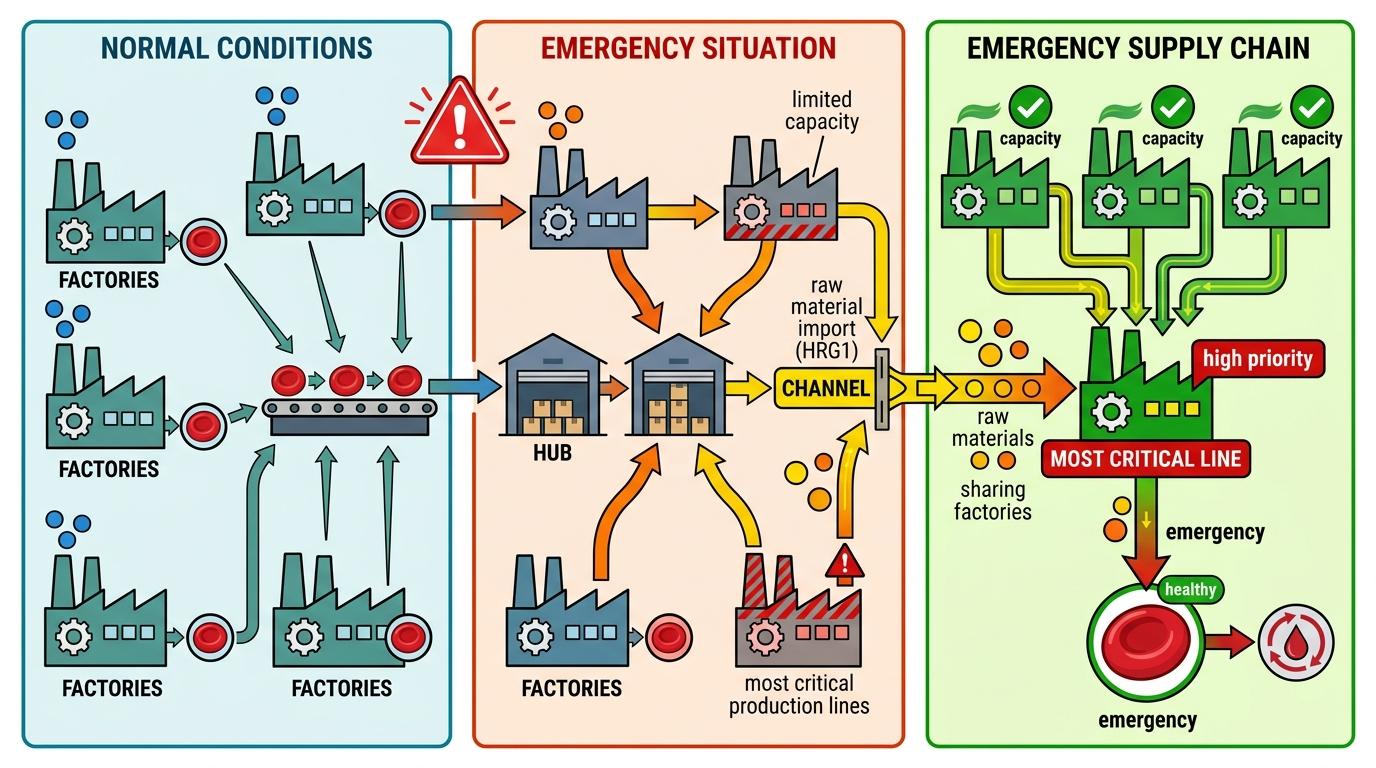
更关键的是,这个机制只在应激状态下启动——比如急性失血、严重缺氧时。平时红细胞前体还是靠自己的线粒体合成血红素,只有当身体急需大量红细胞时,才会开启“共享模式”。
这个发现不止是改写教科书,更给贫血治疗找到了新方向——尤其是β-地中海贫血这种棘手的遗传病。
β-地中海贫血患者的问题,是珠蛋白合成出了故障:β链造不出来,导致α链过剩,而多余的血红素会变成“毒素”,破坏红细胞前体,造成“无效造血”——看起来在造红细胞,其实都是不合格的废品。
研究团队在β-地中海贫血的小鼠模型里做了个实验:适度降低HRG1的活性,减少红细胞前体“借”来的血红素。结果出乎意料:小鼠的贫血症状明显减轻了,成熟红细胞的数量增加了30%,无效造血的情况也得到了缓解。
原因很简单:适度减少血红素的输入,让血红素和珠蛋白的比例重新平衡了——就像给一个原料过剩的生产线减原料,反而能造出合格的产品。但这里的关键是“适度”:如果完全敲除HRG1,会影响巨噬细胞回收血红素,导致新的问题。
当然,这个靶点还处于早期研究阶段:目前还没有专门调节HRG1的药物,也不知道长期调控HRG1会不会有副作用。但至少,我们终于给β-地中海贫血这种“无药可治”的遗传病,找到了一个新的突破口。
我们总以为细胞是一个个独立的“工厂”,自给自足,各自为政。但红细胞的这个“共享机制”,却打破了这种认知:细胞之间其实存在着一套精密的互助系统,在紧急时刻互相支援,保证整个机体的正常运转。
科学的进步往往就是这样:从一个看起来“无解”的悖论出发,一点点撬开自然界的秘密。HRG1的发现,不仅让我们重新理解了红细胞的生成,更给数百万贫血患者带来了新的希望。
细胞不独行,生命是一场集体协作。