对抗知识焦虑,从看懂这条开始
App 下载
1张切片搞定16种检测,稀有肿瘤诊断不再卡壳
肿瘤微环境空间图谱|原发性中枢神经系统弥漫大B细胞淋巴瘤|海南大学|Dumi装置|肿瘤学|生物医学工程|医学健康|前沿科技
对抗知识焦虑,从看懂这条开始
App 下载
肿瘤微环境空间图谱|原发性中枢神经系统弥漫大B细胞淋巴瘤|海南大学|Dumi装置|肿瘤学|生物医学工程|医学健康|前沿科技
当医生面对原发性中枢神经系统弥漫大B细胞淋巴瘤这类稀有肿瘤时,手里的组织切片往往只有寥寥几张——既要用来做病理分型确诊,又要分析肿瘤微环境找治疗靶点,就像攥着半块面包,既要当正餐又要当点心,怎么分都不够。传统免疫组化一次只能测一种标志物,染完几张切片,关键信息还没凑齐,样本先耗光了。
现在,海南大学的团队把这个死局给破了。他们研发的Dumi装置,能用1到2张切片完成16种标志物的并行检测,还能画出整张切片的肿瘤微环境空间图谱。这不是简单的提速,而是给稀有肿瘤的诊断和研究,打开了一扇用有限样本挖尽所有信息的门。为什么这个装置能做到这么极致的样本利用?
你可以把Dumi装置想象成一个能快速变形的实验室工作台:它把三维打印的流体交换结构和两层微流控芯片拼在一起,通过气阀的压力变化,就能在两种模式里无缝切换——
多通道模式下,16条平行的微通道像16个独立的小试管,各自装着不同的检测试剂,精准覆盖切片上的不同区域,一次就能同时检测16种肿瘤标志物。这就像用16支笔在同一张纸上的不同地方同时写字,既不串色,又省了15张纸。
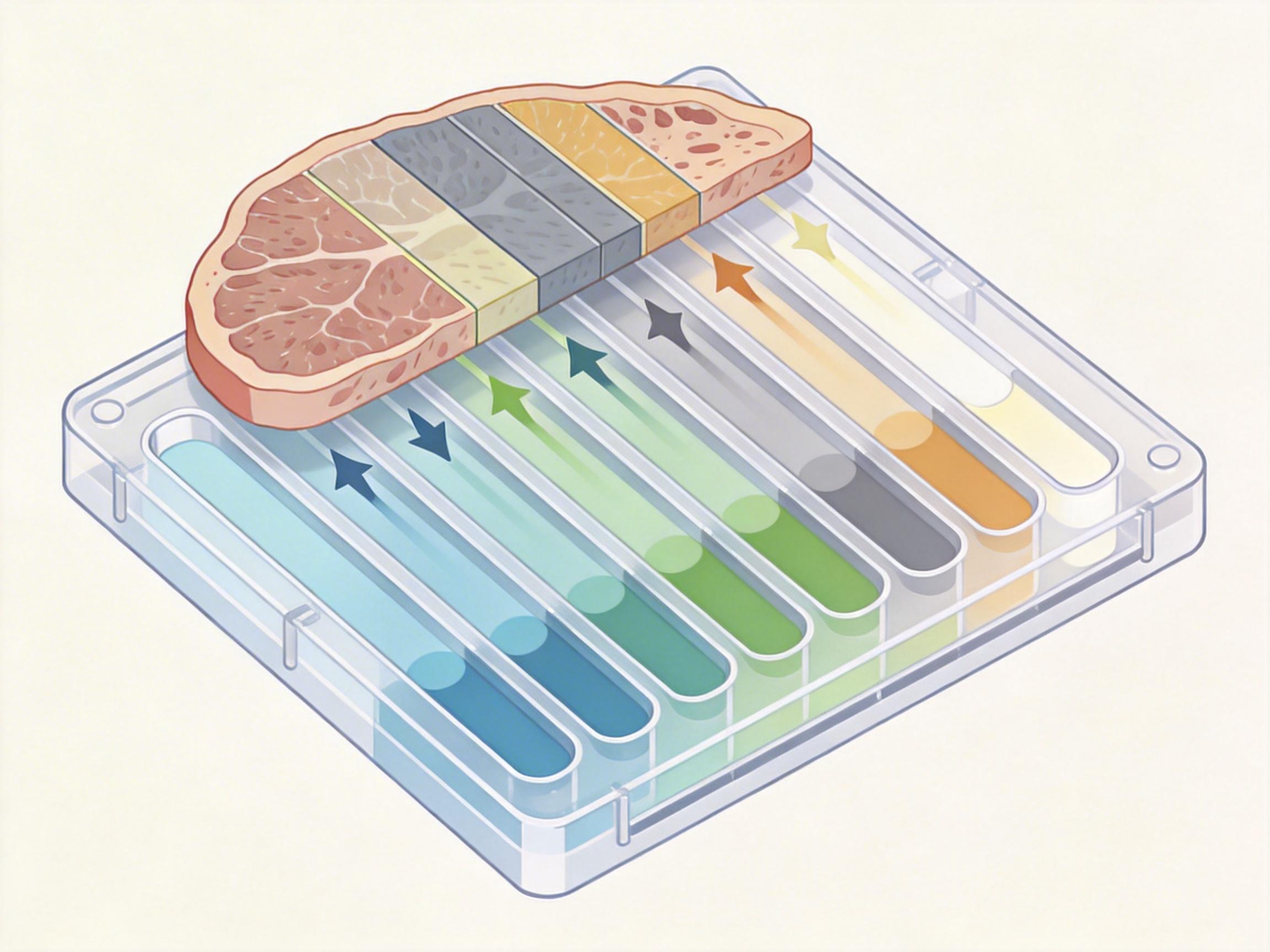
全腔室模式下,气阀切换压力,原本分隔的通道会变成一个覆盖整个切片的大腔室,配合循环多重免疫荧光技术,能给整张切片做一个“全景扫描”,把肿瘤细胞、免疫细胞、血管这些微环境元素的位置和相互关系都画出来,就像给肿瘤拍了一张带细胞级导航的卫星图。
最关键的是,两种模式不用换设备,不用重新处理样本,拧个气阀就能切换——这直接把“先诊断分型,再研究微环境”的两步流程,压缩到了同一张切片上。
传统免疫组化里,抗体孵育一次要1个多小时,不仅慢,还得用大量抗体把切片泡着,像给花浇水一样,大部分试剂都顺着切片流走了,真正用到组织上的没多少。
Dumi的微流控设计把这个逻辑给反过来了:它用精准控制的流速,让抗体溶液贴着切片表面快速循环,直接把抗体“推”到组织的抗原位点上,相当于给植物滴灌,精准又不浪费。团队反复优化了流速和孵育时间,把原本1小时的抗体孵育压缩到了10分钟量级,试剂消耗直接降了90%以上。
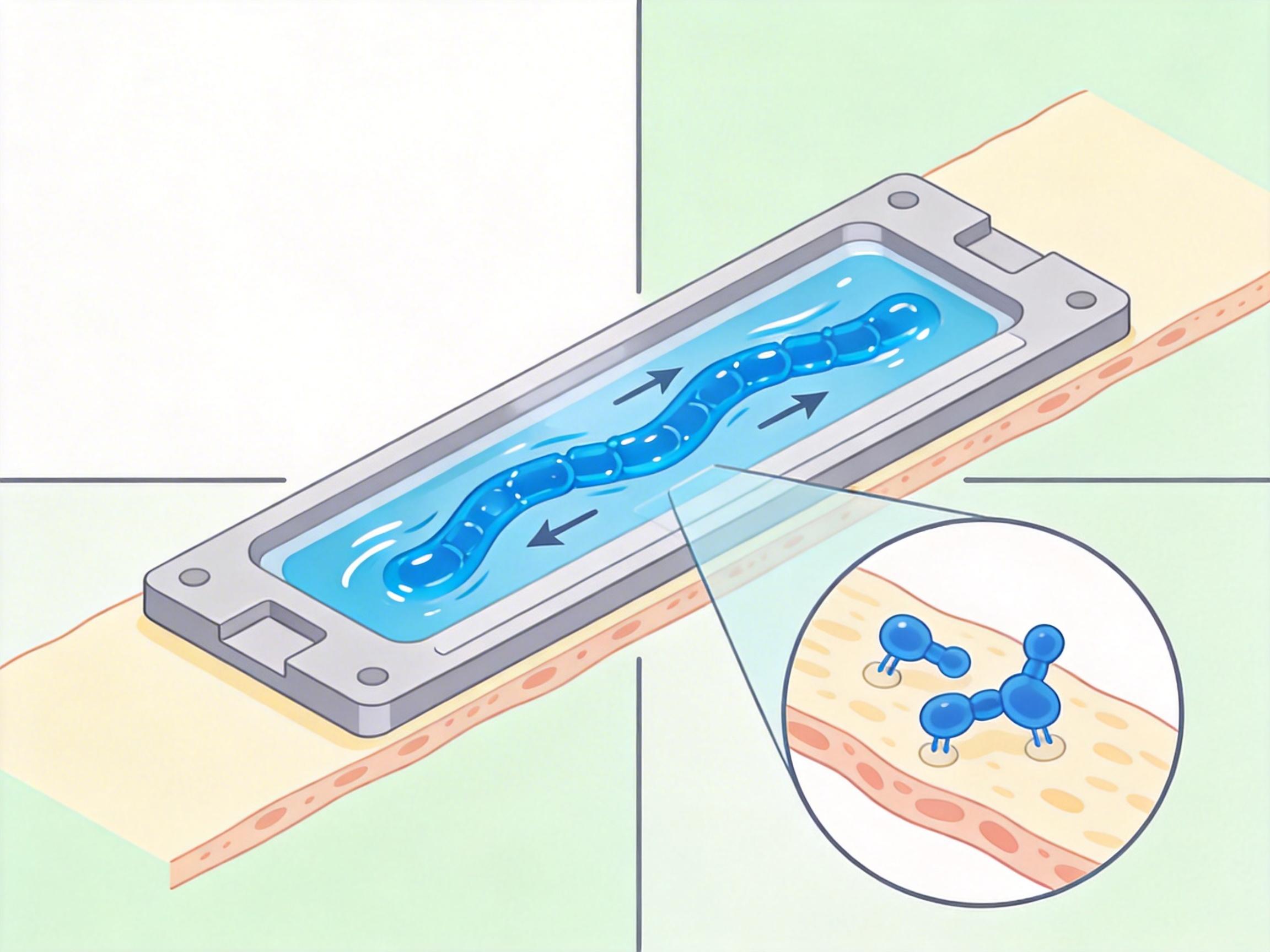
在4例弥漫大B细胞淋巴瘤样本的测试里,Dumi只用了1到2张切片,就完成了传统方法需要5到6张切片才能做的检测,诊断结果和传统病理完全一致。更重要的是,它还能在剩余的切片区域继续做微环境分析——对于那些只能通过手术取到一点点组织的稀有肿瘤来说,这不是省了几张切片,而是给后续的研究和治疗方案制定,多留了一次机会。
当然,它也不是完美的:目前的多通道模式只能覆盖切片的特定区域,还做不到全切片的多标志物并行检测;而且对于一些特殊的组织样本,比如质地过硬的纤维化组织,微流控的试剂循环效果还需要再优化。
过去,医生看肿瘤,就像看一张没有坐标的地图——知道有肿瘤细胞,知道有免疫细胞,但不知道它们在组织里是挨在一起,还是隔得很远。而肿瘤的免疫逃逸、治疗耐药,往往就藏在这些空间关系里。
Dumi的全腔室模式刚好补上了这个缺口。在那例原发性中枢神经系统弥漫大B细胞淋巴瘤的样本里,团队用循环多重免疫荧光技术,画出了肿瘤微环境的空间图谱,发现CD8+免疫细胞都聚集在血管周围,形成了一个“免疫排斥区”——免疫细胞明明就在旁边,却被血管挡在外面,没法攻击肿瘤细胞。这个发现,直接给后续的免疫治疗提供了新的靶点:能不能想办法打通这个血管屏障?
这也是Dumi最核心的价值:它不再是一个单纯的检测工具,而是能把诊断和研究连起来的桥梁——用同一份样本,既能确诊肿瘤类型,又能找到治疗的突破口,对于样本稀缺的稀有肿瘤来说,这种“一站式”的信息获取,可能就是患者的救命稻草。
我们总说精准医疗,精准的前提是能拿到足够的信息。对于稀有肿瘤患者来说,他们最缺的不是先进的治疗方案,而是用有限样本挖尽所有信息的技术——毕竟,连肿瘤的“底细”都没摸清楚,再先进的治疗也打不准靶点。
Dumi的出现,本质上是给“样本稀缺”这个无解的难题,找到了一个“效率优先”的解法:不是去寻找更多样本,而是把每一份样本的价值榨到极致。
有限样本,无限信息,才是稀有肿瘤的破局之道。