
1 个月前

1 个月前
一位晚期结直肠癌患者,腹腔里布满了转移的肿瘤病灶,已经试过4线治疗全部失败。医生没有再给他开静脉输液的化疗药,而是直接把改造后的免疫细胞打进了腹腔——就像给腹腔做了一次「局部免疫手术」。两周后,他腹腔里的肿瘤缩小了76%,而且没有出现传统CAR-T疗法常见的严重副作用。
这不是科幻场景,而是浙江大学联合重庆精准生物团队在《Nature Cancer》发表的一期临床结果。他们改造的这款名为PC13的CAR-T细胞,是全球首个在人体中验证有效的低氧响应型CAR-T。它解决了困扰CAR-T疗法十年的难题:为什么能治好血癌,却对实体瘤束手无策?
要理解PC13的厉害,得先搞懂传统CAR-T在实体瘤里的尴尬——就像一个没头苍蝇,在正常组织里乱撞消耗体力,到了肿瘤跟前已经累瘫了。
实体瘤不是一团软乎乎的癌细胞,它有自己的「防御系统」:内部因为血管跟不上生长速度,普遍处于低氧状态(氧分压不到正常组织的1/10),还堆满了抑制免疫细胞的「垃圾因子」。传统CAR-T细胞一进人体就持续激活,要么在正常组织里误伤无辜(也就是「脱靶毒性」),要么还没到肿瘤就提前耗竭失去战斗力。
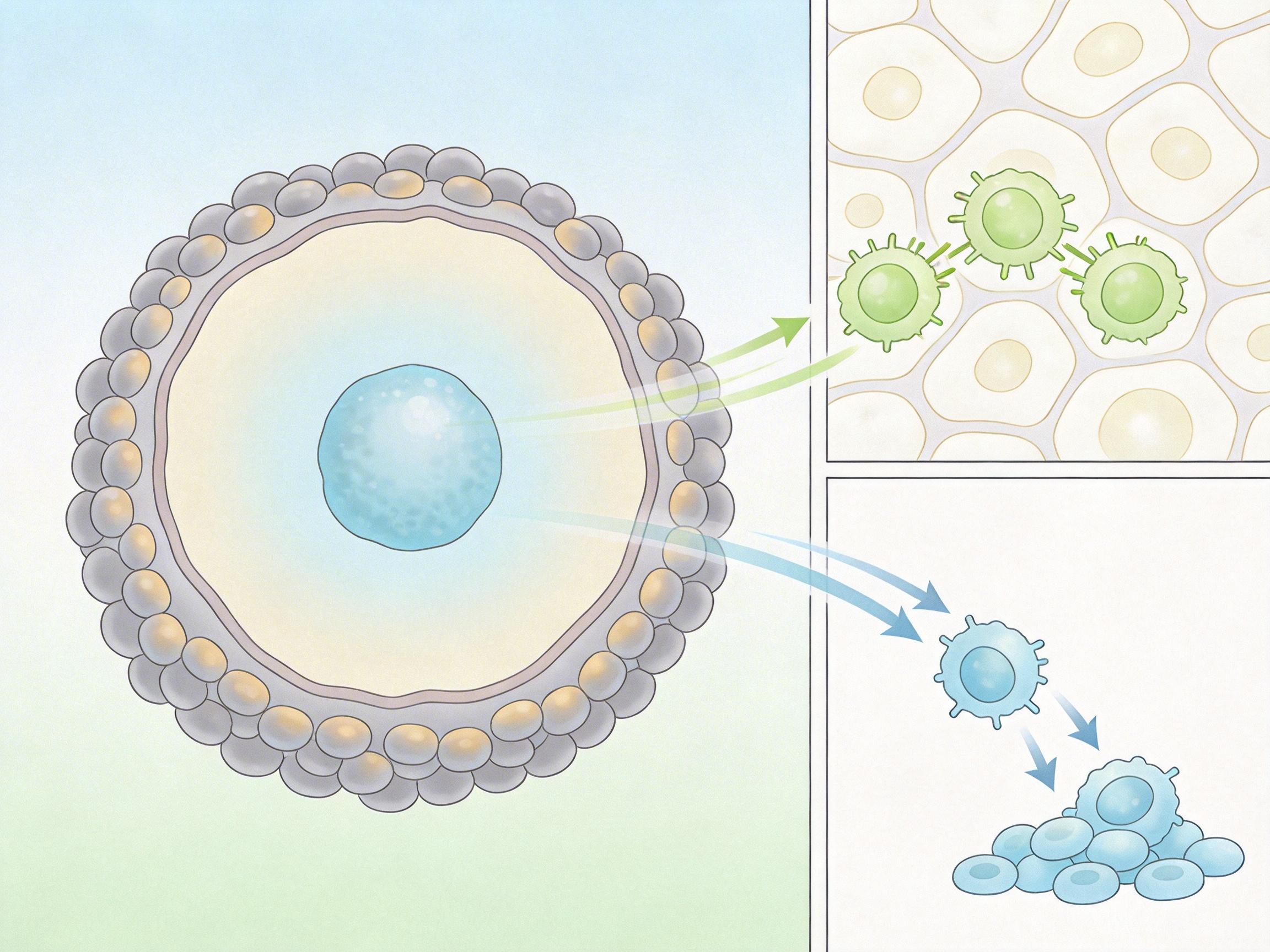
PC13的核心创新,是给CAR-T装了个「低氧开关」——用5个低氧响应元件(HRE)控制CAR蛋白的表达。你可以把它想象成一个只在地下室(低氧的肿瘤内部)才会亮起的灯泡:
更精准的机制是:正常氧环境下,HIF-1α(低氧诱导因子)会被快速降解,无法启动CAR基因的转录;而在低氧的肿瘤里,HIF-1α稳定下来,结合到低氧响应元件上,驱动CAR蛋白合成。这种「肿瘤局部激活,全身循环静默」的设计,直接解决了传统CAR-T的两大死穴:脱靶毒性和提前耗竭。
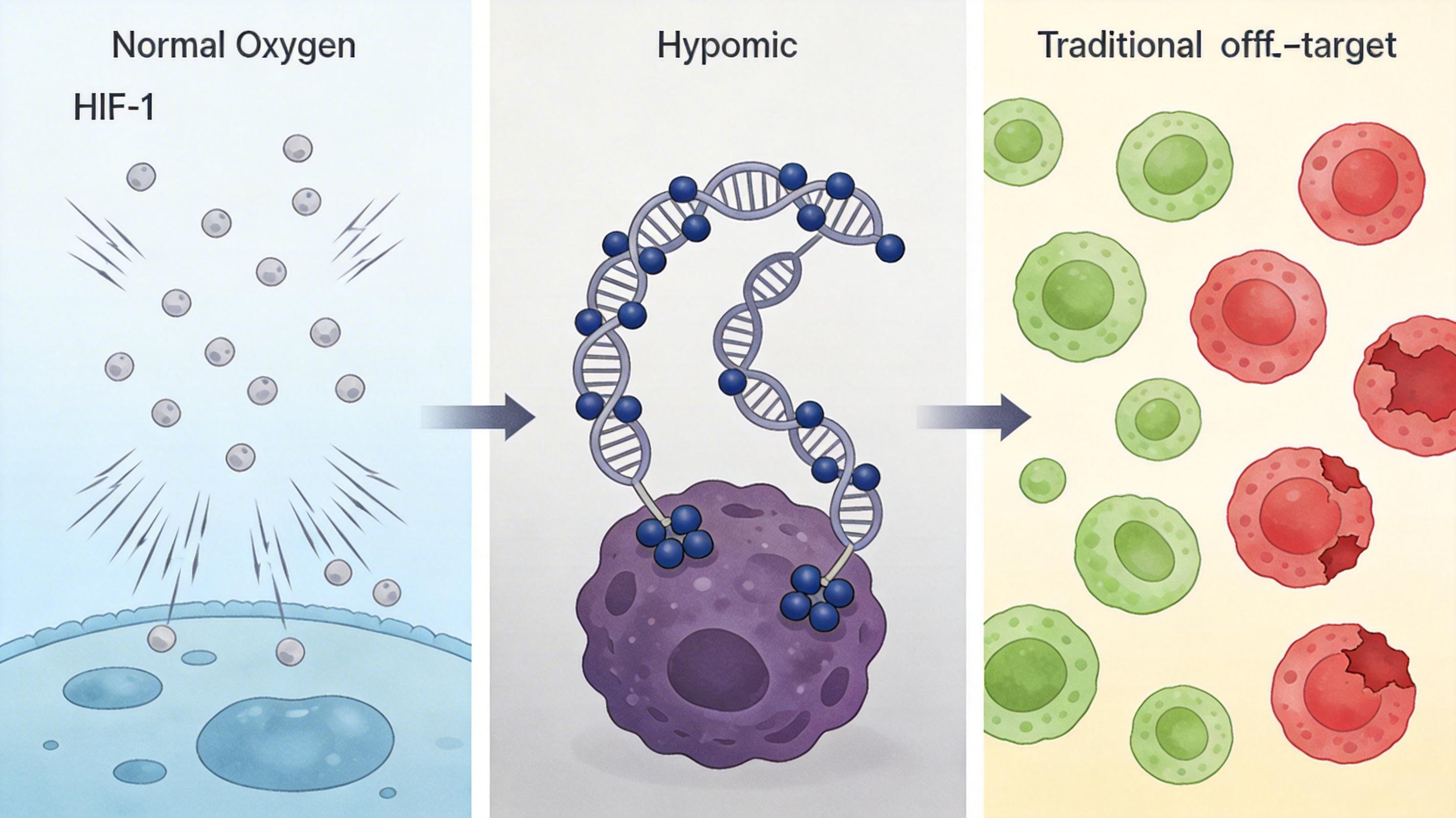
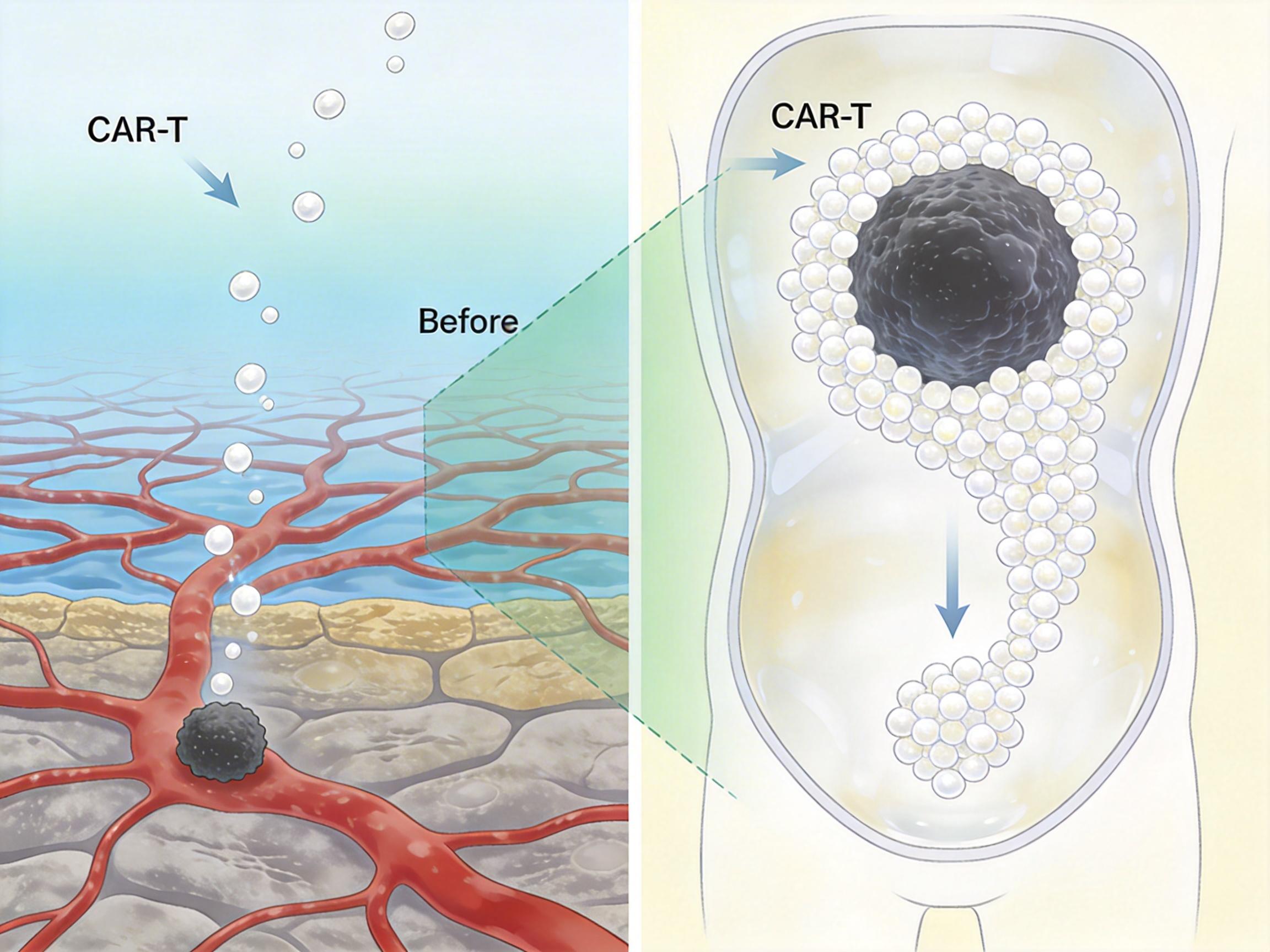
如果说低氧开关是PC13的「智能大脑」,那么腹腔输注就是它的「精准导航」。
对于腹腔转移的实体瘤患者来说,传统静脉输液的CAR-T细胞要穿过层层血管和组织屏障,最终能到达肿瘤的不到1%。就像往河里扔石头,想砸到河底的目标难上加难。而腹腔输注相当于直接把石头扔进了装着肿瘤的「鱼缸」——CAR-T细胞第一时间接触肿瘤病灶,不需要长途跋涉,还能在局部形成高浓度的免疫杀伤区。
临床数据给出了最直接的证明:在43名重度预处理的晚期患者中,腹腔输注组的客观缓解率(ORR)达到23.5%,是静脉输注组(8.0%)的近3倍;疾病控制率更是高达82.4%,意味着绝大多数患者的肿瘤不再进展。尤其是那些腹腔转移且CEA(癌胚抗原)表达超过90%的患者,缓解率居然达到了57.1%——这在过去是不敢想象的数字。
更有意思的是,腹腔输注的CAR-T细胞还能通过淋巴和血液循环进入全身,对远端转移灶产生杀伤作用,形成「局部打击,全身响应」的效果。就像在腹腔里点燃了一把免疫的火,这把火还能顺着管道烧到身体的其他部位。
我认为这是最容易被忽略的突破:它不仅是一种给药方式的创新,更是打破了「CAR-T只能静脉输液」的思维定式——对于不同部位的实体瘤,应该用不同的递送策略,而不是一刀切的静脉输注。
当然,PC13不是治愈实体瘤的万能药,它的局限同样明显。
首先,它只对CEA阳性的实体瘤有效,也就是结直肠癌、胃癌、肺癌等特定癌种;其次,肿瘤的异质性依然是难题——有些肿瘤内部的氧浓度不均匀,可能导致部分区域的CAR-T无法被激活;而且目前只是一期临床,样本量有限,长期疗效和安全性还需要更大规模的试验验证。
但它的意义在于,为实体瘤的CAR-T治疗提供了一个可复制的「智能调控+精准递送」模板:未来的CAR-T不应该是「一激活就全力输出」的莽夫,而应该是能感知肿瘤微环境、精准调整状态的「特种兵」。比如可以给CAR-T装个「pH开关」,只在肿瘤的酸性环境里激活;或者装个「酶开关」,只在肿瘤分泌特定蛋白酶的区域启动。
从产业角度看,低氧响应型CAR-T属于第四代CAR-T,是目前全球CAR-T研发的热门方向。2024年全球CAR-T市场规模约38.7亿美元,预计2034年将超过230亿美元,其中实体瘤CAR-T的增速最快——PC13的成功,无疑给这个赛道注入了一针强心剂。
当我们谈论CAR-T治疗实体瘤的突破时,我们谈论的从来都不是「又治愈了一个患者」,而是「终于找对了方向」。过去十年,我们一直在给CAR-T细胞「增压」——增加共刺激分子、增强杀伤能力,但却忽略了「精准」的重要性。
PC13的成功告诉我们:对付实体瘤,与其用蛮力攻破城墙,不如找到城门的钥匙。低氧开关就是那把钥匙,它让CAR-T从「无差别攻击」的武器,变成了「精准打击」的手术刀。
见氧行事,方得始终——这不仅是CAR-T治疗实体瘤的破局之道,更是所有精准医疗的核心逻辑。未来的癌症治疗,一定是「让药物适应肿瘤」,而不是「让患者适应药物」。
点击充电,成为大圆镜下一个视频选题!