
4 个月前

4 个月前
乳腺癌,全球女性最常见的癌症。对于患者而言,最深的恐惧并非来自原发肿瘤本身,而是它如幽灵般的转移能力。约90%的乳腺癌死亡归因于癌细胞的“远征”——它们脱离故土,潜入血液,在骨、肺、肝等远方器官建立新的“殖民地”。长久以来,我们认为这些癌细胞是孤独的流亡者。然而,一项颠覆性的发现揭示,它们或许并非孤军奋战,而是与体内本应是“卫士”的免疫细胞上演了一出致命的“无间道”。
2025年12月4日,一篇发表于国际顶级期刊《癌症研究》(Cancer Research)的论文,为我们揭开了这场惊人合作的序幕。由南方科技大学洪鑫、文飞球,中山大学何振宇及中南大学覃军领导的联合团队,在乳腺癌患者的转移组织和血液样本中,鉴定出一种前所未见的“混血”细胞亚群。这种细胞同时表达着肿瘤细胞的上皮标记物(EPCAM⁺)和一类特殊巨噬细胞的标记物(CD68⁺ TREM2⁺)。
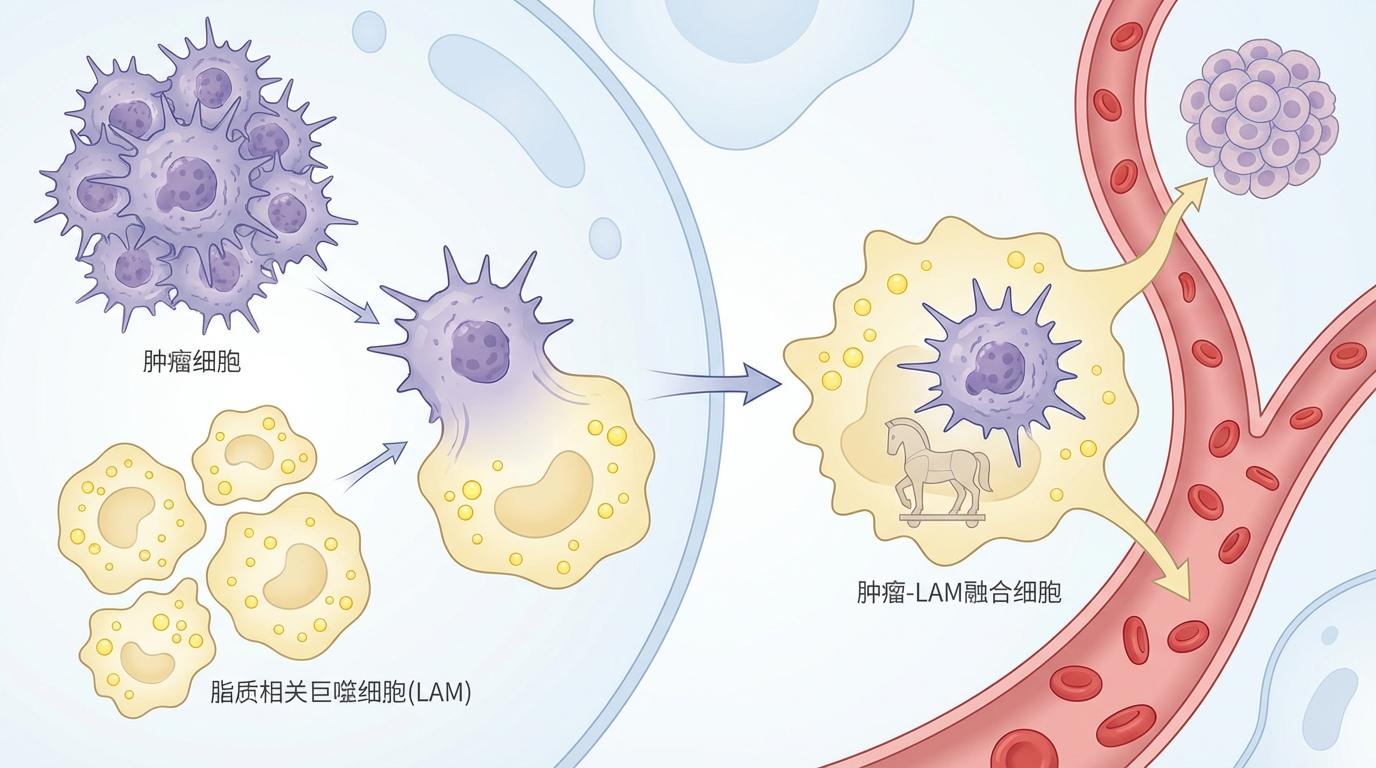
巨噬细胞,作为免疫系统的“清道夫”,本职是吞噬病原体和异常细胞。而此次发现的“脂质相关巨噬细胞”(LAM),更是一种与脂肪代谢密切相关的特殊巨噬细胞。研究表明,这种独特的细胞亚群,极有可能是肿瘤细胞与脂质相关巨噬细胞(LAM)直接融合的产物。这些“肿瘤-LAM融合细胞”如同一个完美的特洛伊木马,兼具癌细胞的无限增殖能力和巨噬细胞的强大移动与伪装能力,它们在血液或转移部位的存在,与癌症的恶性进展显著相关。
细胞间的融合,在生命世界中本是常态,例如受精卵的形成、肌肉的生长。但在癌症的阴影下,这一生理过程却被劫持,沦为恶魔的盟约。当肿瘤细胞与巨噬细胞“联姻”,产生的“混血后代”便获得了远超其任何一方亲本的破坏力。
这种融合细胞,本质上是肿瘤进化的“快车道”,它让癌细胞一步到位地获得了转移所需的多种关键能力,大大增加了治疗的难度。
更进一步,研究团队精准地破译了驱动这场致命融合的分子密码——一条名为CBX3–SNX10–ANO6的信号通路。
在这个过程中:
这条信号通路的发现,不仅从根本上解释了肿瘤细胞如何与巨噬细胞“握手言和”并最终合二为一,更重要的是,它为我们提供了一个前所未有的潜在治疗靶点。如果能切断这条通路中的任何一个环节,就有可能阻止“混血”细胞的诞生。
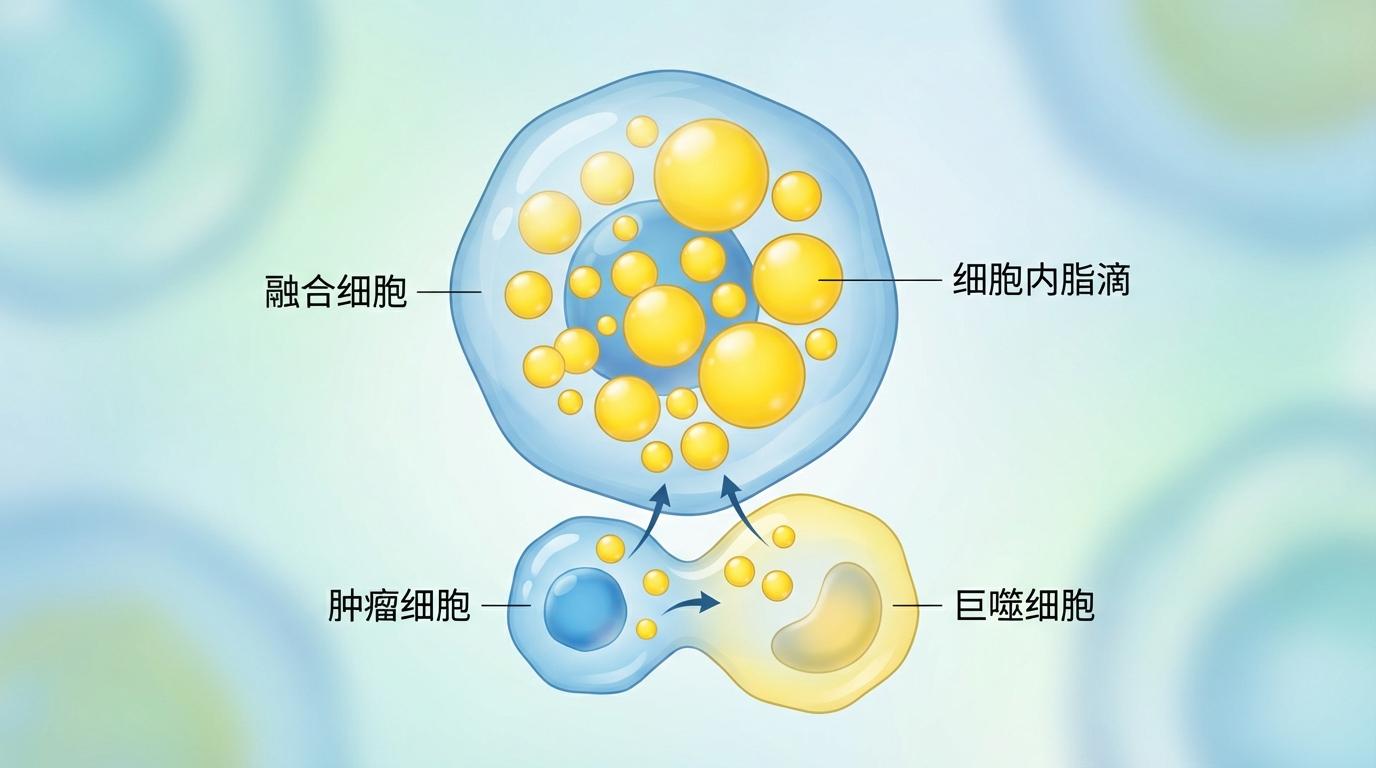
在探索如何摧毁这些危险的融合细胞时,一个意想不到的发现带来了希望。研究团队观察到,这些“肿瘤-LAM融合细胞”内部积累了大量的细胞内脂滴,这正是它们从脂质相关巨噬细胞那里继承来的一个显著特征。
这个特征,恰恰成为了它们的“阿喀琉斯之踵”。
研究人员测试了一种广泛使用的降胆固醇老药——辛伐他汀。结果令人振奋:无论是在体外培养皿中还是在小鼠体内,这些富含脂质的融合细胞对辛伐他汀都表现出高度敏感。辛伐他汀通过抑制细胞的脂质代谢通路,精准地切断了融合细胞的能量供应和生存根本,从而有效抑制了其增殖和转移能力。
这一发现意义重大,它为“老药新用”提供了强有力的科学依据,也为那些面临转移困境的乳腺癌患者,指明了一条潜在的、低成本且安全性已知的治疗路径。
从揭示“细胞融合”这一全新的转移机制,到阐明其背后的分子通路,再到发现“辛伐他汀”这一潜在的治疗策略,这项研究为我们描绘了一幅多维度抗击乳腺癌转移的希望蓝图。
当然,从实验室的突破到临床的广泛应用,仍有漫长的道路要走。未来,科学家们需要回答更多问题:
尽管挑战重重,但这一发现无疑是人类对抗癌症征途中的一个重要里程碑。它再次证明,我们对生命奥秘的每一次深入探索,都可能转化为拯救生命的强大力量。通过不断揭开癌细胞的伪装,我们终将找到直击其要害的利剑,让“转移”不再是绝望的代名词。
点击充电,成为大圆镜下一个视频选题!