对抗知识焦虑,从看懂这条开始
App 下载
五万肿瘤样本揭秘:基因的命运由环境决定
纪念斯隆凯特琳癌症中心|癌症驱动基因|肺腺癌|乳腺癌|PIK3CA基因|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
纪念斯隆凯特琳癌症中心|癌症驱动基因|肺腺癌|乳腺癌|PIK3CA基因|肿瘤学|医学健康
你或许听过“基因突变致癌”,但你一定想不到:同样一个致癌突变,在乳腺癌里是点燃肿瘤的“第一把火”,到了肺腺癌里却成了肿瘤晚期才赶来的“帮凶”。过去二十年,科学家已经发现了数百个癌症驱动基因,但始终没搞懂,为什么同一个基因在不同癌症里扮演的角色天差地别。直到美国纪念斯隆凯特琳癌症中心的团队,把五万多个肿瘤样本的基因数据摆在了一起——这一次,他们终于看清了癌症基因背后的“隐形导演”。
你可以把每个驱动基因想象成一个员工,不同的癌症类型就是不同的公司。在乳腺癌这家“公司”里,PIK3CA基因是核心创始员工,一入职就推动公司扩张(早期克隆突变);可到了肺腺癌“公司”,它只能做个后期入职的实习生,跟着大部队打打下手(晚期亚克隆突变)。
这种“职场差异”的本质,是组织微环境的选择。抑癌基因在“正规大公司”(经典癌种)里,必须彻底辞职(双等位基因失活)才能让公司出问题;但在“初创小公司”(非经典癌种)里,只要它摸鱼(单等位基因失活),公司就会乱套。
研究里最有意思的发现是BRAF基因的“变形记”:在黑色素瘤里,它是独揽大权的CEO(Class I强激活突变);到了非经典癌种里,它要么变成需要搭伙干活的合伙人(Class II二聚体突变),要么成了得靠老板赏饭吃的下属(Class III依赖RAS信号突变)。
现在很多人寄希望于免疫治疗,但这项研究给大家泼了盆冷水:就算你体内有能被免疫细胞识别的致癌突变,也得看你的HLA基因“接不接得住”。
HLA就像人体的“快递站”,负责把癌细胞的突变蛋白打包成“快递”递给免疫细胞。但研究发现,约14%的患者携带目标突变,却只有22%的人刚好有能打包这个“快递”的HLA类型。更糟的是,四分之一的患者还会出现“HLA丢失”——相当于快递站直接倒闭了,免疫细胞根本看不到癌细胞的破绽。
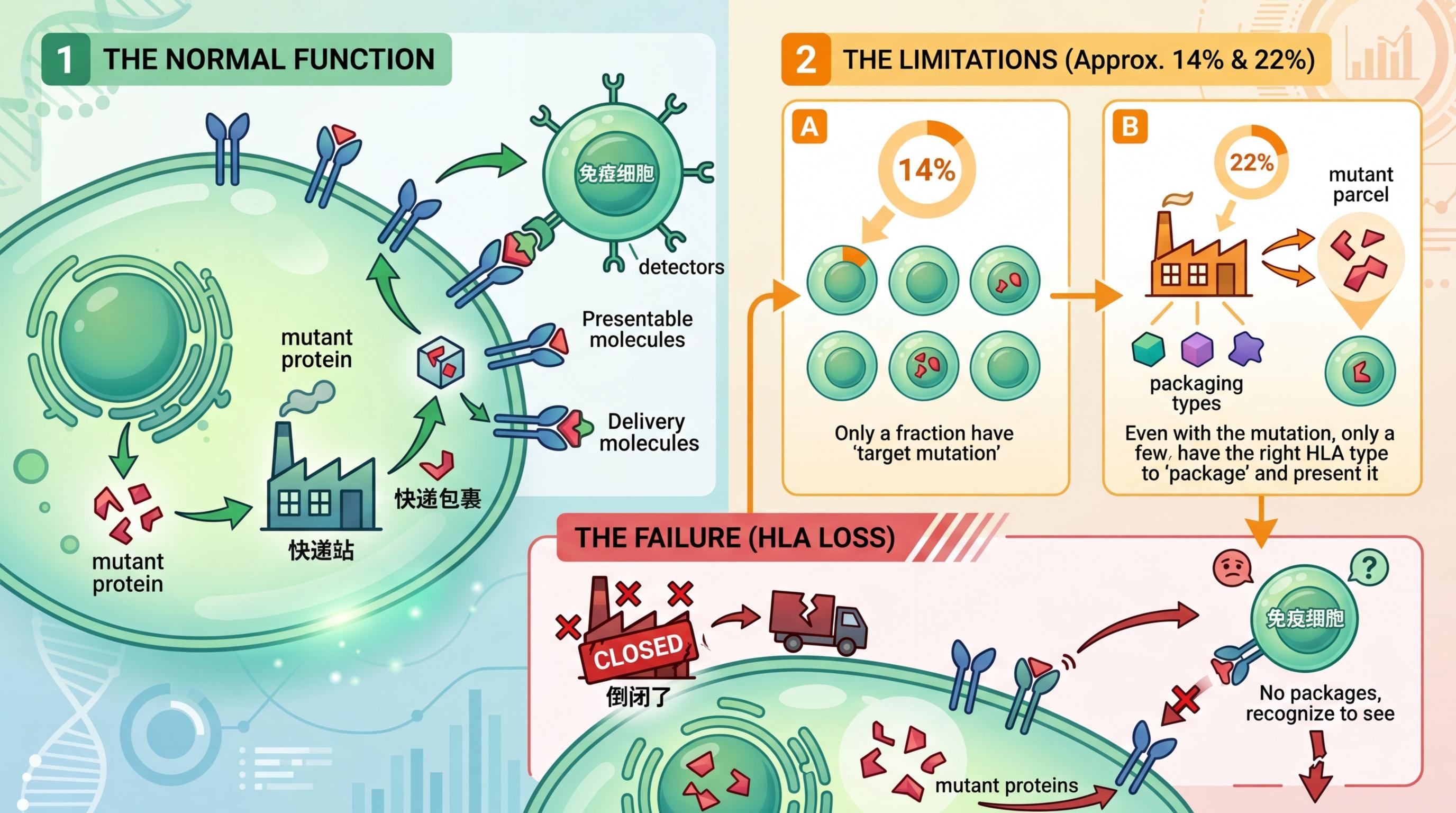
更值得警惕的是,不同种族的HLA类型差异极大,非洲裔患者符合治疗条件的比例远低于其他人种。这意味着,免疫治疗的“公平性”,还有很长的路要走。
当然,研究也带来了好消息:那些由基因融合驱动的癌症,比如ALK、RET融合,往往发病年龄更早,但对应的靶向药效果也更好——这相当于抓住了癌症的“早发把柄”。
过去我们总盯着TP53、KRAS这些“明星基因”,但这次五万样本的研究发现,癌症驱动基因里藏着一条长长的“尾巴”——那些频率低于0.1%的罕见突变,居然影响了5%的患者。
这些“长尾突变”就像职场里的隐形骨干,平时没人注意,但少了他们公司就转不动。比如RRAS2基因的G23和G24突变,在子宫内膜癌里能代替KRAS基因干活,推动肿瘤生长;而EGFR的V834L突变,会跟着经典的L858R突变一起出现,而且是肿瘤后期才“入职”,专门帮癌细胞躲避靶向药。
不过这些“长尾突变”也给精准治疗带来了麻烦:它们太小众了,很难专门为它们开发靶向药。但反过来想,如果能把这些小众突变的规律摸清楚,或许能找到通用的治疗靶点——毕竟,它们很多都在同一个信号通路上干活。
当我们把五万份肿瘤样本的基因数据铺展开来,看到的不是一个个孤立的致癌突变,而是一场场基因与环境的“博弈”。过去我们总以为找到致癌基因就能攻克癌症,现在才明白,基因的命运从来不是自己说了算的——它所在的“土壤”,才是决定它是“恶魔”还是“过客”的关键。
基因的致癌性,从来都是“环境产物”。 未来的癌症治疗,不会再是“一种突变对应一种药”的简单配对,而是要像给病人量身定制衣服一样,把基因、组织微环境、免疫状态甚至种族背景全部考虑进去。这或许很难,但五万份样本告诉我们:只有看清癌症的全貌,我们才能真正接近治愈的可能。