对抗知识焦虑,从看懂这条开始
App 下载
胰岛素没失灵,是肝脏里的酶被偷偷激活了
氧化修饰|肝脏葡萄糖代谢|活性氧|p-GSK-3β酶|代谢内分泌疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
氧化修饰|肝脏葡萄糖代谢|活性氧|p-GSK-3β酶|代谢内分泌疾病|医学健康
你有没有过这种经历:明明刚吃了饭,没过多久又觉得饿,测血糖却发现数值高得离谱?这可能不是你的胰岛素“偷懒”了——中国医学科学院黄波团队的最新研究显示,在脂肪肝、糖尿病早期,肝脏里的胰岛素信号通路其实还好好的,真正搞鬼的是一种本该“休眠”的酶。
当我们摄入高油高脂食物,肝脏里的活性氧(ROS)会悄悄给这种叫p-GSK-3β的酶做个“氧化修饰”,把它从沉睡状态拽回工作岗位。被激活的p-GSK-3β会同时干两件坏事:一边阻止肝脏把多余葡萄糖存成糖原,一边逼着肝脏拼命合成新的葡萄糖。为什么这种“背叛”会发生?我们得从肝脏的日常工作说起。
你可以把肝脏想象成家里的糖罐管理员:饭后血糖升高,胰岛素就像老板发来的指令,让管理员把多余的葡萄糖倒进糖罐(合成糖原),同时关掉“自制葡萄糖”的机器(糖异生);等到饿肚子的时候,管理员又会打开糖罐(糖原分解)和机器,维持血糖稳定。
糖原合酶激酶3β(GSK-3β)就是管理员手里的“开关”:正常情况下,胰岛素会通过AKT信号让这个开关的Ser9位点磷酸化,变成失活的p-GSK-3β——相当于把“存糖”按钮按下,“产糖”按钮锁死。这时候肝脏乖乖存糖,不会乱产葡萄糖。
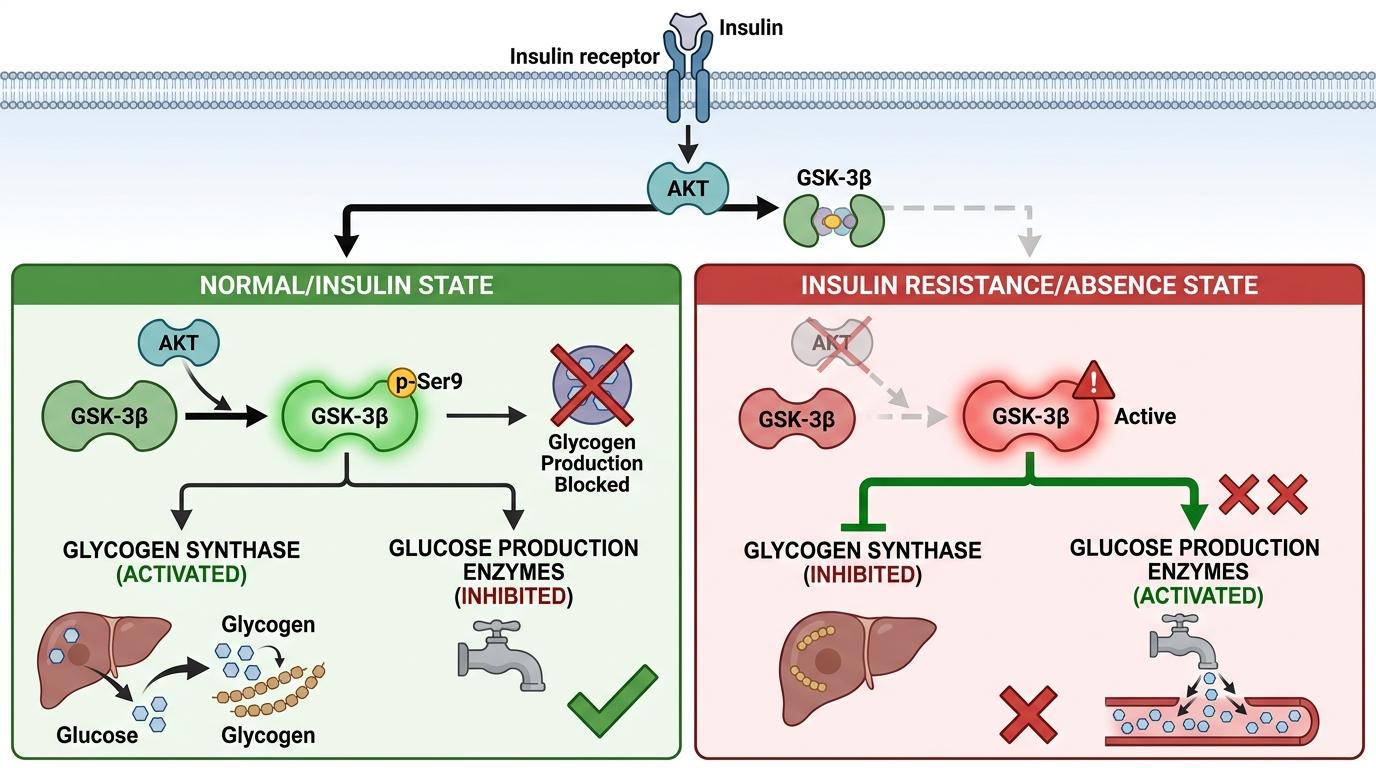
但当我们长期吃高油高脂食物,肝脏里的线粒体就会“喘不过气”,产生大量活性氧(ROS)。这些ROS不是只会搞破坏的“自由基”,它们会精准地找到p-GSK-3β上的半胱氨酸178位点,给它做个亚磺酰化修饰——就像用一把特制钥匙,把被锁死的“产糖”开关又拧开了,同时还把“存糖”按钮给按回了原位。
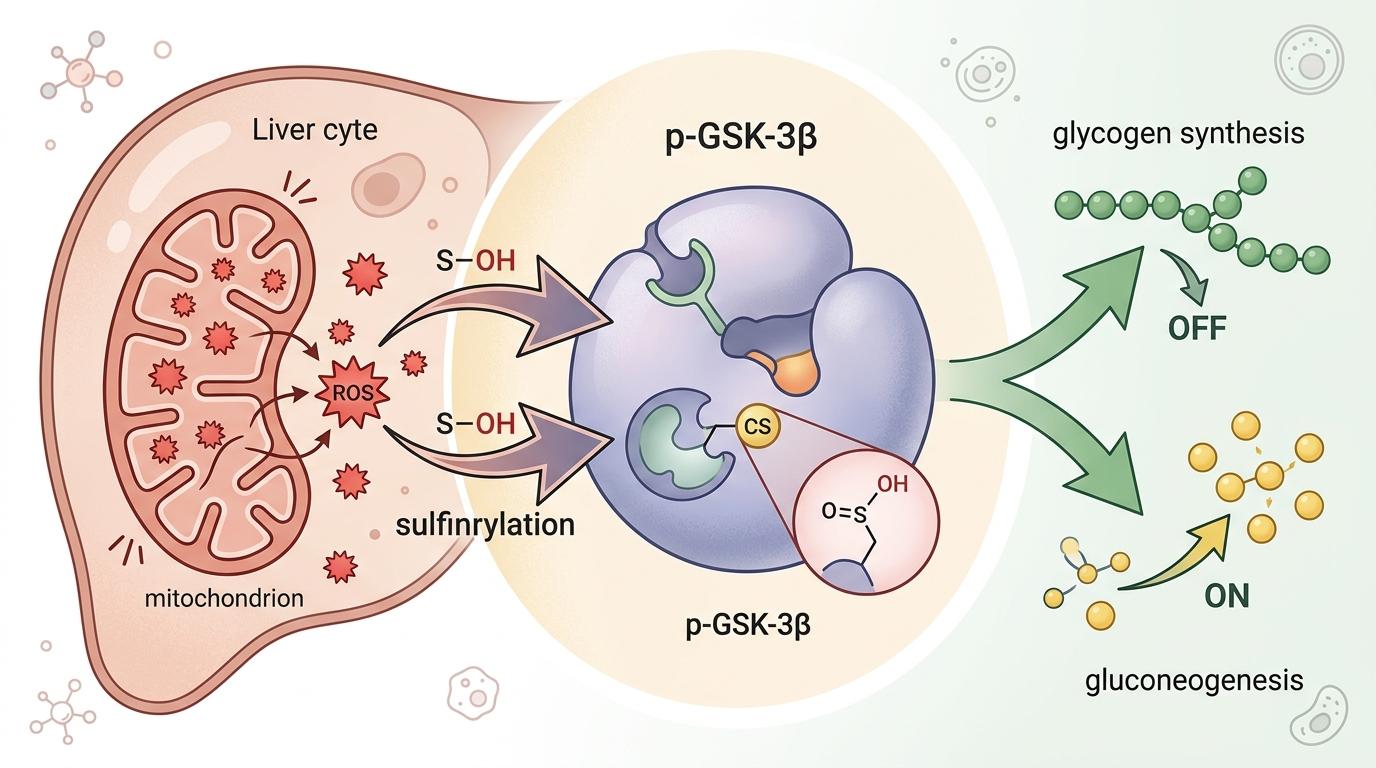
被亚磺酰化修饰后的p-GSK-3β,彻底背叛了胰岛素的指令:
更关键的是,这一切发生的时候,经典的胰岛素信号通路(IR-IRS-PI3K-AKT)还没受损——相当于老板的指令还在正常传递,但管理员已经偷偷换了执行方案。这也解释了为什么很多人在高脂饮食早期,血糖已经不稳定,但胰岛素水平还正常,甚至偏高。
研究团队用质谱技术精准定位了这个被修饰的半胱氨酸位点,又通过基因编辑把这个位点改成不能被氧化的丙氨酸(C178A),结果发现,就算在高脂饮食下,肝脏也能乖乖响应胰岛素,不再乱产葡萄糖。这个实验直接坐实了:p-GSK-3β的亚磺酰化,就是肝脏胰岛素抵抗的“分子开关”。
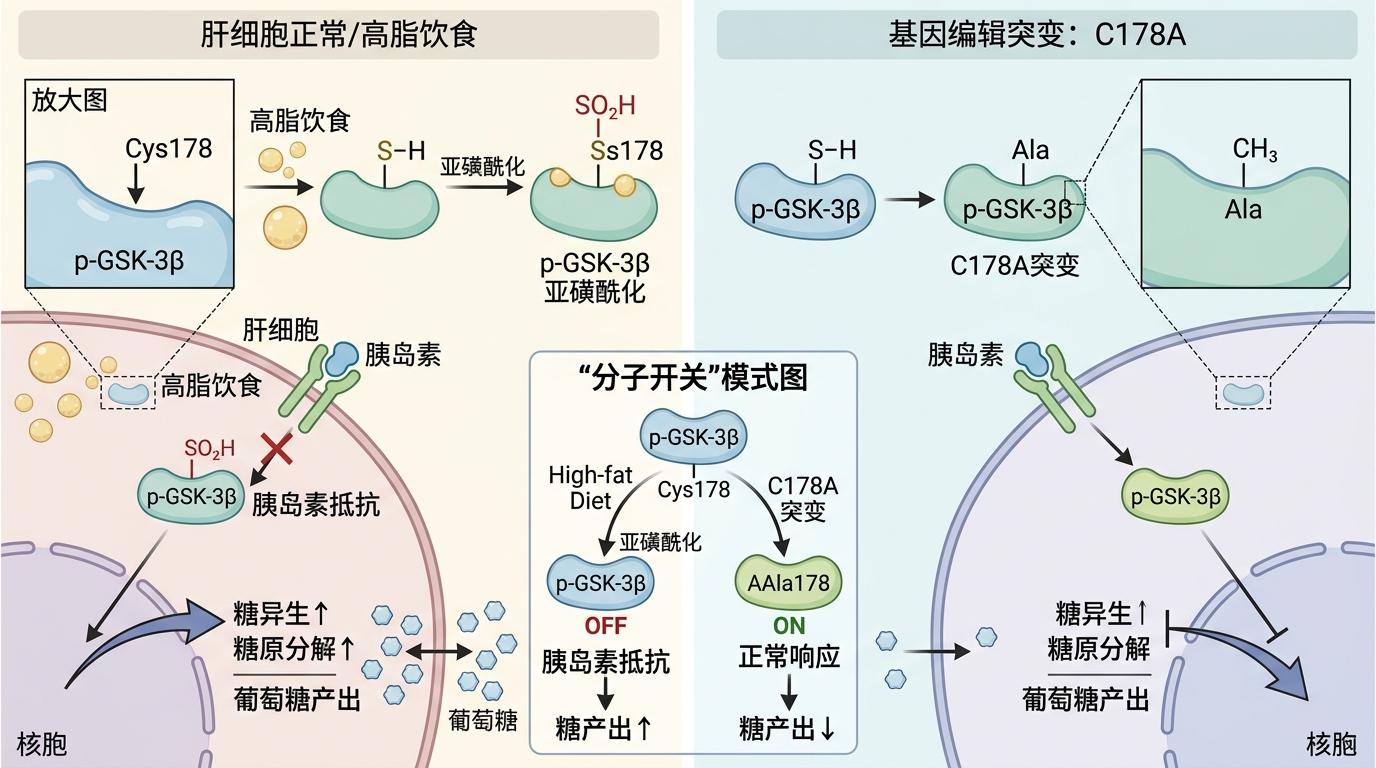
这个发现最直接的意义,是给代谢病治疗找到了新的精准靶点。之前的GSK-3β抑制剂都是针对酶的活性位点,容易“不分好坏”地抑制所有GSK-3β,带来脱发、血糖异常等副作用;而如果能开发出只针对“亚磺酰化p-GSK-3β”的抑制剂,就能精准关掉那个被偷偷激活的“坏开关”,不影响正常的酶功能。
当然,这条路还有不少坎要过:比如怎么精准检测人体内的亚磺酰化p-GSK-3β水平,怎么保证抑制剂只结合被氧化的酶,而不干扰其他正常蛋白。另外,活性氧的“双重身份”也得注意——它不是完全的“坏东西”,少量的ROS是细胞正常信号传导的一部分,直接用强抗氧化剂“一刀切”,可能反而会打乱细胞的正常代谢。
值得一提的是,研究团队还在人类肝脏样本和类器官中验证了这个机制的保守性,意味着这个靶点不仅在小鼠身上有效,在人类身上也很可能适用——这为后续的药物研发打下了扎实的基础。
我们总以为代谢病是“胰岛素不够用”或者“细胞不听指挥”,但黄波团队的研究让我们看到:有时候不是信号断了,而是信号被偷偷篡改了。肝脏里这个小小的酶修饰,就像蝴蝶效应的起点,最终引发了血糖紊乱、脂肪肝甚至糖尿病。
氧化不是只有损伤,更是精准的信号调控。 这个发现不仅刷新了我们对肝脏代谢的认知,更提醒我们:对付代谢病,不能只盯着“胰岛素”这一个靶点,得深入到细胞内部,找到那些被悄悄操控的“分子开关”。未来,或许我们真的能开发出一种药,精准地把那个被激活的坏酶重新“催眠”,让肝脏回到它该有的工作节奏里。