对抗知识焦虑,从看懂这条开始
App 下载
新疆发现H11禽流感,已悄悄感染牛羊
新疆枢纽|候鸟迁徙路线|牛羊感染|石河子大学|H11亚型禽流感|生物多样性|感染性疾病|生命科学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
新疆枢纽|候鸟迁徙路线|牛羊感染|石河子大学|H11亚型禽流感|生物多样性|感染性疾病|生命科学|医学健康
当我们还在紧盯H5N1的跨物种传播时,另一种禽流感已经悄悄完成了跨界渗透。2026年4月,石河子大学团队的研究撕开了这个隐秘的口子:在新疆,H11亚型禽流感不仅已在鸡群中隐秘传播——当地家禽血清阳性率最高达65%,更罕见地在牛和骆驼体内检测到了病毒抗体。这是H11病毒自然感染哺乳动物的直接证据,而新疆,这个欧亚候鸟迁徙的十字路口,正是这场病毒隐秘扩散的关键枢纽。为什么偏偏是新疆?H11又藏着怎样的跨物种密码?
你可以把候鸟迁徙路线想象成空中的洲际高速公路,而新疆就是连接东亚、南亚与欧洲、非洲的超级换乘站——每年春秋,数百万只候鸟在这里停歇、觅食,同时也完成了病毒的“接力传递”。
研究人员分析了全球1179条H11病毒的HA基因序列,发现它的扩散轨迹完全贴合候鸟迁徙路线:从南亚的越冬地北上,在新疆完成基因重组和种群扩增,再向西飞向欧洲、中东和非洲。新疆分离出的两株H11病毒,基因片段分别来自中国、韩国、意大利、蒙古甚至南极洲——就像带着多国护照的旅行者,每一段基因都标记着它的迁徙足迹。
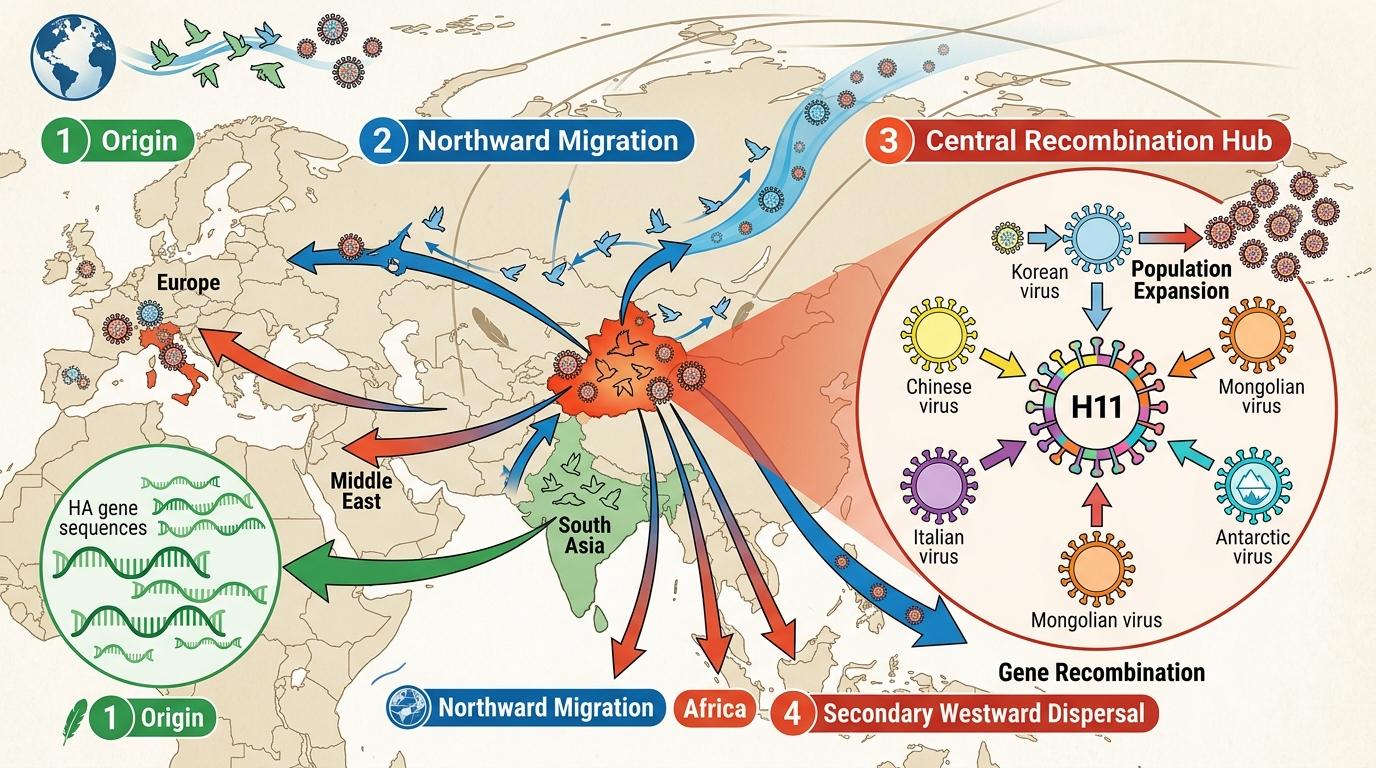
其中BL0/H11N3的PA基因片段,直接匹配南极分离株的序列。这意味着,一只可能从未踏足南极的候鸟,通过沿途的基因交换,把南极的病毒片段带到了新疆。这种跨洲际的基因流动,正是禽流感病毒演化出跨物种能力的核心动力。
H11病毒的跨物种潜力,藏在它的基因重组能力里。你可以把病毒的8个基因片段想象成8个独立的零件,候鸟就像移动的“零件交换站”——当不同亚型的禽流感病毒在同一只候鸟体内相遇,它们会随机交换零件,组装出全新的病毒株。
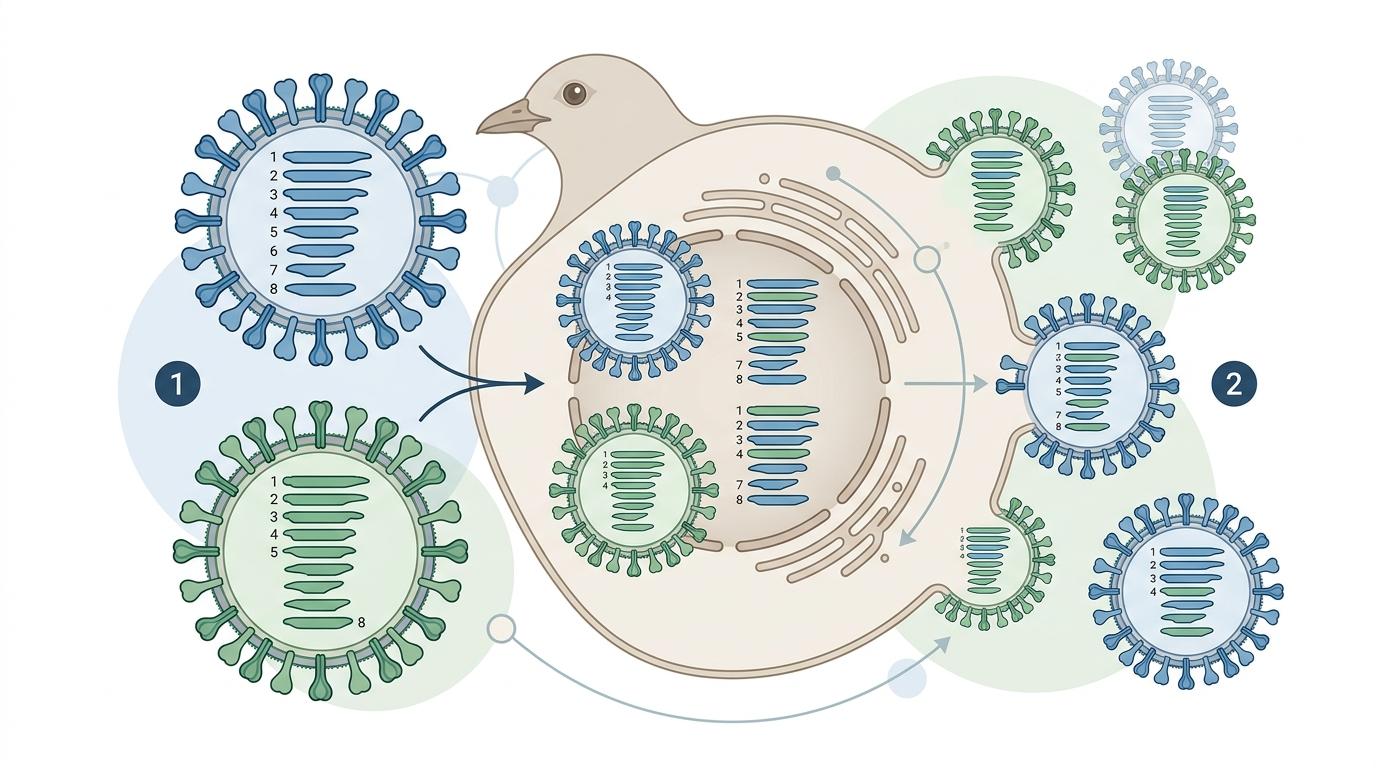
新疆分离的K77/H11N2就是个典型的“混血儿”:它的PB2基因来自韩国的H10N7,NP基因来自中国的H5N6,M基因则来自俄罗斯的H11N9。更关键的是,它还携带了PB2-I292V、NP-52H/313F等突变——这些被称为“哺乳动物适应性标记”的突变,能让病毒在哺乳动物细胞里更高效地复制。
实验室数据更直接:K77/H11N2不仅能在鸡的肺、肾、肠道等器官里全身复制,还能在人肺腺癌细胞(A549)中中等程度复制,甚至能引起小鼠肺部的局部炎症。而另一株没有这些突变的BL0/H11N3,在哺乳动物细胞里几乎无法复制。
这就是基因重组的可怕之处:它能让原本只感染鸟类的病毒,突然获得感染哺乳动物的能力。
新疆的牛和骆驼体内检测到H11抗体,这是最值得警惕的信号——它意味着病毒已经突破了鸟类和哺乳动物的物种屏障,完成了“溢出”。
这些牛羊并没有出现明显的临床症状,就像鸡群感染H11后也只是“无症状携带者”——这种隐匿性传播,恰恰是防控的最大难点。当病毒在哺乳动物体内悄悄适应,就可能在某个不经意的时刻,演化出能在人类中传播的能力。
家鸭在这场传播中扮演了关键的“桥梁角色”。研究发现,家鸭是H11病毒传播网络的核心,它能把病毒传给野生鸟类、鸡、鹅,甚至通过粪便污染环境,让牛羊间接接触感染。新疆家禽65%的血清阳性率,说明病毒已经在当地家禽中形成了稳定的传播链,而这正是病毒向哺乳动物扩散的“蓄水池”。
更现实的问题是:我们对H11的监测几乎是空白。此前国内的H11病毒主要集中在东部省份,新疆的发现直接填补了西部的监测盲区,但也暴露了一个更大的隐患:那些候鸟迁徙的枢纽地带,还有多少未被发现的病毒亚型?
当我们把目光聚焦在高致病性禽流感上时,低致病性的H11正在悄悄完成它的演化积累。新疆的发现,不是一个孤立的事件,而是全球禽流感跨物种传播的一个缩影——候鸟的翅膀没有国界,病毒的演化也不会停下脚步。
病毒的跨界传播,从来不是突然发生的“跳跃”,而是一次次隐秘的“试探”:先在鸟类中传播,再通过基因重组获得适应哺乳动物的能力,最后悄悄感染哺乳动物,完成物种屏障的突破。
候鸟不停歇,病毒不止步。 这场与病毒的赛跑,我们需要的不只是紧盯已知的高致病性亚型,更要在那些候鸟迁徙的十字路口,提前布下监测的网——因为下一次病毒的“跳跃”,可能就藏在某只候鸟的粪便里,某个牛羊牧场的血清样本中。