
9 天前

9 天前
你有没有过这样的时刻:久坐起身时腰突然僵得像块石板,弯腰系鞋带都要咬着牙缓半天?这种困扰全球2.66亿人的腰痛,大多背后藏着同一个元凶——椎间盘退变。70岁以上人群里,90%的人都有不同程度的椎间盘老化,可医生能做的往往只是止疼、理疗,或是最后一步的手术。直到陆军军医大学的团队在《Advanced Science》上发表的研究,终于把这层藏了几十年的窗户纸捅破:椎间盘的衰老,可能是被细胞里的一个「表观遗传开关」悄悄关掉了活力。
要理解这个开关,得先搞懂一个叫H3K4me3的东西——你可以把它看成细胞基因上的「活力贴纸」,贴得越多,负责细胞增殖、代谢的基因就越活跃。研究团队对比了121例患者的椎间盘组织后发现:退变的椎间盘里,这种「活力贴纸」的数量足足少了一大半。
为了确认不是巧合,他们用了更狠的办法:给细胞用了H3K4me3抑制剂,结果原本好好的髓核细胞立刻开始「躺平」——增殖变慢,衰老标记物翻倍,DNA损伤也跟着增加。这就像把工厂里的动力开关关了一半,机器自然越转越慢。
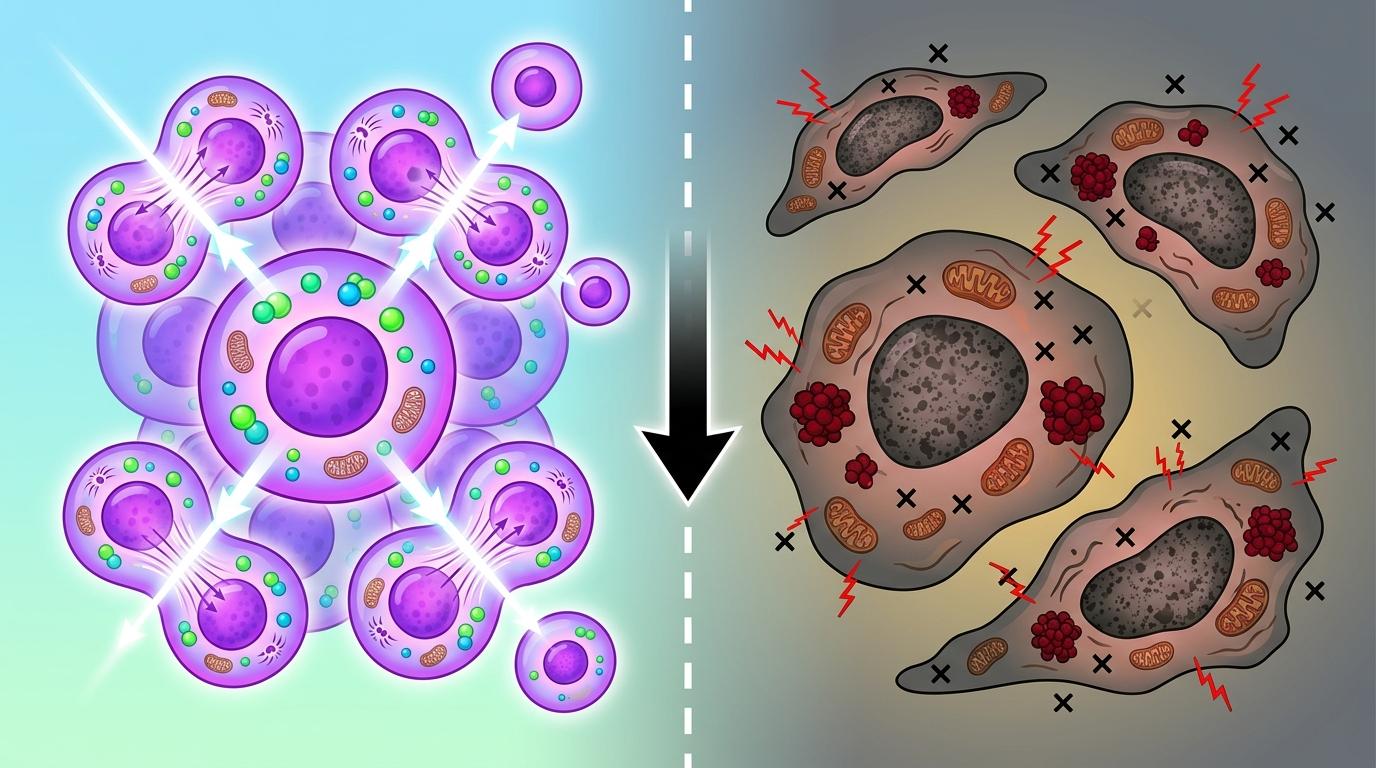
而负责贴这些「活力贴纸」的「工人」,就是SETD1A——一种专门给基因贴H3K4me3的酶。退变的椎间盘里,SETD1A的含量也跟着H3K4me3一起降,两者就像同一条船上的人,一损俱损。
科学家们接着往下挖,终于揪出了一整条从「开关失灵」到「细胞罢工」的连锁反应链:
当SETD1A减少,H3K4me3这个「活力贴纸」就没法贴在HELZ2基因的启动区——这个基因就像细胞里的「代谢调度员」,负责和PPARα组成搭档,调控细胞的能量供应。
HELZ2一罢工,搭档PPARα也跟着歇菜,直接导致下游的HIF1α含量暴跌。HIF1α是什么?它是髓核细胞的「能量总司令」——因为椎间盘里没有血管,细胞只能靠无氧糖酵解供能,而HIF1α就是指挥这条生产线的核心。
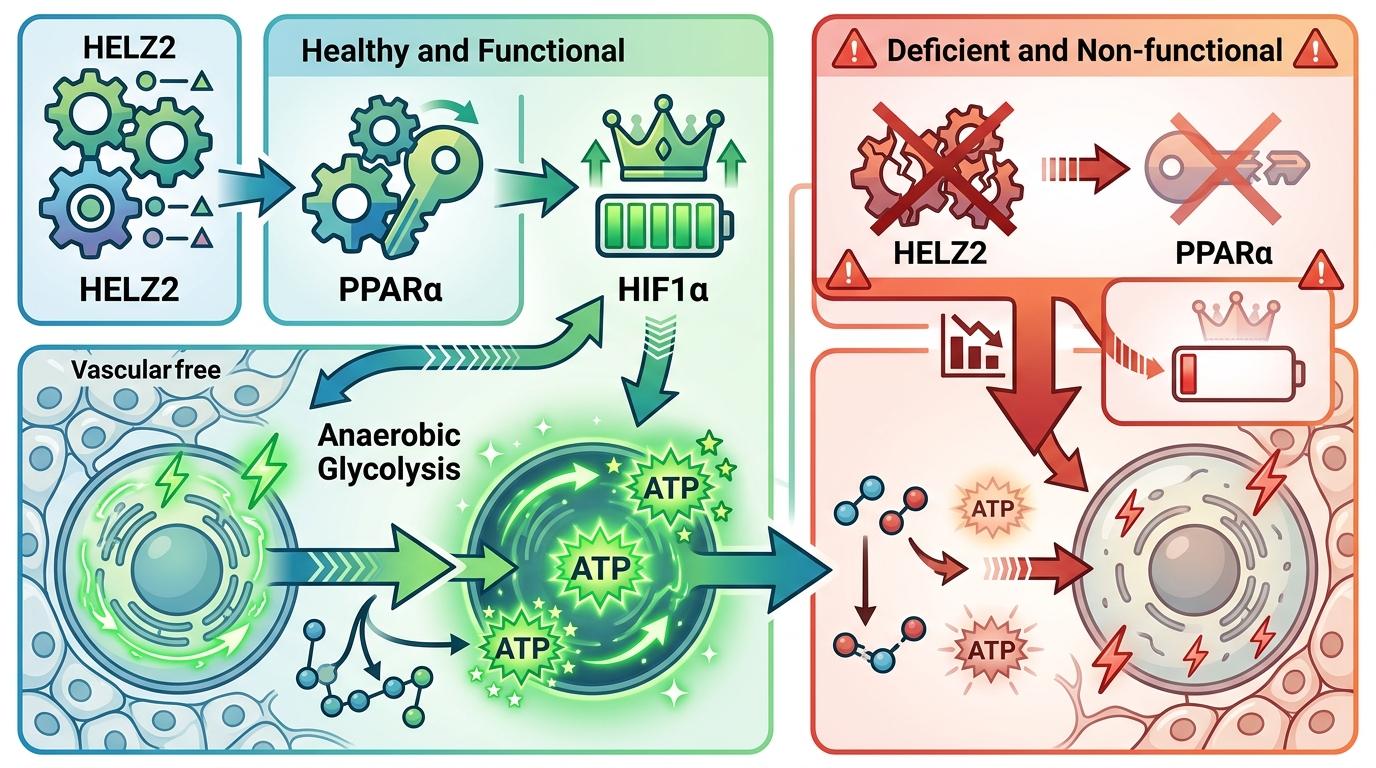
HIF1α一缺,糖酵解生产线直接停摆:细胞里的ATP含量降了,葡萄糖用不起来,乳酸也排不出去,就像工厂断了电,机器彻底转不动,细胞只能一步步走向衰老。
他们在小鼠身上验证了这个逻辑:敲掉SETD1A的小鼠,椎间盘高度明显降低,纤维化程度翻倍;而给小鼠过表达SETD1A,椎间盘的老化进程居然被硬生生放慢了。
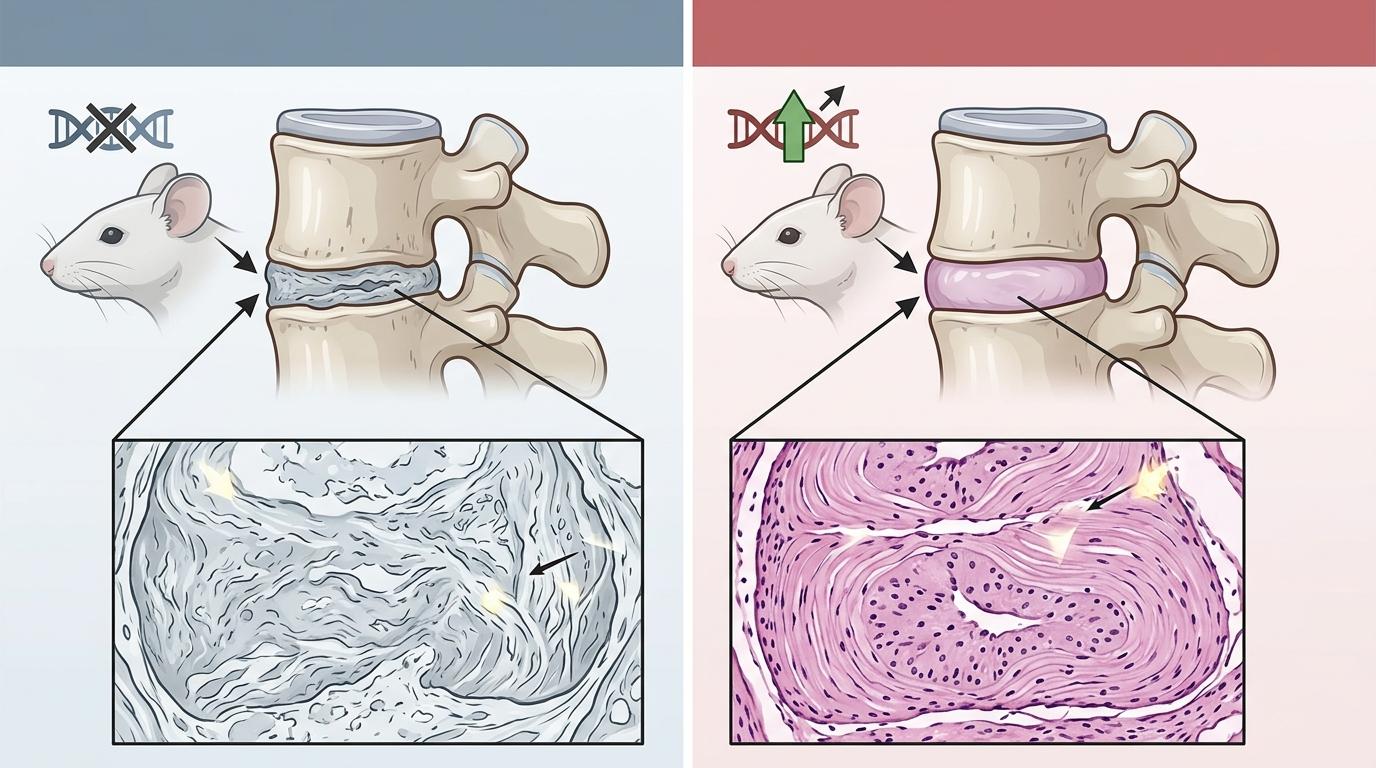
当然,这项研究也不是完美的。目前所有的验证都还停留在细胞和动物实验阶段,要用到人身上,还有好几道坎要跨:比如怎么精准地给椎间盘里的细胞补充SETD1A,怎么避免脱靶效应,还有长期使用的安全性问题。
更重要的是,椎间盘退变是个多因素问题——遗传、肥胖、长期弯腰劳作都会推波助澜,SETD1A这条通路只是其中的一个关键环节,不是唯一的答案。但它的意义在于,第一次把表观遗传和细胞代谢这两条线连了起来,给过去只能「治标」的腰痛治疗,提供了一个「治本」的新方向。
比如未来可能会出现针对SETD1A的激活剂,或者用基因编辑技术直接修复这个「开关」,甚至用外泌体把SETD1A递送到椎间盘里——这些现在听起来还像科幻的想法,已经有了初步的实验基础。
我们总以为腰背痛是「用坏了的零件」,只能修或者换,但这项研究告诉我们:有些「老化」其实是「开关失灵」,只要找到那个藏在细胞里的开关,就有可能重新激活细胞的活力。
「衰亡不是必然,而是可以调控的进程。」这句话放在细胞里成立,放在我们的身体上,或许也有新的启示。未来的某一天,当我们再遇到腰痛,医生可能不会只开止疼药,而是会给我们的细胞「开个开关」——想想就让人期待。
点击充电,成为大圆镜下一个视频选题!