对抗知识焦虑,从看懂这条开始
App 下载
口腔常驻菌竟促肠癌,关键靶点已找到
LPBDCP蛋白|结直肠癌|华中科技大学|Gemella morbillorum|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
LPBDCP蛋白|结直肠癌|华中科技大学|Gemella morbillorum|肿瘤学|医学健康
你或许从未听说过Gemella morbillorum——一种原本安分待在口腔和肠道里的普通球菌,平时顶多在免疫力低下时引发点轻微感染。但华中科技大学的最新研究把它推到了聚光灯下:这种看似无害的共生菌,竟是推动结直肠癌的隐秘推手。更关键的是,科学家不仅揪出了它,还精准锁定了它作案的「钥匙」和「凶器」——这意味着我们终于有了从源头打断它致癌路径的可能。这种平时不起眼的细菌,到底是怎么悄悄把健康肠道细胞拖向癌变的?
你可以把肠道细胞想象成一间锁好的屋子,而G. morbillorum身上带着一把特制的「钥匙」——LPBDCP蛋白。这把钥匙能精准插进肠道细胞表面的「锁孔」TMEM140蛋白里,两者一结合,就像触发了开门密码,细菌直接钻进细胞内部。
但真实的机制比这更精确:LPBDCP和TMEM140的结合会引发肠道细胞内钙离子浓度骤升,这种信号变化会下调一种叫RASA4的蛋白。而RASA4本来是细胞里的「刹车」,专门抑制Ras信号通路的过度激活。刹车失灵后,Ras通路彻底失控,一方面通过PI3K-AKT-NF-κB通路让细胞疯狂增殖、逃避死亡,另一方面通过RAF-MEK-ERK通路加速细胞周期,让正常细胞一步步滑向恶性。
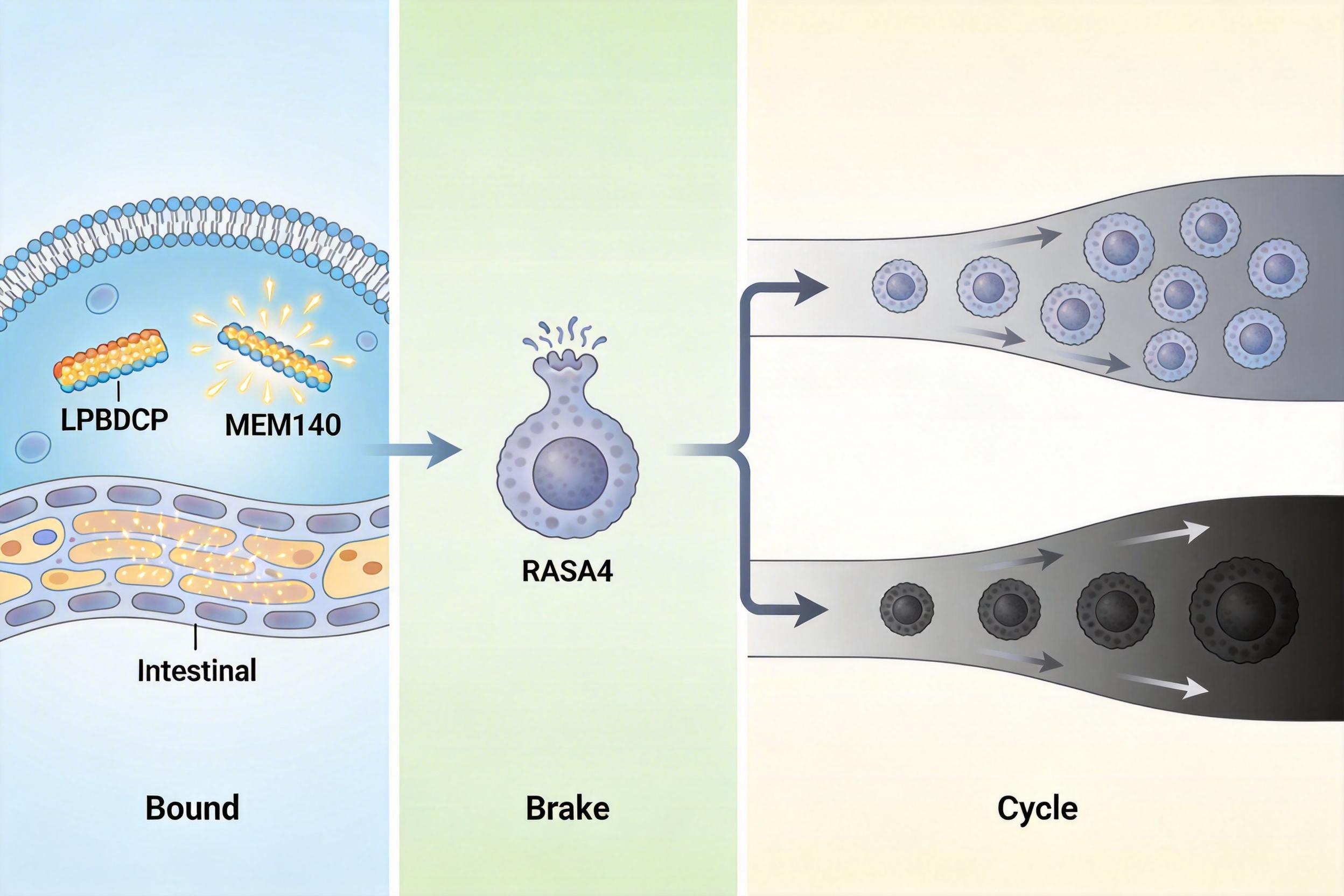
更狠的是,钻进细胞的G. morbillorum还会分泌另一种「凶器」——NDPD蛋白。这种蛋白会给细胞里的「抑癌卫士」p53做一次致命的「去乙酰化手术」,让p53失去稳定性被快速降解。没有了p53的监管,癌细胞就像脱缰的野马,彻底摆脱了「出错就凋亡」的约束。
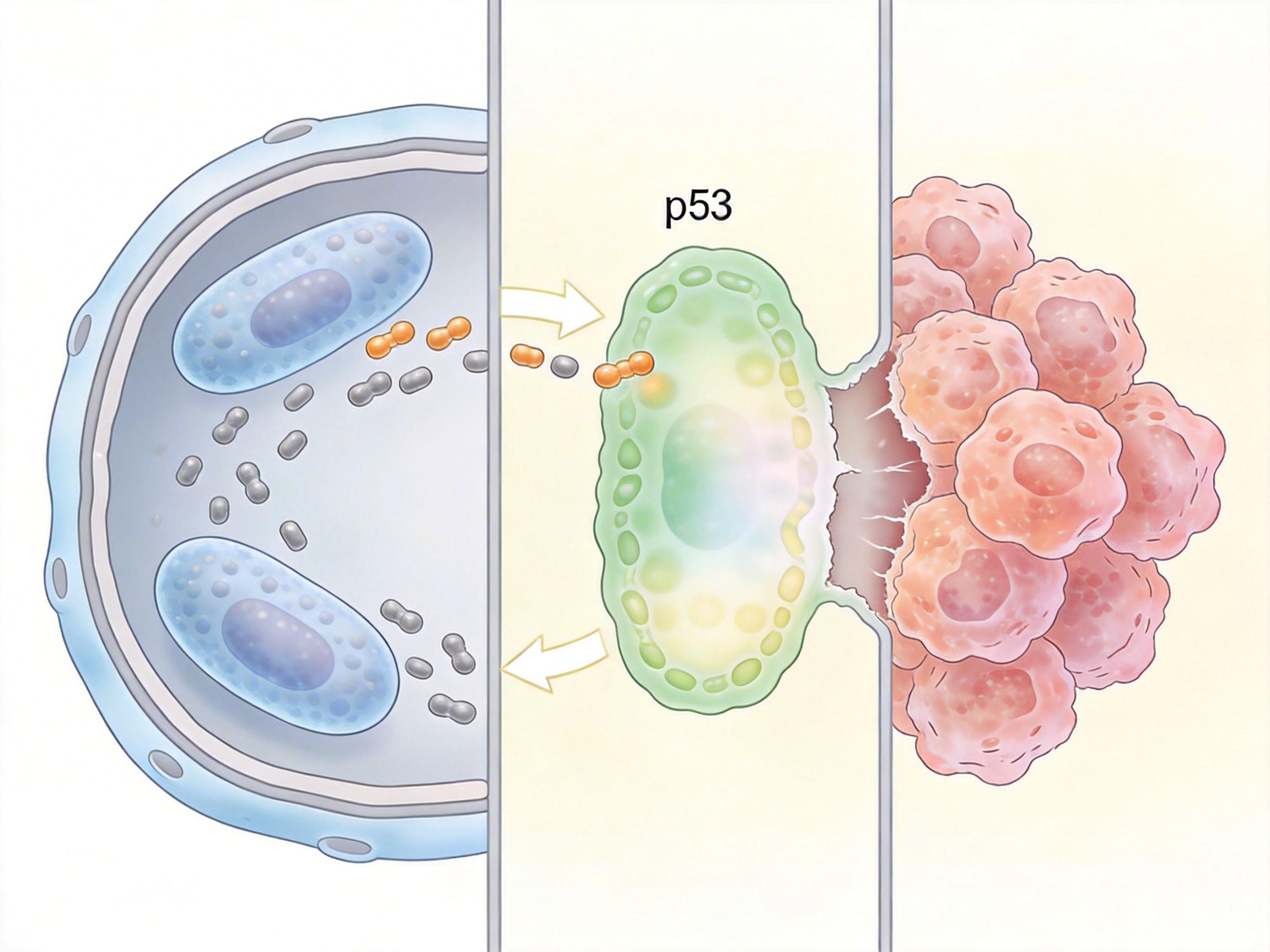
在肠道致癌菌的「黑名单」里,G. morbillorum的作案手法算得上独树一帜。
比如同样从口腔跑到肠道的具核梭杆菌,靠的是黏附在肿瘤细胞表面激活炎症通路,更像在细胞外「煽风点火」;而产肠毒素脆弱拟杆菌是靠分泌毒素破坏肠道屏障,引发慢性炎症间接促癌。但G. morbillorum不一样,它直接「破门而入」,在细胞内部同时操控增殖信号和抑癌蛋白,相当于既给细胞踩油门,又拆了刹车。
更值得关注的是,这种直接侵入的机制让它的致癌性有了明确的「开关」:只要敲除细菌身上的LPBDCP,或者让肠道细胞的TMEM140失活,G. morbillorum就再也钻不进细胞,它的致癌能力也会彻底消失。在小鼠实验里,敲除了LPBDCP的G. morbillorum不仅不能促癌,甚至连基本的细胞侵入都做不到。这和其他致癌菌复杂的调控机制比,干预靶点清晰得像明牌。
当然,这项研究离真正的临床应用还有距离。首先,G. morbillorum只是肠道致癌菌群中的一员,单独清除它未必能完全阻断肠癌的发生——肠道菌群是个复杂的生态系统,一种细菌的减少可能会让其他致病菌趁机繁殖。
其次,直接靶向TMEM140可能存在风险:这种蛋白不仅是细菌的「锁孔」,本身也参与正常肠道细胞的增殖调控,盲目抑制可能影响肠道的正常功能。而针对NDPD的抑制剂研发,也需要解决特异性问题,避免影响人体自身的去乙酰化酶。
不过,它带来的启发已经足够重要:以往我们总把肠道致癌菌的作用归结为炎症或代谢产物,G. morbillorum的发现让我们看到,细菌还能直接侵入细胞、操控核心癌基因。这为肠癌的预防和治疗打开了新的思路——或许未来我们能通过检测粪便中G. morbillorum的丰度,提前预警肠癌风险;也可能开发出专门阻断LPBDCP和TMEM140结合的药物,从源头切断这种细菌的致癌路径。
我们总把癌症看作细胞自身的叛变,却常常忽略了那些藏在体内的「外部帮凶」。G. morbillorum的发现,再次提醒我们肠道菌群这个「隐形器官」的力量——它们不是无关紧要的共生者,而是能直接改写细胞命运的参与者。
「菌群小,可撬动癌的大齿轮」。未来的癌症治疗,或许不再只盯着癌细胞本身,而是会把目光投向那些藏在我们体内的微小生命,从调控生态系统开始,重新定义抗癌的边界。